„Mukoviszidose“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Kuebi (Diskussion | Beiträge) →Symptomatische Behandlung: +Osteo |
Kuebi (Diskussion | Beiträge) →Einzelnachweise: +Quellen |
||
| Zeile 301: | Zeile 301: | ||
<ref name="PMID24429096">M. P. Boyle, K. De Boeck: ''A new era in the treatment of cystic fibrosis: correction of the underlying CFTR defect.'' In: ''The Lancet. Respiratory medicine.'' Band 1, Nummer 2, April 2013, {{ISSN|2213-2600}}, S. 158–163, {{DOI|10.1016/S2213-2600(12)70057-7}}, PMID 24429096 (Review).</ref> |
<ref name="PMID24429096">M. P. Boyle, K. De Boeck: ''A new era in the treatment of cystic fibrosis: correction of the underlying CFTR defect.'' In: ''The Lancet. Respiratory medicine.'' Band 1, Nummer 2, April 2013, {{ISSN|2213-2600}}, S. 158–163, {{DOI|10.1016/S2213-2600(12)70057-7}}, PMID 24429096 (Review).</ref> |
||
<ref name="PMID24517344">S. V. Raju, J. H. Tate u. a.: ''Impact of heterozygote CFTR mutations in COPD patients with chronic bronchitis.'' In: ''Respiratory research.'' Band 15, 2014, {{ISSN|1465-993X}}, S. 18, {{DOI|10.1186/1465-9921-15-18}}, PMID 24517344, {{PMC|3925354}}.</ref> |
<ref name="PMID24517344">S. V. Raju, J. H. Tate u. a.: ''Impact of heterozygote CFTR mutations in COPD patients with chronic bronchitis.'' In: ''Respiratory research.'' Band 15, 2014, {{ISSN|1465-993X}}, S. 18, {{DOI|10.1186/1465-9921-15-18}}, PMID 24517344, {{PMC|3925354}}.</ref> |
||
<ref name="PMID24627308">L. S. Conwell, A. B. Chang: ''Bisphosphonates for osteoporosis in people with cystic fibrosis.'' In: ''The Cochrane database of systematic reviews.'' Band 3, 2014, {{ISSN|1469-493X}}, S. CD002010, {{DOI|10.1002/14651858.CD002010.pub4}}, PMID 24627308 (Review).</ref> |
|||
<ref name="PMID24801204">V. A. Peotta, P. Bhandary u. a.: ''Reduced blood pressure of CFTR-F508del carriers correlates with diminished arterial reactivity rather than circulating blood volume in mice.'' In: ''PloS one.'' Band 9, Nummer 5, 2014, {{ISSN|1932-6203}}, S. e96756, {{DOI|10.1371/journal.pone.0096756}}, PMID 24801204, {{PMC|4011854}}.</ref> |
<ref name="PMID24801204">V. A. Peotta, P. Bhandary u. a.: ''Reduced blood pressure of CFTR-F508del carriers correlates with diminished arterial reactivity rather than circulating blood volume in mice.'' In: ''PloS one.'' Band 9, Nummer 5, 2014, {{ISSN|1932-6203}}, S. e96756, {{DOI|10.1371/journal.pone.0096756}}, PMID 24801204, {{PMC|4011854}}.</ref> |
||
<ref name="PMID25217870">T. A. VanWort, J. A. Lee u. a.: ''Female cystic fibrosis mutation carriers and assisted reproductive technology: does carrier status affect reproductive outcomes?'' In: ''Fertility and sterility.'' Band 102, Nummer 5, November 2014, {{ISSN|1556-5653}}, S. 1324–1330, {{DOI|10.1016/j.fertnstert.2014.07.1234}}, PMID 25217870.</ref> |
<ref name="PMID25217870">T. A. VanWort, J. A. Lee u. a.: ''Female cystic fibrosis mutation carriers and assisted reproductive technology: does carrier status affect reproductive outcomes?'' In: ''Fertility and sterility.'' Band 102, Nummer 5, November 2014, {{ISSN|1556-5653}}, S. 1324–1330, {{DOI|10.1016/j.fertnstert.2014.07.1234}}, PMID 25217870.</ref> |
||
Version vom 21. März 2015, 16:47 Uhr
| Klassifikation nach ICD-10 | |
|---|---|
| E84 | Zystische Fibrose |
| E84.0 | Zystische Fibrose mit Lungenmanifestationen |
| E84.1 | Zystische Fibrose mit Darmmanifestationen |
| E84.8 | Zystische Fibrose mit sonstigen Manifestationen |
| E84.9 | Zystische Fibrose, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |
Mukoviszidose (lat. mucus ‚Schleim‘ und viscidus ‚zäh‘, bzw. ‚klebrig‘), auch zystische Fibrose (ZF, engl. cystic fibrosis, CF) genannt, ist eine autosomal-rezessiv vererbte Stoffwechselerkrankung. Die Ursache dieser Erkrankung ist eine durch Mutation bedingte Fehlfunktion von Chloridkanälen bestimmter Körperzellen, wodurch die Zusammensetzung aller Sekrete exokriner Drüsen verändert wird. Die betroffenen Zellen sind nicht in der Lage mittels Osmose Wasser in das umliegende Gewebe zu ziehen, wodurch der Wassergehalt des Bronchialsekrets sowie der Sekrete der Bauchspeicheldrüse, der Leber (Galle), inneren Geschlechtsorgane und akzessorischen Geschlechtsdrüsen sowie des Dünndarms zu niedrig ist. Die Sekrete werden dadurch zähflüssig und in den betroffenen Organen kann es zu Funktionsstörungen unterschiedlicher Art kommen. Mukoviszidose ist daher eine Multisystemerkrankung. Bisher sind über 1900 unterschiedliche Mutationen bekannt, die bei den Betroffenen zu einer Mukoviszidose führen können.[1]
Erste Symptome zeigen sich in bereits in der frühen Kindheit.[2] Die Erkrankung ist derzeit nicht heilbar. Durch den medizinischen Fortschritt konnten über die letzten Jahrzehnte neue Behandlungsmöglichkeiten etabliert werden, durch die die mittlere Lebenserwartung von ursprünglich etwa 20 Jahren mehr als verdoppelt wurde.[3] Mukoviszidose ist die häufigste autosomal-rezessive Erbkrankheit und die häufigste letale genetische Erkrankung in der hellhäutigen Bevölkerung. Statistisch gesehen kommt in dieser Bevölkerungsgruppe auf 2000 Lebendgeburten ein erkranktes Kind.[2] Dabei gibt es erhebliche regionale Schwankungen in der Häufigkeit der Erkrankung.
Epidemiologie
In Europa liegt die Wahrscheinlichkeit der Geburt eines Kindes mit Mukoviszidose bei etwa 1:2000. In Deutschland leben derzeit ungefähr 8000 an Mukoviszidose erkrankte Menschen. Pro Jahr werden etwa 300 Kinder mit Mukoviszidose in Deutschland geboren.[4] Mukoviszidose steht an erster Stelle der Erbkrankheiten, die bei Kindern bis zum 15. Lebensjahr zum Tod führen.[5]
Die Allelfrequenz liegt in der deutschen Bevölkerung bei etwa 0,04 bis 0,05[4]. Diese Zahl ist ein Maß für die relative Häufigkeit eines Allels in einer Population. Der Wert von 0,04 bedeutet, dass 4 % der Bevölkerung ein defektes CFTR-Gen trägt. Diese rund drei Millionen Menschen sind gesunde Genträger, die das mutierte Allel weitervererben können. Man spricht in diesem Fall von heterozygoten Merkmalsträgern. Die Wahrscheinlichkeit, dass zwei heterozygote Merkmalsträger ein Kind zeugen hat – bezogen auf die Gesamtpopulation dann eine Wahrscheinlichkeit von 0,04² = 0,16 % = 1:625. Da dem autosomal-rezessiven Erbgang folgend nur jedes vierte Kind dabei an Mukoviszidose erkrankt, reduziert sich die Wahrscheinlichkeit auf 1:2500. In epidemiologischen Studien wurde für Deutschland ein Wert von 1:3300 ermittelt.[6][7][8] Weltweit betrachtet sind die Mukoviszidose-Inzidenzen sehr unterschiedlich. Die weltweit höchste Wahrscheinlichkeit für die Geburt eines Kindes mit Mukoviszidose hat Irland mit 1:1800.[7][8] Den in Europa niedrigsten Wert hat Finnland mit 1:25.000.[8] Bei Menschen afrikanischer Abstammung beträgt das Risiko etwa 1:17.000. Für Menschen asiatischer Abstammung ist es mit etwa 1:90.000 am unwahrscheinlichsten mit der Erkrankung geboren zu werden.
Derzeit sind 1994 unterschiedliche Mutationen im CFTR-Gen statistisch erfasst (Stand März 2015).[9] Diese Mutationen sind über die Gesamtbevölkerung sehr ungleichmäßig verteilt. So haben weniger als 20 Mutationen einen Anteil von über 0,1 Prozent und nur fünf Mutationen einen Anteil von über 1 Prozent an der Gesamtzahl der Mukoviszidoseerkrankungen. Die mit Abstand am häufigsten auftretende Mutation hat die Bezeichnung ΔF508. Sie findet sich in etwa 2/3 aller CFTR-Allele von Mukoviszidosepatienten.[10] Innerhalb von Europa nimmt dabei die Prävalenz von Nord-West nach Süd-Ost ab.[11][12]
Bei den 1994 erfassten Mutationen stellen nicht-synonyme Mutationen, das sind Punktmutationen, bei denen für eine andere Aminosäure codiert wird, mit 39,7 % den Hauptanteil. Es folgen Frameshift-Mutationen, das sind Verschiebungen des Leserasters von CFTR auf der DNA, mit 15,7 % und Spleißmutationen mit 11,4 %. Der Anteil an Nonsense-Mutationen liegt bei 8,3 %, der von in frame-Deletionen und in frame-Insertionen 2,0 %. Große Insertionen und Deletionen haben eine Häufigkeit von 2,6 %. Promotermutationen im CFTR-Gen, das sind Punktmutationen im Promoterbereich von CFTR, die zu einer verminderten Genexpression von CFTR führen, sind mit einem Anteil von 0,75 % vergleichsweise selten. Lediglich 13,5 % der erfassten Mutationen in codierenden Bereichen von CFTR führen nicht zu einer Erkrankung. Bei insgesamt 6,1 % ist der Mutationstyp noch unbekannt.[9]
Durch den Gründereffekt können manche, eher seltene Mutationen in einigen Populationen deutlich überrepräsentiert sein.[13][14] Der Gründereffekt kann dabei durch religiöse, ethnische oder geografische Isolation entstehen.[10]
Genetik und Molekularbiologie
Die Ursache für Mukoviszidose sind verschiedene Mutationen im CFTR-Gen, das beim Menschen auf dem langen Arm von Chromosoms 7 (Genlocus q31.2) sitzt. Das CFTR-Gen codiert für das Protein Cystic Fibrosis Transmembrane Conductance Regulator (CFTR). Dieses Genprodukt fungiert in der Zellmembran als Chloridkanal. Durch die Veränderung im Gen wird ebenso das Protein verändert und die Kanalfunktion bleibt aus oder ist eingeschränkt. Es handelt sich somit um eine Mutation, die zu einem Funktionsverlust des betroffenen Proteins führt (Loss-of-Function-Mutation). Die häufigste Mutation dieses Gens wird ΔF508 genannt. ΔF508 bezeichnet das Fehlen der Aminosäure Phenylalanin (‚F‘ im Einbuchstabencode) an der Position 508 im CTFR-Protein und betrifft etwa sieben von zehn Menschen mit Mukoviszidose.[15]
Bisher sind insgesamt über 1900 verschiedene Mutationen des CFTR-Gens bekannt, welche in unterschiedlichen Populationen mehr oder weniger gehäuft auftreten. Eine Besonderheit dabei ist, dass bei der Mukoviszidose auch zwei verschiedene Mutationen des CFTR-Gens, also zwei verschiedene Allele desselben Gens, dennoch zur Erkrankung führen können. Diese besondere Konstellation eines autosomal-rezessiven Erbgangs wird dementsprechend Compound-Heterozygot genannt.[16]
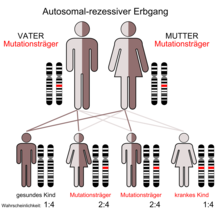
Da Mukoviszidose autosomal-rezessiv vererbt wird, tritt die Erkrankung nur dann auf, wenn der Merkmalsträger von beiden Elternteilen je ein mutiertes Gen erbt. Sind beide Elternteile Träger je eines mutierten und eines unveränderten Genes, dann ist die Wahrscheinlichkeit, dass ein Kind zwei intakte Genkopien erhält, 25 %. Die Wahrscheinlichkeit, dass das Kind mit einer intakten und einer mutierten Kopie zwar gesund ist, aber die Mutation weitervererben kann, ist 50 % und die Wahrscheinlichkeit, dass das Kind erkrankt, also von beiden Eltern die krankmachende Variante erbt, beträgt ebenfalls 25 %. Sind beide Eltern erkrankt, würden auch alle Kinder die Erkrankung erben. Allerdings ist dies sehr unwahrscheinlich, da die Betroffenen meist unfruchtbar[17] sind.
Pathologie
Das CFTR-Protein ist ein an der Zellmembran lokalisierter, durch cyclisches Adenosinmonophosphat (cAMP) regulierter Chloridkanal, der vor allem von Epithelzellen exprimiert wird.[18] Je nach Mutation kann die Expression des Chloridkanals unterdrückt werden oder es befinden sich nur defekte oder in ihrer Funktion oder Funktionsdauer eingeschränkte CFTR-Protein in der Zellmembran. Dadurch ist wiederum die Chloridsekretion der betroffenen Zelle gestört, was eine geringere osmotische Treibkraft des Wassers und damit eine geringere Diffusion von Wasser aus der Zelle zur Folge hat.[19] Auf dieses Ungleichgewicht beim transzellulären Ionentransport reagiert die Zelle durch eine vermehrte Expression von epithelialen Natriumkanälen (ENaC), was eine erhöhte Aufnahme von Natriumionen durch die Zelle nach sich zieht. Zum osmotischen Ausgleich der hohen Konzentration von Natriumionen in der Zelle strömt Wasser in die Zelle ein.[20] Der Verlust von Wasser auf der apikalen Seite der Zelle führt zu einer Erhöhung der Viskosität der Zellsekrete.
Das aus 1480 Aminosäuren bestehende CFTR-Protein wird von den Endothelzellen in neun bis zehn Minuten im endoplasmatischen Retikulum synthetisiert.[21] Die Faltung des hochkomplexen Proteins dauert etwa 30 bis 120 Minuten. Der Faltungsprozess wird durch ein ganzes Arsenal von Chaperonen,[22] wie beispielsweise Hsp70, Hsp40, Hsp90 und Calnexin untersützt.[23] Liegt das Protein in diesem Zeitraum nicht korrekt gefaltet vor, so wird über Chaperone wie Hsp70 die Ubiquitin-Protein-Ligase UBR1 rekrutiert, die das falsch gefaltete CFTR ubiquitinyliert und dadurch dem Abbau im 26s-Proteasom zuführt.[23] Diese Proteinqualitätskontrolle ist ein zelluärer Schutzmechanismus, der für die Aufrechterhaltung eines funktionierenden Proteoms und zum Überleben der Zelle von grundlegender Wichtigkeit ist. Das Kriterium, das über Abbau im Proteasom und – im Fall von CFTR – Transport zur Zellmembran entscheidet, ist allerdings nicht eine verminderte Funktion des Proteins, sondern seine signifikant reduzierte Faltungskinetik. Möglicherweise würde das Protein, wenn es ausreichend Zeit hätte, noch korrekt falten.[24] Tatsächlich werden auch im gesunden homozygoten Menschen etwa 75 % der CFTR-Proteine von der Proteinqualitätskontrolle als „falsch“ gefaltet erkannt und abgebaut.[21]
Mutationsklassen

Die fast 2000 Mutationen die Mukoviszidose verursachen lassen sich in sechs Klassen einteilen, die sich in ihrem Pathomechanismus unterscheiden.[25]
- Klasse I
Bei Klasse-I-Mutationen ist der Gendefekt so schwerwiegend, dass kein CFTR-Protein produziert wird. Die Ursache hierfür können verfrühte Stopcodons sein, die bei der Transkription zu einer gekürzten, instabilen mRNA führen. Beispiele hierfür sind die Mutationen Gly542X, Trp1282X, and Arg553X. Eine andere Ursache können kanonische Spleißmutationen, wie zum Beispiel 621+1G→T, und chromosomale Deletionen, wie CFTRdel2,3, sein, die ebenfalls zu einem Ausfall der CFTR-Produktion im endoplasmatischen Retikulum führen.[1]
- Klasse II
Eine Proteinsyntese findet bei Klasse-II-Mutationen zwar statt, jedoch stimmt durch eine Mutation im CFTR-Gen die Primärstruktur des CFTR-Proteins nicht. Dies wirkt sich auf die Tertiärstruktur des Proteins aus, das Protein ist falsch gefaltet. Diese Proteinfehlfaltung wird von der Proteinqualitätskontrolle der Zelle erkannt, das Protein wird ubiquitinyliert, ins Proteasom transportiert und dort zerlegt. Die weltweit häufigste CFTR-Mutation ΔF508 gehört zu dieser Klasse, ebenso wie die Mutationen Asn1303Lys, Ile507del, Arg560Thr und Gly85Glu.[1]
- Klasse III
Im Fall von Klasse-III-Mutationen wird das CFTR-Protein produziert und an der Zellmembran auch exprimiert. Der Chloridkanal ist allerdings nicht funktionsfähig, weil er sich nicht öffnen lässt. Beispiele für diese Klasse sind die Mutationen Gly551Asp, Gly178Arg, Gly551Ser und Ser549Asn.[1]
- Klasse IV
Auch bei Klasse-IV-Mutationen wird CFTR an der Zellmembran exprimiert. Der Chloridkanal lässt sich öffnen, allerdings ist seine Durchlässigkeit für Chloridionen stark eingeschränkt. Dies ist beispielsweise bei den Mutationen Arg117His, Arg347Pro, Arg117Cys und Arg334Trp der Fall.[1]
- Klasse V
Bei Klasse-V-Mutationen wird zu wenig CFTR-Protein produziert. Ursache hierfür sind meist Mutationen in Introns, die zu einem alternativen Spleißen führen und dadurch unmittelbar negativ die Menge an produziertem CFTR-Protein beeinflussen. Beispiele hierfür sind die Mutationen 3849 + 10kbC→T, 2789 + 5G→A und 5T.[1]
- Klasse VI
Diese Mutationsklasse ist vergleichsweise selten. Bei ihr wird funktionsfähiges CFTR-Protein an der Zellmembran exprimiert, allerdings ist die Stabilität des Proteins an der Zellmembran reduziert, so dass es vergleichsweise schnell wieder in das Zytoplasma zurückkehrt und abgebaut wird. Ein Beispiel hierfür ist die Mutation 4326delTC.[1] Im Vergleich zum Wildtyp hat dieses Genprodukt eine um den Faktor 5 bis 6 höhere Degradationsrate.[26]
Klinisches Bild
Je nach Typ der Mutation sind die Symptome der Erkrankung mehr oder weniger stark ausgeprägt. Hat der Patient verschiedene Mutationen der CFTR-Gene beider Chromosomen, kommt es nur zur Ausprägung der Symptome des geringeren Defekts. Menschen mit wenig beeinträchtigenden Mutationen haben häufig nur Bauchspeicheldrüsenprobleme, bei schwerwiegenden Mutationen können alle genannten Symptome auftreten.
Atemtrakt
Der zähflüssige Schleim in den Bronchien führt zu chronischem Husten, Bronchiektasien, häufig wiederkehrenden Lungeninfekten und schweren Lungenentzündungen. Das zähe Sekret kann vom Flimmerepithel der Trachea und der Bronchien nur schwer abtransportiert werden. Daher stellt es ein gutes Nährmedium für Krankheitserreger wie Pseudomonas aeruginosa, Staphylococcus aureus, Burkholderia cepacia, Stenotrophomonas maltophilia und die „schwarze Hefe“ (Exophiala dermatitidis und Exophiala phaeomuriformis) dar. Häufig leiden Betroffene auch an Aspergillose. Eine Folge der häufigen und langwierigen Lungeninfekte kann eine zunehmende Lungeninsuffizienz sein, die sich durch chronischen Sauerstoffmangel und Atemnot bemerkbar macht. Durch den chronischen Sauerstoffmangels hat die Mehrzahl der betroffenen Menschen Uhrglasnägel und Trommelschlägelfinger. Die chronischen endobronchialen Infektionen führen im Endstadium zu Zysten, Abszesse und Lungenfibrose, also zu einer extensiven Zerstörung der Atemwege, die auch meist die Ursache für die frühe Sterblichkeit von Mukoviszidosepatienten ist.[27]
Oxidativer Stress reduziert die Expression von CFTR in der Lunge.[28] So konnten bei gesunden Rauchern, im Vergleich zu gesunden Nichtrauchern, Hinweise auf niedrigere Werte von CFTR in der Lunge gefunden werden.[29] Oxidativer Stress wiederum kann durch Glutathion, ein körpereigenes Antioxidans, reduziert werden. Es hat eine wichtige Funktion zum Schutz der Lunge bei oxidativem Stress. Das Enzym Glutamatcysteinligase beeinflusst die Glutathion-Synthese in den Zellen. Ein Polymorphismus am GCLC-Gen, das für die Glutamatcysteinligase codiert, kann eine erhöhte Produktion von Glutathion in der Lunge bewirken. In einer Studie aus dem Jahr 2006 wurden 440 Mukoviszidose-Patienten auf den möglichen Einfluss des GCLC-Polymorphismus auf das Krankheitsbild untersucht. Dabei wurde ein signifikater Zusammenhang zwischen dem funktionalen Polymorphismus von CFLC und der schwere der Mukoviszidose bei Patienten mit einem CFTR-Genotyp der milden Form festgestellt.[30]
Verdauungstrakt
Im Darm kommt es bei Säuglingen in 10 % der Fälle zum Mekonium-Ileus, einer schweren Darmobstruktion durch die zähen ersten Faeces (Stuhl). Bei Älteren finden sich in 20 % Obstruktionssyndrome durch zähflüssige Darmsekrete. Hierbei kann es im Einzelfall zur Komplikation kommen, dem Mekonium-Ileus-Äquivalent. Auch die Funktion der Bauchspeicheldrüse ist gestört. 2 % der Kinder und 50 % der Erwachsenen haben einen Diabetes mellitus (Zuckerkrankheit). Durch das fehlende Sekret entstehen chronische Durchfälle, Maldigestion, Mangelernährung und Verdauungsstörungen sowie Untergewicht. Ist auch die endokrine Funktion des Pankreas betroffen, kann es zum so genannten pankreatogenen Diabetes mellitus kommen. Durch Störung der Leber- und Gallenwegsfunktion neigen betroffene Erwachsene zu Leberzirrhose und Gallensteinen.
Fortpflanzungsorgane
Durch Störung der Sekrete der Geschlechtsorgane besteht bei erkrankten Männern meist Unfruchtbarkeit durch Funktionsstörung der Samenleiter. Spermien werden jedoch normal gebildet. Bei Frauen ist durch zähflüssige Sekrete im Zervixkanal die Fruchtbarkeit vermindert.
Skelettsystem

Die bei Mukoviszidosepatienten in den vergangenen Jahrzehnten erreichten erheblichen Verbesserungen in der Überlebensrate führen zum vermehrten Aufkommen von Spätkomplikationen, zu denen Osteoporose zählt.[32] Erwachsene Mukoviszidosepatienten haben eine signifikant reduzierte Knochendichte.[33][34] Dies erhöht das Risiko von Knochenbrüchen und die Ausbildung einer Kyphose („Buckel“).[35] Rippenfrakturen sind bei erwachsenen Mukoviszidosepatienten um den Faktor 10 bis 100 häufiger, als in einer gesunden Vergleichsgruppe.[31][35]
Die genauen Ursachen für die reduzierte Knochendichte sind noch nicht ausreichend erforscht. Es handelt sich offensichtlich um ein sehr komplexes Zusammenspiel mehrerer Pathomechanismen. Eine wesentliche Rolle spielt dabei offensichtlich der schlechte Ernährungszustand, die Malabsorption von Vitamin D und K,[32] sowie ein verminderter Calcium- und Phasphatgehalt im Serum.[36] Studien konnten zudem zeigen, dass während infektiöser Phasen die Knochenresorption (Knochenabbau) erhöht ist und Störungen in der Knochenbildung zu beobachten sind.[32] So ist in solchen Phasen die Zahl der für den Knochenabbau verantwortlichen Osteoklasten signifikant erhöht.[37][38] Neuere Forschungsergebnisse deuten außerdem darauf hin, dass die gestörte Funktion des CFTR-Proteins zu einer Funktionsstörung der für die Knochenbildung verantwortlichen Osteoblasten führt.[32] Osteoblasten exprimieren CFTR.[39] Das Fehlen des Chloridkanals führt bei Osteoblasten offensichtlich zu Störungen des Gleichgewichts zwischen Osteoprotegerin und Prostaglandin E2.[40] Auch die langzeitige Anwendung von Medikamenten, insbesondere von Glucocorticoiden zur Verbesserung des respiratorischen Zustands, kann den Knochenabbau fördern. Dies ist vor allem bei Mukoviszidosepatienten mit einer Lungentransplantation der Fall. Sie erhalten zu Unterdrückung der Organabstoßung in der akuten Phase Glucocorticoide in hohen, danach in niedrigen Dosen.[41][32]
Sonderfall CAVD
Die kongenitale bilaterale Aplasie des Vas deferens (CAVD für engl. congenital aplasia of vas deferens) ist eine angeborene Fehlbildung, die zu einem Fehlen der Samenleiter führt. Die meisten betroffenen Männer tragen Mutationen im CFTR-Gen.[42] Solche Fälle können als milde Sonderform einer Mukoviszidose angesehen werden. Verantwortlich für die milde Ausprägung ist ein besonderes Mutationsspektrum, insbesondere des 5T-Allels. 70 bis 80 % der Männer mit CAVD haben zwei Mutationen im CFTR-Gen, wobei eine davon ein mildes Allel ist, das beispielsweise nur einen Aminosäureaustausch in einer Transmembranregion verursacht.[43]
Diagnostik
Der Schweißtest ist bei Verdacht auf Mukoviszidose das Mittel der Wahl.[44] Dabei wird mit Hilfe des Arzneistoffs Pilocarpin die Schweißausscheidung stimuliert. Dazu wird ein schwacher Gleichstrom auf der Haut angelegt, der die Diffusion von Pilocarpin zu den Schweißdrüsen der Haut vermittelt. Dieses Verfahren wird Iontophorese genannt. Mit einer Kapillare wird eine Schweißprobe aus dem stimulierten Areal aufgesaugt und die Probe quantitativ auf den Gehalt von Natrium oder Chlorid analysiert. Liegt der Gehalt an Natriumchlorid in der Probe oberhalb von 80 mmol/l, so besteht ein erheblicher Verdacht auf Mukoviszidose. Der Normalwert liegt im Bereich von 5 bis 55 mmol/l. Der Schweißtest wird üblicherweise an zwei verschiedenen Tagen wiederholt. Fällt er positiv aus oder sind die Ergbnisse nicht eindeutig erfolgt im Normalfall eine DNA-Analyse (Gentest).[45]
Eine aufwendigere Alternative zum Schweißtest ist die Bestimmung von immunreaktivem Trypsin im Blutserum.[45] Er wird üblicherweise am fünften Lebenstag durchgeführt. Dazu wird Vollblut aus der Ferse entnommen und das Trypsin mittels Radioimmunassay bestimmt. Der Normalwert liegt unterhalb von 80 ng/ml. Die Ergebnisse sind aussagekräftiger als beim Schweißtest.[46]
Schon vorgeburtlich kann man mit molekulargenetischer Diagnostik aus fetalen Zellen verschiedene Prädispositionen nachweisen.
Die ersten Programme für ein Neugeborenenscreening (NGS) auf Mukoviszidose begannen 1981 in Neuseeland und Australien.[47] In der Schweiz wird seit 2011 im Rahmen des Neugeborenenscreenings routinemäßig auch auf Mukoviszidose geprüft.[48] Derzeit (Stand 2013) wird dies auch in den Vereinigten Staaten, England, Irland, Schottland, Frankreich, Österreich, Polen, in den Niederlanden sowie in Regionen Italiens und Spaniens so gehandhabt.
In Mecklenburg-Vorpommern wird seit 2012 bei allen Neugeborenen im Rahmen des Neugeborenenscreening auf Stoffwechselkrankheiten auch ein Test auf Mukoviszidose angeboten.[49] Im Jahr 2013 wurden nur etwa 15 % der Neugeborenen in Deutschland auf Mukoviszidose hin untersucht. Deshalb wird nur bei etwa 58 % der Kinder mit Mukoviszidose die Erkrankung im ersten Lebensjahr erkannt. Das Durchschnittsalter bei der Diagnosestellung beträgt 4,8 Jahre. 7,6 % der Patienten sind bei der ersten Diagnosestellung 18 Jahre oder älter (Stand 2012).[50] Eine frühzeitige Diagnosestellung ermöglicht eine zeitnahe Behandlung, mit der der Verlauf und die Lebensqualität der Patienten verbessert werden kann. Gegenüber der klinischen Diagnosestellung verspricht man sich auch einen langfristigen Kostenvorteil.[51] Es gibt daher seit Jahren, speziell aus dem Bereich der Ärzteschaft, die Forderung nach einem bundesweiten Neugeborenenscreening.[52][51] In den Vereinigten Staaten, Großbritannien, Frankreich und Australien wird ein genbasiertes Verfahren verwendet. Das deutsche Gendiagnostikgesetz gestattet dies nur unter strengen Auflagen. Auch aus diesem Grund wird in Deutschland der Trypsin-Test favorisiert.[53]
Therapie
Dank Krankengymnastik, Inhalationen und Medikamenten, insbesondere durch ständig verbesserte Verdauungsenzyme und Antibiotika, die in den vergangenen Jahren auf den Markt gekommen sind, hat sich die Prognose der erkrankten Menschen in den letzten Jahren erheblich verbessert. Die Behandlung wirkt jedoch nicht ursächlich heilend, sondern nur symptomatisch. Die Mukoviszidose ist ein Systemdefekt, der verschiedene Organe betrifft; da eine ursächliche Behandlung nicht möglich ist, muss jede Störung der einzelnen Organsysteme gesondert therapiert werden.
Symptomatische Behandlung
Bei Kindern mit Gedeihverzögerung kann eine Therapie mit Wachstumshormonen indiziert sein. Ein besseres Wachstum mit verbessertem Körpergewicht führt auch zu weniger Krankenhausaufnahmen, weniger Antibiotika-Behandlungen und einer verbesserten Lungenfunktion.[54] Genauso wichtig ist die Gabe von Medikamenten zum Lösen des zähen Schleims in den Bronchien durch Inhalation und Durchführung der anschließenden autogenen Drainage oder der modifizierten autogenen Drainage, beides speziell entwickelte Atemtherapien zum schonenden Abtransport des Sekretes aus der Lunge.
Neben Medikamenten zur Inhalation, die den zähen Schleim lösen, kommen auch Inhalationsmedikamente zur Erweiterung der Bronchien zum Einsatz, ebenso Antibiotika oder Corticosteroide, die ebenfalls inhalativ appliziert werden.
Ferner ist die gezielte antibiotische Behandlung der häufigsten Erreger zu nennen, sowie die Verabreichung von fettlöslichen Vitaminen (A, D, E und K).
Die Lunge von Menschen mit Mukoviszidose wird häufig von immer wiederkehrenden Infekten heimgesucht, die das Lungengewebe dauerhaft schädigen. Insbesondere Problemkeime wie beispielsweise Pseudomonas aeruginosa, Burkholderia cepacia oder resistente Keime verursachen häufig schwere Lungenentzündungen bei Mukoviszidose. Eine große Bedeutung kommt daher der Bekämpfung dieser Keime zu. Die Lunge der meisten betroffenen Erwachsenen weist eine chronische Besiedelung mit dem Bakterium Pseudomonas aeruginosa auf, was häufig zu einer Verschlechterung der Lungensituation führt.
Einige der genannten Bakterien, z. B. Pseudomonas aeruginosa, bilden zusammen mit dem zähen Schleim einen Biofilm in der Lunge der Erkrankten. Durch den zähen Schleim finden die Bakterien einen idealen Nährboden vor, in dem sie sich regelrecht verschanzen und für Antibiotika daher nur schwer zugänglich sind. Hier werden hochdosierte Antibiotika-Gaben meist intravenös und in dreimonatigen Abständen über eine Dauer von 14 Tagen verabreicht. Außerdem gibt es inzwischen Antibiotika auf dem Markt, die die Kommunikation der Bakterien untereinander stören. Die Bakterien sind nur dann in der Lage, einen Biofilm aufzubauen, wenn sie untereinander kommunizieren können. An der Entwicklung weiterer Substanzen wird geforscht.
Bei zunehmender Lungeninsuffizienz wird der Atemluft dauerhaft Sauerstoff zugemischt (Sauerstoff-Langzeittherapie). Unter dem Markennamen Pulmozyme wird rekombinante humane DNase (rhDNAse, Dornase alpha) als inhalatives Medikament zur Auflösung der im Schleim vorhandenen DNA-Filamente eingesetzt. Diese DNA-Filamente sind Überbleibsel von Neutrophilen Granulozyten. Neutrophile Granulozyten sind Zellen des Immunsystems, die in die Lunge einwandern, um dort angesiedelte Bakterien zu attackieren. Nach getaner Arbeit werden die Neutrophilen Granulozyten von wieder anderen Zellen des Immunsystems entsorgt, wobei besagte DNA-Filamente der Neutrophilen Granulozyten übrig bleiben. Diese DNA-Filamente tragen zusätzlich zur Zähigkeit des ohnehin schon zähen Schleims in der Lunge der Betroffenen bei. Durch die Gabe von Dornase alpha wird die Spinnbarkeit des Schleims herabgesetzt und die mukoziliäre Clearance verbessert.
Bei Sonderproblemen wie Diabetes mellitus oder der gestörten Produktion von Gallensäuren müssen auch diese Probleme medikamentös behandelt werden. Bei auftretendem Darmverschluss, dem sogenannten Mekonium-Ileus-Äquivalent, muss sofort ärztliche Hilfe in Anspruch genommen werden.
Für die Behandlung von Osteoporose bei Mukoviszidose gibt es bisher noch keine Richtlinien. Der Schwerpunkt sollte bei vorbeugenden Maßnahmen liegen, die unter anderem eine gesunde Ernährung mit Calcium- und Vitamin-D-Substitution, sowie körperliche Aktivität beinhalten. Eine vorhandene Osteoporose kann prinzipiell mittels Bisphosphonaten, Hormonersatztherapie oder Calcitonin behandelt werden. Die wenigen verfügbaren Studien über Bisphosphonatbehandlung bei Patienten mit Mukoviszidose belegen zwar eine Zunahme der Knochendichte, aber die Zahl der Knochenbrüche wird nicht signifikant gesenkt.[55]Referenzfehler: Ungültige Verwendung von <ref>: Der Parameter „name“ darf kein reiner Zahlenwert sein. Benutze einen beschreibenden Namen. Über die Behandlung der Osteoporose mit Raloxifen, Strontiumranelat und Teriparatid bei Patienten mit Mukoviszidose liegen noch keine Studienergebnisse vor.Referenzfehler: Ungültige Verwendung von <ref>: Der Parameter „name“ darf kein reiner Zahlenwert sein. Benutze einen beschreibenden Namen.
Regelmäßige Kontrolluntersuchungen in einer speziellen Ambulanz in einem Krankenhaus, einer Uniklinik oder bei einem niedergelassenen Spezialisten sind ein wesentlicher Bestandteil der der Therapie.
Unterstützende Maßnahmen
Dem durch die exokrine Pankreasinsuffizienz bedingten Gewichtsverlust wird durch die Gabe hochkalorischer, fettreicher Kost und die Verabreichung von Verdauungsenzymen entgegengewirkt. Dem Körpergewicht von Mukoviszidose-Patienten kommt eine große Bedeutung zu. Je länger ein normales oder ideales Gewicht gehalten und Untergewicht verhindert werden kann, desto günstiger wirkt sich dies auf die Lungenfunktion der Betroffenen aus. Erkrankte mit starkem Untergewicht weisen bei den Kontrolluntersuchungen in der Regel schlechtere Lungenfunktionswerte auf als solche mit normalem Körpergewicht oder mit nur minimalem Untergewicht. Von dieser Regel gibt es selbstverständlich Ausnahmen. Zu beachten ist, dass die erschwerte Atmung (z. B. durch Obstruktion der Lunge) den Kalorienverbrauch abermals erhöht. Dieser Tatsache wird üblicherweise durch Erhöhung der Kalorienzufuhr Rechnung getragen.
Zur unterstützenden Therapie gehört regelmäßige sportliche Betätigung wie Laufen, Joggen, Radfahren, Tanzen o. ä.. Die für den Einzelnen jeweils günstigste Sportart, wird dem jeweiligen Gesundheitszustand angepasst und vom behandelnden Arzt empfohlen.
Medikamentöse Behandlung der primären Krankheitsursache

Ivacaftor (Kalydeco) (Pharmazeutischer Unternehmer: Vertex Pharmaceuticals) ist das erste Medikament, das für die Behandlung der primären Ursache einer Mukoviszidose zugelassen wurde.[56] Es wurde im Januar 2012 von der Food and Drug Administration (FDA)[57] und im Juli desselben Jahres von der Europäischen Arzneimittel-Agentur (EMA)[58][59] für die Behandlung von Patienten im Alter über sechs Jahren mit einer G551D-Mutation[60] freigegeben.[61] Etwa 4 bis 5 % aller Mukoviszidose-Patienten weisen diese Mutation auf.[62] Dies entspricht etwa 3000 Patienten weltweit.[8] In Europa haben etwa 1500 Mukoviszidose-Patienten eine G551D-Mutation.[62] In Deutschland weisen nur für etwa 2 % der Mukoviszidose-Patienten die notwendige Indikation für eine Behandlung mit Ivacaftor auf.[63] Die Behandlungskosten betragen in den Vereinigten Staaten etwa 300.000 $ pro Patient und Jahr.[64] Ivacaftor wurde mit finanzieller Unterstützung der US-amerikanischen Patientenorganisation Cystic Fibrosis Foundation entwickelt. Vertex Pharmaceuticals erhielt insgesamt 75 Millionen $.[64] Die Foundation bekommt dafür einen Teil der Gewinne von Vertex Pharmaceuticals.[62] In Deutschland werden die Behandlungskosten in Höhe von über 330.000 € pro Patient und Jahr[65] von den gesetzlichen Krankenkassen voll übernommen.[63] Im Vergleich dazu liegen die Arzneimittelkosten der Standardtherapie bei etwa 21.000 € pro Patient und Jahr. Eine Lungetransplantation wird mit etwa 150.000 € angesetzt.[65] Die G551D-Mutation bewirkt einen Klasse-III-Defekt im CFTR-Kanal. Ivacaftor gehört zur Gruppe der CFTR-Potentiatoren.[66] Es ist ein CFTR-Kanalöffner, der den defekten CTFR-Kanal öffnet und so die verminderte Aktivität von CFTR erhöht.
Andere medikamentöse Ansätze zielen auf eine medikamentöse Verbesserung des durch den Gendefekt unwirksamen CFTR-Proteins (beispielsweise Gentamicin, Denufosol, Flavonoide). Hier werden teilweise auch Mittel, die der Alternativmedizin entstammen, untersucht und kontrovers diskutiert (beispielsweise Curcumin). Andere potenzielle Wirkstoffe sollen gezielt die Veränderung in der Ionenleitfähigkeit beeinflussen, indem alternative Chloridkanäle aktiviert werden (beispielsweise INS37217). Auch die direkte pharmakologische Beeinflussung des defekten CFTR-Kanals auf Protein-Ebene wird untersucht. Im Frühjahr 2008 wurde am Klinikum Essen von Erich Gulbins die Indikation für Amitriptylin auch auf die Krankheit Mukoviszidose erweitert.[67][68] Amitriptylin hemmt die saure Sphingomyelinase indirekt[69] und wirkt damit als FIASMA. Ein weiterer Ansatz beruht darauf, das defekte Gen trotz der Mutation vollständig auszulesen. Dieses soll mit Hilfe von z. B. Ataluren möglich sein.
Lungentransplantation
Organtransplantationen, besonders von Lunge, Leber und Bauchspeicheldrüse, werden heute regelmäßig in Transplantations-Zentren durchgeführt und stellen für viele Menschen eine echte Alternative in der Behandlung der Mukoviszidose dar. Der Nutzen einer Lungentransplantation bei dieser Indikation ist jedoch umstritten.[70]
Schwangerschaft/Fertilität
Bei stabiler Gesamtsituation ist für Mukoviszidose-Patientinnen das Austragen einer Schwangerschaft möglich. Männliche Mukoviszidose-Patienten sind durch die Verlegung der Samenkanäle zum größten Teil unfruchtbar (98 %).
CFTR-heterozygote Frauen haben Studien zu Folge im Vergleich zu Frauen mit zwei nicht-mutierten CFTR-Allelen keine reduzierte Fruchtbarkeit.[71]
Prognose
Während noch vor zwei Jahrzehnten viele Patienten mit Mukoviszidose schon im Jugendalter verstarben, besteht heute aufgrund der sich stetig verbessernden Therapiemöglichkeiten eine gute Chance, das 4. Lebensjahrzehnt zu erreichen. Die Lebenserwartung liegt heute bei etwa 40 Jahren. Für heute Neugeborene wird bereits ein Wert von 45 bis 50 Jahren angegeben. Minimal Erkrankte haben eine normale Lebenserwartung und sind in der Lage, Kinder zu zeugen oder auszutragen.
Heterozygote Merkmalsträger
Heterozygote CFTR-Mutationsträger können zwar nicht an einer Mukoviszidose erkranken, haben allerdings eine signifikant geringere Expression an CFTR-Protein. In einer Reihe von Studien wurde untersucht, ob dies möglicherweise anderweitige gesundheitliche Auswirkungen hat – neagtive wie auch positive.
Allgemeine Erkrankungsrisiken
Gesichert ist, dass heterozygote CFTR-Mutationsträger anfälliger für eine Pankreatitis (Bauchspeicheldrüsenentzündung) sind. Das Risiko an einer idiopathischen chronischen Pankreatitis zu erkranken ist etwa um den Faktor zwei[72] bis elfmal[73] höher als bei Menschen ohne defektes CFTR-Gen. Die genauen Ursachen hierfür sind noch unbekannt.[74]
Bereits 1976 konnte in einer Studie festgestellt werden, dass heterozygote CFTR-Mutationsträger auch für Allergien anfälliger sind.[75] Die Studienergebnisse über den Zusammenhang eines erhöhten Asthmarisikos bei heterozygoten CFTR-Mutationsträger sind dagegen bisher sehr widersprüchlich. Sie reichen von einem erhöten Risiko[76][77] bis zu einer leichten Schutzfunktion[78].[79]
Über die Gesamtpopulation betrachtet scheint die Fortpflanzungsfähigkeit von weiblichen und männlichen Merkmalsträgern der der Restbevölkerung zu entsprechen.[71][80][81] CFTR-Mutationen erhöhen auch nicht das Risiko, dass sich aus einer chronischen Bronchitis eine chronisch obstruktive Lungenerkrankung (COPD) entwickelt.[82]
Merkmalsträger haben, wie auch Mukoviszidosepatienten, einen reduzierten Blutdruck.[83][84] Dieser Befund wurde in der Vergangenheit über den erhöhten Elektrolytverlust erklärt.[85] Neuere Untersuchungen aus dem Jahr 2013[86] zeigen jedoch, dass die reduzierte CFTR-Expression auch Veränderungen an den Blutgefäßen bewirkt. Die Agonist-induzierte Freisetzung von Calciumionen durch die glatten Muskelzellen der Aorta wird vermindert. Auch dies reduziert den Blutdruck.[87] Der Effekt des reduzierten Blutdrucks bei Merkmalsträgern macht sich vor allem in fortgeschrittenem Alter und beim systolischen Blutdruck bemerkbar.[84] In einer britischen Studie mit über 1200 Probandinnen lag bei heterozygoten Merkmalsträgerinnen der systolische um 7 mmHg und der diastolische Blutdruck um 4 mmHg niederiger als in der Vergleichsgruppe. Erniedrigter Blutdruck bietet einen erhöhten Schutz vor Schlaganfällen und koronarer Herzkrankheit. Aus den Blutdruckwerten errechneten die Autoren der Studie für heterozygote Frauen ein um 30 % reduziertes Risiko für einen Schlaganfall und ein um 20 % reduziertes Risiko für einen Myokardinfarkt.[84]
Selektionsvorteil des heterozygoten Genotyps
Es gibt derzeit noch keine schlüssige Erklärung dafür, warum ein Allel, das eine so schwerwiegende Erkrankung hervorruft, so weit verbreitet ist und nicht im Laufe der Evolution ausselektiert wurde. Die Vermutung liegt daher nahe, dass bei einem heterozygoter Genotyp, das heißt, nur eines der beiden CFTR-Allele hat einen Funktionsverlust, ein Selektionsvorteil besteht. Tatsache ist, dass beim heterozygoten Genotyp die Anzahl der funktionsfähigen Chlorid-Kanäle reduziert ist. Die Vermutung ist, dass dies den Selektionsvorteil bietet.
- Anfangs wurde vielerorts die Theorie vertreten, dass das heterozygote Vorliegen des defekten CFTR-Gens die Dichte der (funktionierenden) Chlorid-Kanäle im Darm verringere, was die Symptome der Cholera positiv beeinflussen sollte (bei dieser Durchfallserkrankung werden Chloridkanäle dauerhaft geöffnet, was zu massivem Wasserverlust führt). Dies konnte in verschiedenen Studien nicht sicher belegt werden. Auch spricht die Epidemiologie der Mukoviszidose gegen diese Theorie, denn das mutierte Gen ist ausgerechnet in jenen Populationen häufig, in denen die Cholera eher selten auftritt, und umgekehrt.
- Auch eine Beziehung zum Typhus konnte nicht sicher hergestellt werden. Das Bakterium ist immerhin auf die CFTR-Kanäle angewiesen, um in die Darmzellen zu gelangen.
- Eine weitere mögliche Erklärung liegt in dem mit der Veranlagung für Mukoviszidose wahrscheinlich einhergehenden Schutz vor Tuberkulose. Diese These eines Selektionsvorteils konnte mittlerweile recht gut in klinischen Tests bestätigt werden, es bleibt nur die Frage nach der Verbreitungsdichte der Erbträger, die sich deutlich über die Tuberkulosegebiete hinaus als populationsfähig erwiesen haben.
- Eine weitere These stellt eine Korrelation zwischen der allgemeinen adulten Milchzuckertoleranz und der Erkrankungshäufigkeit in bestimmten Völkern fest. So ist die Rate in der europäischen und nordamerikanischen europäischstämmigen Bevölkerung, die jeweils eine hohe Milchzuckertoleranz aufweist, am höchsten, während sie in Asien bei der dort weit verbreiteten Milchzuckerintoleranz am niedrigsten liegt. Daraus ließe sich ein Zusammenhang ableiten und auch ein Selektionsvorteil für nichterkrankte Merkmalsträger, der den Gendefekt bisher nicht hat aussterben lassen.
Medizingeschichte


Aus Mutationsfrequenzanalysen weiß man, dass die Mukoviszidose eine sehr alte Krankheit ist. Die häufigsten Mutationen im CFTR-Gen entstanden vor ca. 50.000 Jahren im arabisch-vorderasiatischen Raum. Sehr wahrscheinlich war die ethnische Gruppe der Belutschen die Ursprungspopulation. Die lebten zu dieser Zeit auf dem Persischen Plateu in zentraler Lage eines querenden Völkerwanderungsweges. Über diesen Weg konnte sich die Mukoviszidose durch Wanderjäger sehr schnell nach Europa ausbreiten. Dort tauchten sie vor der letzten Eiszeit, etwa 30.000 bis 40.000 vor Christus im Beginn des Jungpaläolithikum,[88] erstmals auf.[89]
Rückblickend betrachtet lässt sich das Krankheitsbild Mukoviszidose in einer Reihe von Fallbeispielen ab der Mitte des 17. Jahrhunderts in der medizinischen Literatur finden.[90] Die Erkenntnis, dass es sich dabei um eine eigenständige Multisystemerkrankung handelt fehlte jedoch. Die erste genauere Beschreibung der Symptome einer geschwollenen, verhärteten, weißlich schimmernden Bauchspeicheldrüse stammt dabei aus einem Obduktionsbericht des Leidener Anatoms Peter Pauw aus dem Jahr 1595. Pauw untersuchte dabei die Leiche eines angeblich verhexten 11-jährigen Mädchens.[91]
Schon vor Jahrhunderten wurde der salzige Geschmack von Säuglingen als unheilvolles Zeichen für die Gesundheit des Kindes und die verkürzte Lebenserwartung erkannt. Ernst Ludwig Rochholz schrieb dazu 1857 in seinem Buch Alemannisches Kinderlied und Kinderspiel aus der Schweiz:
„Das Kind stirbt bald wieder, dessen Stirne beim Küssen salzig schmeckt.“
In der Literatur wird häufig die Version aus einem Wörterbuch der Schweizerdeutschen Sprache zitiert:
„Wehe dem Kind, das beim Kuss auf die Stirn salzig schmeckt, es ist verhext und muss bald sterben.“
Der Schweizer Kinderarzt Guido Fanconi beschrieb 1936[96] erstmals das Krankheitsbild der Mukoviszidose als „Coeliakiesyndrom bei angeborener zystischer Pankreasfibromatose“. In der Veröffentlichung schildern Fanconi und seine beiden Co-Autoren zwei Fälle einer offensichtlich tödlichen Krankheit von Kleinkindern. Sie gingen damals davon aus, dass es sich um ein sehr seltenes Syndrom handelt.[97]
Die Symptome der Erkrankung hatte allerdings der Österreicher Karl Landsteiner, der Entdecker der Blutgruppen, bereits 1905[98] beschrieben.[99] Landsteiner beschrieb den Fall eines Mädchens, das am fünften Lebenstag „mit einem aufgetriebenen Bauch“ gestorben war. Bei der Obduktion stellte er fest, dass das Mekonium graugelb und von ausgesprochen zäher Konsistenz, wie „eingedickter Glaserkitt“, war. In diesem Zustand konnte es nicht durch die Kräfte des Darms weiterbewegt werden. Landsteiner konstatierte:
„Es ist also zu erkennen, dass die abnorme Beschaffenheit des Meconiums die letzte Ursache des Darmverschlusses bildete, da die Eindickung schon längere Zeit (also schon im Mutterleib. F. K.) bestanden hat“
Im Pankreas des Mädchens fand er eine „sehr erhebliche Vermehrung“ des Bindegewebes (Fibrose).[100]
Den Begriff «Zystische Fibrose» (engl. cystic fibrosis) prägte die US-amerikanische Kinderärztin und Pathologin Dorothy Hansine Andersen 1938[101].[99] Sie orientierte sich dabei an den Gewebeveränderungen der betroffenen Organe mit Schleimdrüsen.[102] Außerdem definierte sie als erste das Krankheitsbild. [88] Der US-amerikanische Pathologe Sidney Farber nannte 1944 die Erkrankung wegen der Produktion zähen Schleims «Mukoviszidose».[103] Diese Bezeichnung hat sich vor allem im deutschsprachigen Raum durchgesetzt.
Mit der Verfügbarkeit der Antibiotika von Penicillin (ab 1944), Chlortetracyclin (ab 1948), Oxytetracyclin (ab 1950), Chloramphenicol und Erythromycin (beide ab 1951) wurde die Basis der palliativen Therapie der Mukoviszidose geschaffen.[91]
1949 erkannte Charles Upton Lowe (1921–2012),[104] dass es sich bei der Mukoviszidose um eine Erbkrankheit handelt. Er stellte außerdem den autosomal-rezessiven Erbgang fest und postulierte, dass die Erkrankung durch einen Defekt in einem einzelen Gen verursacht wird.[25] Die erste Veröffentlichung über den erhöhten Elektrolytgehalt im Schweiß von Mukoviszidosepatienten stammt aus dem Jahr 1953 von Paul di Sant’Agnese (1914–2005) und Kollegen.[88] Sie stellten bei neun Kindern mit Mukoviszidose eine um den Faktor drei erhöhte Chloridionenkonzentration im Schweiß fest.[105] Diese Erkenntnis wird bis heute im Schweißtest zur Diagnosestellung herangezogen. Zudem wurde eine wissenschaftliche Basis für die Erkenntnisse aus dem Mittelalter über den salzigen Geschmack des Schweißes bei Kindern mit Mukoviszidose geschaffen.[89] Diese Erkenntnis war auch die Grundlage für die Entwicklung des Pilocarpin-Iontophorese-Schweißtestes durch Lewis E. Gibson (1927–2008) und Robert E. Cooke (1920–2014) im Jahr 1959.[106] Die Ursache für die erhöhte Salzkonzentration fand Paul M. Quinton 1983 indem er isolierte Schweißdrüsenausführungsgänge (Ductus sudoriferus) von Mukoviszidosepatienten untersuchte und dabei eine sehr geringe Natriumchlorid-Reabsorption feststellte, die er durch eine abnorm geringe Chloridionen-Permeabilität der Endothelien verursacht wird.[107] Zwei Jahre wurde dann die molekulargentische Basis der Mukoviszidose gefunden. Eine internationale Arbeitsgruppe um Robert G. Knowlton identifizierte Chromosom 7 als Ort des Gendefekts.[108] 1989 wurde das CFTR-Gen erstmals kloniert[109][18] und die Drei-Basen-Deletion ΔF508 wurde als die Mutation erkannt, die für die meisten Fälle von Mukoviszidose verantwortlich ist.[110]
Durch die wachsenden Erkenntnisse über die Pathophysilogie der Mukoviszidose konnten in der Folgezeit neue Therapiekonzepte entwickelt werden, mit denen die Lebenserwartung der Betroffenen erheblich gesteigert werden konnte. Der vorläufige Höhepunkt ist die 2012 erfolgte Zulassung des ersten Medikaments, mit dem bei einem Teil der Patienten die Mukoviszidose ursächlich behandelt werden kann.
Weiterführende Literatur
- Margaret Hodson, Andrew Bush, Duncan Geddes: Cystic Fibrosis. 3. Auflage, CRC Press, 2012, ISBN 978-1-444-11369-3, 486 S. (eingeschränkte Vorschau in der Google-Buchsuche )
- Deutsche Gesellschaft für Pädiatrische Infektiologie (DGPI): DGPI-Handbuch. Infektionen bei Kindern und Jugendlichen. ZDB-ID 1308754-x.
- Kurt Kallenbach (Hrsg): Kinder mit besonderen Bedürfnissen. Ausgewählte Krankheitsbilder und Behinderungsformen. Marhold, Berlin 1998, ISBN 3-89166-208-4.
- Cormac Sheridan1: First cystic fibrosis drug advances towards approval. In: Nature Biotechnology. 29, 6, Juni 2011, ISSN 1087-0156, S. 465–456, doi:10.1038/nbt0611-465.
- Isabel Stenzel Byrnes, Anabel Stenzel: The Power of Two. A Twin Triumph Over Cystic Fibrosis. University of Missouri Press, Columbia MO 2007, ISBN 978-0-8262-1754-7.
- S1-Leitlinie Mukoviszidose (Cystische Fibrose): Ernährung und exokrine Pankreasinsuffizienz der Gesellschaft für Pädiatrische Gastroenterologie und Ernährung (GPGE). In: AWMF online (Stand 2011)
- S1-Leitlinie Diagnose der Mukoviszidose der Deutschen Gesellschaft für Kinder- und Jugendmedizin (DGKJ). In: AWMF online (Stand 2013)
Weblinks
- Cystic Fibrosis. In: Online Mendelian Inheritance in Man. (englisch)
- Mukovisdose e. V.
- Cystische Fibrose - Lernprogramm für Medizinstudenten der Uni Bern
- Lungeninformationsdienst.de - Mukoviszidose
Einzelnachweise
- ↑ a b c d e f g M. P. Boyle, K. De Boeck: A new era in the treatment of cystic fibrosis: correction of the underlying CFTR defect. In: The Lancet. Respiratory medicine. Band 1, Nummer 2, April 2013, ISSN 2213-2600, S. 158–163, doi:10.1016/S2213-2600(12)70057-7, PMID 24429096 (Review).
- ↑ a b M. S. Gelman, R. R. Kopito: Cystic fibrosis: premature degradation of mutant proteins as a molecular disease mechanism. In: Methods in molecular biology. Band 232, 2003, ISSN 1064-3745, S. 27–37, doi:10.1385/1-59259-394-1:27, PMID 12840537 (Review).
- ↑ A. Jaffé, A. Bush: Cystic fibrosis: review of the decade. In: Monaldi archives for chest disease = Archivio Monaldi per le malattie del torace / Fondazione clinica del lavoro, IRCCS [and] Istituto di clinica tisiologica e malattie apparato respiratorio, Università di Napoli, Secondo ateneo. Band 56, Nummer 3, Juni 2001, ISSN 1122-0643, S. 240–247, PMID 11665504 (Review).
- ↑ a b Daniel Merk, Manfred Schubert-Zsilavecz: Personalisierte Medizin: Neue Ansätze bei Mukoviszidose. In: pharmazeutische-zeitung.de. 2011, abgerufen am 13. März 2015.
- ↑ Antwort der Bundesregierung auf eine Kleine Anfrage: Bekämpfung der Mukoviszidose im Kindesalter Drucksache 9/2188, vom 26. November 1982 (PDF-Datei)
- ↑ G. Romeo, M. Devoto, L. J. Galietta: Why is the cystic fibrosis gene so frequent? In: Human genetics. Band 84, Nummer 1, Dezember 1989, ISSN 0340-6717, S. 1–5, PMID 2691388 (Review).
- ↑ a b G. Lucotte, S. Hazout, M. De Braekeleer: Complete map of cystic fibrosis mutation DF508 frequencies in Western Europe and correlation between mutation frequencies and incidence of disease. In: Human biology. Band 67, Nummer 5, Oktober 1995, ISSN 0018-7143, S. 797–803, PMID 8543293.
- ↑ a b c d J. L. Bobadilla, M. Macek u. a.: Cystic fibrosis: a worldwide analysis of CFTR mutations–correlation with incidence data and application to screening. In: Human mutation. Band 19, Nummer 6, Juni 2002, ISSN 1098-1004, S. 575–606, doi:10.1002/humu.10041, PMID 12007216 (Review).
- ↑ a b Cystic Fibrosis Mutation Database: Statistics. In: genet.sickkids.on.ca. Abgerufen am 11. März 2015 (englisch).
- ↑ a b C. Castellani, H. Cuppens u. a.: Consensus on the use and interpretation of cystic fibrosis mutation analysis in clinical practice. In: Journal of cystic fibrosis. Band 7, Nummer 3, Mai 2008, ISSN 1569-1993, S. 179–196, doi:10.1016/j.jcf.2008.03.009, PMID 18456578, PMC 2810954 (freier Volltext) (Review).
- ↑ N. Morral, J. Bertranpetit u. a.: The origin of the major cystic fibrosis mutation (delta F508) in European populations. In: Nature genetics. Band 7, Nummer 2, Juni 1994, ISSN 1061-4036, S. 169–175, doi:10.1038/ng0694-169, PMID 7920636.
- ↑ X. Estivill, C. Bancells, C. Ramos: Geographic distribution and regional origin of 272 cystic fibrosis mutations in European populations. The Biomed CF Mutation Analysis Consortium. In: Human mutation. Band 10, Nummer 2, 1997, ISSN 1059-7794, S. 135–154, doi:10.1002/(SICI)1098-1004(1997)10:2<135::AID-HUMU6>3.0.CO;2-J, PMID 9259197.
- ↑ O. Lao, A. M. Andrés u. a.: Spatial patterns of cystic fibrosis mutation spectra in European populations. In: European journal of human genetics. Band 11, Nummer 5, Mai 2003, ISSN 1018-4813, S. 385–394, doi:10.1038/sj.ejhg.5200970, PMID 12734544.
- ↑ E. Mateu, F. Calafell u. a.: Can a place of origin of the main cystic fibrosis mutations be identified? In: American journal of human genetics. Band 70, Nummer 1, Januar 2002, ISSN 0002-9297, S. 257–264, doi:10.1086/338243, PMID 11713719, PMC 384895 (freier Volltext).
- ↑ The CFTR mutations database: The CFTR gene. In: Universal Mutation Database. Abgerufen am 2. März 2015.
- ↑ R. Sebro, H. Levy u. a.: Cystic fibrosis mutations for p.F508del compound heterozygotes predict sweat chloride levels and pancreatic sufficiency. In: Clinical genetics. Band 82, Nummer 6, Dezember 2012, ISSN 1399-0004, S. 546–551, doi:10.1111/j.1399-0004.2011.01804.x, PMID 22035343, PMC 4279028 (freier Volltext).
- ↑ A. Ahmad, A. Ahmed, P. Patrizio: Cystic fibrosis and fertility. In: Current opinion in obstetrics & gynecology. Band 25, Nummer 3, Juni 2013, ISSN 1473-656X, S. 167–172, doi:10.1097/GCO.0b013e32835f1745, PMID 23429570 (Review).
- ↑ a b J. R. Riordan, J. M. Rommens u. a.: Identification of the cystic fibrosis gene: cloning and characterization of complementary DNA. In: Science. Band 245, Nummer 4922, September 1989, ISSN 0036-8075, S. 1066–1073, PMID 2475911.
- ↑ M. T. Clunes, R. C. Boucher: Cystic Fibrosis: The Mechanisms of Pathogenesis of an Inherited Lung Disorder. In: Drug discovery today. Disease mechanisms. Band 4, Nummer 2, 2007, ISSN 1740-6765, S. 63–72, doi:10.1016/j.ddmec.2007.09.001, PMID 18560471, PMC 2430075 (freier Volltext).
- ↑ Geraldine Leier: Mechanismus der CFTR-Aktivierung durch Sildenafil in Hinblick auf Mukoviszidose. Dissertation, Westfälische Wilhelms-Universität Münster, 2011, S. 6.
- ↑ a b C. L. Ward, R. R. Kopito: Intracellular turnover of cystic fibrosis transmembrane conductance regulator. Inefficient processing and rapid degradation of wild-type and mutant proteins. In: The Journal of biological chemistry. Band 269, Nummer 41, Oktober 1994, ISSN 0021-9258, S. 25710–25718, PMID 7523390.
- ↑ M. D. Amaral: CFTR and chaperones: processing and degradation. In: Journal of molecular neuroscience. Band 23, Nummer 1–2, 2004, ISSN 0895-8696, S. 41–48, doi:10.1385/JMN:23:1-2:041, PMID 15126691 (Review).
- ↑ a b S. J. Kim, W. R. Skach: Mechanisms of CFTR Folding at the Endoplasmic Reticulum. In: Frontiers in pharmacology. Band 3, 2012, ISSN 1663-9812, S. 201, doi:10.3389/fphar.2012.00201, PMID 23248597, PMC 3521238 (freier Volltext).
- ↑ D. N. Hebert, M. Molinari: In and out of the ER: protein folding, quality control, degradation, and related human diseases. In: Physiological reviews. Band 87, Nummer 4, Oktober 2007, ISSN 0031-9333, S. 1377–1408, doi:10.1152/physrev.00050.2006, PMID 17928587 (Review).
- ↑ a b S. M. Rowe, S. Miller, E. J. Sorscher: Cystic fibrosis. In: The New England journal of medicine. Band 352, Nummer 19, Mai 2005, ISSN 1533-4406, S. 1992–2001, doi:10.1056/NEJMra043184, PMID 15888700.
- ↑ M. Haardt, M. Benharouga u. a.: C-terminal truncations destabilize the cystic fibrosis transmembrane conductance regulator without impairing its biogenesis. A novel class of mutation. In: The Journal of biological chemistry. Band 274, Nummer 31, Juli 1999, ISSN 0021-9258, S. 21873–21877, PMID 10419506.
- ↑ Dirk Stolz: Zur Häufigkeit der Mutation CFTRdele2,3(21kb) im Gen CFTR in einem deutschen Patientenkollektiv. Dissertation, Justus-Liebig-Universität Gießen, 2006, S. 2.
- ↑ A. M. Cantin, G. Bilodeau u. a.: Oxidant stress suppresses CFTR expression. In: American journal of physiology. Cell physiology. Band 290, Nummer 1, Januar 2006, ISSN 0363-6143, S. C262–C270, doi:10.1152/ajpcell.00070.2005, PMID 16162662.
- ↑ A. M. Cantin, J. W. Hanrahan u. a.: Cystic fibrosis transmembrane conductance regulator function is suppressed in cigarette smokers. In: American journal of respiratory and critical care medicine. Band 173, Nummer 10, Mai 2006, ISSN 1073-449X, S. 1139–1144, doi:10.1164/rccm.200508-1330OC, PMID 16497995.
- ↑ E. F. McKone, J. Shao u. a.: Variants in the glutamate-cysteine-ligase gene are associated with cystic fibrosis lung disease. In: American journal of respiratory and critical care medicine. Band 174, Nummer 4, August 2006, ISSN 1073-449X, S. 415–419, doi:10.1164/rccm.200508-1281OC, PMID 16690975, PMC 2648118 (freier Volltext).
- ↑ a b N. C. Dean, D. H. Van Boerum, T. G. Liou: Rib plating of acute and sub-acute non-union rib fractures in an adult with cystic fibrosis: a case report. In: BMC research notes. Band 7, 2014, ISSN 1756-0500, S. 681, doi:10.1186/1756-0500-7-681, PMID 25270323, PMC 4197343 (freier Volltext).
- ↑ a b c d e R. M. Javier, J. Jacquot: Bone disease in cystic fibrosis: what's new? In: Joint, bone, spine. Band 78, Nummer 5, Oktober 2011, ISSN 1778-7254, S. 445–450, doi:10.1016/j.jbspin.2010.11.015, PMID 21233000 (Review).
- ↑ G. Döring, S. P. Conway: Osteoporosis in cystic fibrosis. In: Jornal de pediatria. Band 84, Nummer 1, 2008, ISSN 0021-7557, S. 1–3, doi:10.2223/JPED.1749, PMID 18264617.
- ↑ C. S. Haworth, P. L. Selby u. a.: Osteoporosis in adults with cystic fibrosis. In: Journal of the Royal Society of Medicine. Band 91 Suppl 34, 1998, ISSN 0141-0768, S. 14–18, PMID 9709383, PMC 1296368 (freier Volltext) (Review).
- ↑ a b R. M. Aris, J. B. Renner u. a.: Increased rate of fractures and severe kyphosis: sequelae of living into adulthood with cystic fibrosis. In: Annals of internal medicine. Band 128, Nummer 3, Februar 1998, ISSN 0003-4819, S. 186–193, PMID 9454526.
- ↑ S. M. Lang, R. Fischer u. a.: Hohe Osteoporose-Prävalenz bei erwachsenen Patienten mit zystischer Fibrose. In: Deutsche medizinische Wochenschrift (1946). Band 129, Nummer 28–29, Juli 2004, ISSN 0012-0472, S. 1551–1555, doi:10.1055/s-2004-828988, PMID 15243902.
- ↑ E. F. Shead, C. S. Haworth u. a.: Osteoclast function, bone turnover and inflammatory cytokines during infective exacerbations of cystic fibrosis. In: Journal of cystic fibrosis. Band 9, Nummer 2, März 2010, ISSN 1873-5010, S. 93–98, doi:10.1016/j.jcf.2009.11.007, PMID 20006563.
- ↑ E. F. Shead, C. S. Haworth u. a.: Osteoclastogenesis during infective exacerbations in patients with cystic fibrosis. In: American journal of respiratory and critical care medicine. Band 174, Nummer 3, August 2006, ISSN 1073-449X, S. 306–311, doi:10.1164/rccm.200512-1943OC, PMID 16675777.
- ↑ E. F. Shead, C. S. Haworth u. a.: Cystic fibrosis transmembrane conductance regulator (CFTR) is expressed in human bone. In: Thorax. Band 62, Nummer 7, Juli 2007, ISSN 0040-6376, S. 650–651, doi:10.1136/thx.2006.075887, PMID 17600296, PMC 2117234 (freier Volltext).
- ↑ L. Le Heron, C. Guillaume u. a.: Cystic fibrosis transmembrane conductance regulator (CFTR) regulates the production of osteoprotegerin (OPG) and prostaglandin (PG) E2 in human bone. In: Journal of cystic fibrosis. Band 9, Nummer 1, Januar 2010, ISSN 1873-5010, S. 69–72, doi:10.1016/j.jcf.2009.11.005, PMID 20005786.
- ↑ E. Shane, S. J. Silverberg u. a.: Osteoporosis in lung transplantation candidates with end-stage pulmonary disease. In: The American journal of medicine. Band 101, Nummer 3, September 1996, ISSN 0002-9343, S. 262–269, doi:10.1016/S0002-9343(96)00155-6, PMID 8873487.
- ↑ J. Yu, Z. Chen u. a.: CFTR mutations in men with congenital bilateral absence of the vas deferens (CBAVD): a systemic review and meta-analysis. In: Human reproduction. Band 27, Nummer 1, Januar 2012, ISSN 1460-2350, S. 25–35, doi:10.1093/humrep/der377, PMID 22081250 (Review).
- ↑ Thilo Dörk, Manfred Stuhrmann: Mukoviszidose (Zystische Fibrose, CF). In: Detlev Ganten, Klaus Ruckpaul: Monogen bedingte Erbkrankheiten Band 6, Springer-Verlag, 2013, ISBN 3-642-57043-7, S. 173-194 eingeschränkte Vorschau in der Google-Buchsuche
- ↑ Olaf Sommerburg: Mukoviszidose: Gendefekt mit schlimmen Folgen. In: pharmazeutische-zeitung.de. 2008, abgerufen am 16. März 2015.
- ↑ a b Claus Kroegel, Ulrich Costabel: Klinische Pneumologie: Das Referenzwerk für Klinik und Praxis. Georg Thieme, 2013, ISBN 3-131-75781-7, S. 655 eingeschränkte Vorschau in der Google-Buchsuche
- ↑ M. J. Müller, J. Westenhöfer u. a.: Ernährungsmedizinische Untersuchungen. In: Manfred James Müller: Ernährungsmedizinische Praxis: Methoden - Prävention - Behandlung. 2. Auflage, Springer-Verlag, 2007, ISBN 3-540-38231-3, S. 162 eingeschränkte Vorschau in der Google-Buchsuche
- ↑ J. Massie, B. Clements: Diagnosis of cystic fibrosis after newborn screening: the Australasian experience–twenty years and five million babies later: a consensus statement from the Australasian Paediatric Respiratory Group. In: Pediatric pulmonology. Band 39, Nummer 5, Mai 2005, ISSN 8755-6863, S. 440–446, doi:10.1002/ppul.20191, PMID 15704202 (Review).
- ↑ Corina S. Rueegg, Claudia E. Kuehni, Sabina Gallati, Matthias Baumgartner, Toni Torresani, Juerg Barben: Neugeborenen-Screening auf zystische Fibrose in der Schweiz: Evaluation nach einem Jahr . In: Deutsches Ärzteblatt. Band 110, Nr. 20. Deutscher Ärzte-Verlag, 17. Mai 2013, S. 356-63, doi:10.3238/arztebl.2013.0356.
- ↑ Mukoviszidose: Neugeborenen-Screening im Nordosten. In: aerztezeitung.de. 12. Oktober 2012, abgerufen am 16. März 2015.
- ↑ B. Sens, M. Stern (Hrsg.): Berichtsband: Qualitätssicherung Mukoviszidose .2012 Hippocampus Verlag, ISBN 978-3-88579-906-1, S. 39.
- ↑ a b M. Stopsack, J. Hammermann: Neugeborenenscreening auf Mukoviszidose. In: Monatsschrift Kinderheilkunde. Band 157, Nummer 12, S. 1222-1229 doi:10.1007/s00112-009-2042-6
- ↑ Lutz Nährlich, Klaus-Peter Zimmer: Neugeborenen-Screening auf Mukoviszidose: Lasst uns beginnen! . In: Deutsches Ärzteblatt. Band 110, Nr. 20. Deutscher Ärzte-Verlag, 17. Mai 2013, S. 354-5, doi:10.3238/arztebl.2013.0354.
- ↑ Ingeborg Bördlein: Angeborene Stoffwechselkrankheiten: Langzeitstudie belegt Nutzen des Neugeborenenscreenings . In: Deutsches Ärzteblatt. Band 108, Nr. 36. Deutscher Ärzte-Verlag, 9. September 2011, S. A-1855 / B-1581 / C-1570.
- ↑ D. S. Hardin: Growth problems and growth hormone treatment in children with cystic fibrosis. In: Journal of pediatric endocrinology & metabolism. Band 15 Suppl 2, Mai 2002, ISSN 0334-018X, S. 731–735, PMID 12092687 (Review).
- ↑ L. S. Conwell, A. B. Chang: Bisphosphonates for osteoporosis in people with cystic fibrosis. In: The Cochrane database of systematic reviews. Band 3, 2014, ISSN 1469-493X, S. CD002010, doi:10.1002/14651858.CD002010.pub4, PMID 24627308 (Review).
- ↑ G. L. McPhail, J. P. Clancy: Ivacaftor: the first therapy acting on the primary cause of cystic fibrosis. In: Drugs of today. Band 49, Nummer 4, April 2013, ISSN 1699-3993, S. 253–260, doi:10.1358/dot.2013.49.4.1940984, PMID 23616952.
- ↑ FDA approves Kalydeco to treat rare form of cystic fibrosis. In: fda.gov. 31. Januar 2012, abgerufen am 2. März 2015 (englisch).
- ↑ Kalydeco – ivacaftor. In: ema.europa.eu. 6. August 2012, abgerufen am 2. März 2015 (englisch).
- ↑ Zusammenfassung des EPAR für die Öffentlichkeit: Kalydeco - Ivacaftor. European Medicines Agency, Juli 2014 (PDF-Datei; 61 kB)
- ↑ K. Kotha, J. P. Clancy: Ivacaftor treatment of cystic fibrosis patients with the G551D mutation: a review of the evidence. In: Therapeutic advances in respiratory disease. Band 7, Nummer 5, Oktober 2013, ISSN 1753-4666, S. 288–296, doi:10.1177/1753465813502115, PMID 24004658 (Review).
- ↑ I. Sermet-Gaudelus: Ivacaftor treatment in patients with cystic fibrosis and the G551D-CFTR mutation. In: European respiratory review. Band 22, Nummer 127, März 2013, ISSN 1600-0617, S. 66–71, doi:10.1183/09059180.00008512, PMID 23457167 (Review).
- ↑ a b c rme/aerzteblatt.de: Mukoviszidose: Ivacaftor in Europa zugelassen. In: aerzteblatt.de. 27. Juli 2012, abgerufen am 6. März 2015.
- ↑ a b muko.info: Ivacaftor (Kalydeco®; VX-770) in Deutschland zugelassen. In: muko.info. 29. November 2012, abgerufen am 6. März 2015.
- ↑ a b Andrew Pollack: F.D.A. Approves New Cystic Fibrosis Drug. In: nytimes.com. 31. Januar 2012, abgerufen am 6. März 2015 (englisch).
- ↑ a b Neue Arzneimittel 2012/2013 – eine kritische Bewertungeine kritische Bewertung. Vortrag auf einer Fortbildungsveranstaltung der deutschen Arzneimittelkommission der deutschen Ärzteschaft gemeinsam mit der Ärztekammer Sachsen-Anhalt und der KV Sachsen-Anhalt 27. April 2013 in Halle (Saale); (PDF-Datei)
- ↑ N. Derichs: Targeting a genetic defect: cystic fibrosis transmembrane conductance regulator modulators in cystic fibrosis. In: European respiratory review. Band 22, Nummer 127, März 2013, ISSN 1600-0617, S. 58–65, doi:10.1183/09059180.00008412, PMID 23457166 (Review-Artikel, im Volltext frei zugänglich).
- ↑ V. Teichgräber, M. Ulrich u. a.: Ceramide accumulation mediates inflammation, cell death and infection susceptibility in cystic fibrosis. In: Nature medicine. Band 14, Nummer 4, April 2008, ISSN 1546-170X, S. 382–391, doi:10.1038/nm1748, PMID 18376404.
- ↑ Neue Behandlungsmethode für Mukoviszidose. In: science.orf.at. 30. März 2008, abgerufen am 6. März 2015.
- ↑ J. Kornhuber, M. Muehlbacher u. a.: Identification of novel functional inhibitors of acid sphingomyelinase. In: PloS one. Band 6, Nummer 8, 2011, ISSN 1932-6203, S. e23852, doi:10.1371/journal.pone.0023852, PMID 21909365, PMC 3166082 (freier Volltext).
- ↑ T. G. Liou, F. R. Adler u. a.: Lung transplantation and survival in children with cystic fibrosis. In: The New England journal of medicine. Band 357, Nummer 21, November 2007, ISSN 1533-4406, S. 2143–2152, doi:10.1056/NEJMoa066359, PMID 18032764, PMC 2522236 (freier Volltext).
- ↑ a b T. A. VanWort, J. A. Lee u. a.: Female cystic fibrosis mutation carriers and assisted reproductive technology: does carrier status affect reproductive outcomes? In: Fertility and sterility. Band 102, Nummer 5, November 2014, ISSN 1556-5653, S. 1324–1330, doi:10.1016/j.fertnstert.2014.07.1234, PMID 25217870.
- ↑ N. Sharer, M. Schwarz u. a.: Mutations of the cystic fibrosis gene in patients with chronic pancreatitis. In: The New England journal of medicine. Band 339, Nummer 10, September 1998, ISSN 0028-4793, S. 645–652, doi:10.1056/NEJM199809033391001, PMID 9725921.
- ↑ J. A. Cohn, K. J. Friedman u. a.: Relation between mutations of the cystic fibrosis gene and idiopathic pancreatitis. In: The New England journal of medicine. Band 339, Nummer 10, September 1998, ISSN 0028-4793, S. 653–658, doi:10.1056/NEJM199809033391002, PMID 9725922.
- ↑ Tilman Horn: Pankreatitis bei Patienten mit Hyperparathyreoidismus: Assoziation mit Mutationen im SPINK1 und CFTR Gen. Dissertation, Ruhr-Universität Bochum, Fakultät für Medizin, 2009, S. 47.
- ↑ J. O. Warner, A. P. Norman, J. F. Soothill: Cystic fibrosis heterozygosity in the pathogenesis of allergy. In: Lancet. Band 1, Nummer 7967, Mai 1976, ISSN 0140-6736, S. 990–991, PMID 57442.
- ↑ M. Dahl, A. Tybjaerg-Hansen u. a.: DeltaF508 heterozygosity in cystic fibrosis and susceptibility to asthma. In: Lancet. Band 351, Nummer 9120, Juni 1998, ISSN 0140-6736, S. 1911–1913, PMID 9654257.
- ↑ C. Lázaro, R. de Cid u. a.: Missense mutations in the cystic fibrosis gene in adult patients with asthma. In: Human mutation. Band 14, Nummer 6, 1999, ISSN 1059-7794, S. 510–519, doi:10.1002/(SICI)1098-1004(199912)14:6<510::AID-HUMU10>3.0.CO;2-O, PMID 10571949.
- ↑ S. A. Schroeder, D. M. Gaughan, M. Swift: Protection against bronchial asthma by CFTR delta F508 mutation: a heterozygote advantage in cystic fibrosis. In: Nature medicine. Band 1, Nummer 7, Juli 1995, ISSN 1078-8956, S. 703–705, PMID 7585155.
- ↑ N. Maurya, S. Awasthi, P. Dixit: Association of CFTR gene mutation with bronchial asthma. In: The Indian journal of medical research. Band 135, Nummer 4, April 2012, ISSN 0971-5916, S. 469–478, PMID 22664493, PMC 3385229 (freier Volltext) (Review).
- ↑ I. Gallego Romero, C. Ober: CFTR mutations and reproductive outcomes in a population isolate. In: Human genetics. Band 122, Nummer 6, Januar 2008, ISSN 1432-1203, S. 583–588, doi:10.1007/s00439-007-0432-1, PMID 17901983.
- ↑ M. Dahl, A. Tybjaerg-Hansen u. a.: Cystic fibrosis Delta F508 heterozygotes, smoking, and reproduction: studies of 9141 individuals from a general population sample. In: Genomics. Band 50, Nummer 1, Mai 1998, ISSN 0888-7543, S. 89–96, doi:10.1006/geno.1998.5272, PMID 9628826.
- ↑ S. V. Raju, J. H. Tate u. a.: Impact of heterozygote CFTR mutations in COPD patients with chronic bronchitis. In: Respiratory research. Band 15, 2014, ISSN 1465-993X, S. 18, doi:10.1186/1465-9921-15-18, PMID 24517344, PMC 3925354 (freier Volltext).
- ↑ C. R. Lake, P. B. Davis u. a.: Electrolytes and norepinephrine levels in blood of patients with cystic fibrosis. In: Clinica chimica acta; international journal of clinical chemistry. Band 92, Nummer 2, März 1979, ISSN 0009-8981, S. 141–146, PMID 487568.
- ↑ a b c M. Super, A. Irtiza-Ali u. a.: Blood pressure and the cystic fibrosis gene: evidence for lower pressure rises with age in female carriers. In: Hypertension. Band 44, Nummer 6, Dezember 2004, ISSN 1524-4563, S. 878–883, doi:10.1161/01.HYP.0000145901.81989.46, PMID 15477385.
- ↑ J. Lieberman, S. Rodbard: Low blood pressure in young adults with cystic fibrosis: an effect of chronic salt loss in sweat? In: Annals of internal medicine. Band 82, Nummer 6, Juni 1975, ISSN 0003-4819, S. 806–808, PMID 1138590.
- ↑ J. J. Guo, D. A. Stoltz u. a.: Genotype-specific alterations in vascular smooth muscle cell function in cystic fibrosis piglets. In: Journal of cystic fibrosis. Band 13, Nummer 3, Mai 2014, ISSN 1873-5010, S. 251–259, doi:10.1016/j.jcf.2013.10.009, PMID 24183914, PMC 3972271 (freier Volltext).
- ↑ V. A. Peotta, P. Bhandary u. a.: Reduced blood pressure of CFTR-F508del carriers correlates with diminished arterial reactivity rather than circulating blood volume in mice. In: PloS one. Band 9, Nummer 5, 2014, ISSN 1932-6203, S. e96756, doi:10.1371/journal.pone.0096756, PMID 24801204, PMC 4011854 (freier Volltext).
- ↑ a b c Gerhard Dockter, Hermann Lindemann: In: Hermann Lindemann, Burckhardt Tümmler, Gerhard Dockter (Hrsg): Mukoviszidose – Zystische Fibrose. 4. Auflage, Georg Thieme, 2004, ISBN 3-131-38604-5, S. 1–2 eingeschränkte Vorschau in der Google-Buchsuche
- ↑ a b Ulrich Grossekettler: Erhöhte Serum-Konzentrationen von IL-18 und IL-12 p40 bei Mukoviszidose Dissertation, Johann Wolfgang Goethe-Universität Frankfurt am Main, 2005, S. 5 eingeschränkte Vorschau in der Google-Buchsuche
- ↑ R. Busch: On the history of cystic fibrosis. In: Acta Universitatis Carolinae. Medica. Band 36, Nummer 1–4, 1990, ISSN 0001-7116, S. 13–15, PMID 2130674 (Review).
- ↑ a b James M. Littlewood: History of cystic fibrosis. In: Margaret Hodson, Andrew Bush, Duncan Geddes: Cystic Fibrosis. 3. Auflage, CRC Press, 2012, ISBN 978-1-444-11369-3, S. 3–19 (eingeschränkte Vorschau in der Google-Buchsuche ).
- ↑ Ernst Ludwig Rochholz: Alemannisches Kinderlied und Kinderspiel aus der Schweiz J.J. Weber, Leipzig, 1857 eingeschränkte Vorschau in der Google-Buchsuche
- ↑ M. Griese, D. Reinhardt: Differentialdiagnose pathologischer Schweißtestresultate In: Dietrich Reinhardt, Manfred Götz, Richard Kraemer, Martin H. Schöni (Hrsg.): Cystische Fibrose. Springer-Verlag, 2013, ISBN 978-3-642-56796-4, S. 212 (eingeschränkte Vorschau in der Google-Buchsuche ).
- ↑ C. Falkman: Cystic fibrosis–a psychological study of 52 children and their families. In: Acta paediatrica Scandinavica. Supplement. Nummer 269, 1977, ISSN 0300-8843, S. 1–93, PMID 274900.
- ↑ J. X. Pfyffer: Zitierend aus dem Wörterbuch der Schweizerdeutschen Sprache Band 7, 1848, S. 899. Siehe dazu: James L. Littlewood: History of cystic fibrosis. In: Margaret Hodson, Andrew Bush, Duncan Geddes: Cystic Fibrosis. 3. Auflage, CRC Press, 2012, ISBN 978-1-444-11369-3, 486 S. (eingeschränkte Vorschau in der Google-Buchsuche )
- ↑ G. Fanconi, E. Uehlinger, C. Knauer: Das Coeliakiesyndrom bei angeborener zystischer Pankreasfibrose und Bronchiektasien. In: Wien Med Wochenschr. Band 86, 1936, S. 753–756.
- ↑ U. Stephan, M. Götz, K. Stephan, S. Bender: Cystic Fibrosis. In: P. Frick, G.-A. von Harnack, G. A. Martini, A. Prader, H. P. Wolff (Hrsg.): Advances in Internal Medicine and Pediatrics. Band 44, Springer Berlin Heidelberg, 1980, ISBN 978-3-642-67559-1, S. 73–174 doi:10.1007/978-3-642-67557-7_3
- ↑ a b K. Landsteiner: Darmverschluss durch eingedicktes Meconium: Pankreatitis. In: Centralblatt für allgemeine Pathologie und pathologische Anatomie. Band 16, 1905, S. 903.
- ↑ a b Ralf Bröer: Ein Pädiater, der streng, neugierig und menschlich war. In: aerztezeitung.de. 11. Oktober 2004, abgerufen am 12. März 2015.
- ↑ Friedrich Katscher: Hoffnung für Mukoviszidosekranke. In: wienerzeitung.at. 26. November 1999, abgerufen am 12. März 2015.
- ↑ D. H. Andersen: Cystic fibrosis of the pancreas and its relation to celiac disease. In: American Journal of Diseases of Children. Band 56, 1938, S. 344–399.
- ↑ S. Zabransky, S. Isabel Zink: IRT-Bestimmung in Vollblutproben getrocknet auf Filterpapier als Suchtest auf Cystische Fibrose In: Siegfried Zabransky (Hrsg.): Screening auf angeborene endokrine und metabole Störungen. 2001, S. 269-296 doi:10.1007/978-3-7091-6252-1_33, ISBN 978-3-7091-7260-5
- ↑ S. Farber: Pancreatic function and disease in early life. V. Pathology changes associated with pancreatic insufficiency in early life. In: Arch Path. Band 37, 1944, S. 238.
- ↑ C. U. Lowe, C. D. May, S. C. Reed: Fibrosis of the pancreas in infants and children; a statistical study of clinical and hereditary features. In: American journal of diseases of children. Band 78, Nummer 3, September 1949, ISSN 0096-8994, S. 349–374, doi:10.1001/archpedi.1949.02030050362008, PMID 18138931.
- ↑ R. C. Darling, P. A. di Sant’Agnese u. a.: Electrolyte abnormalities of the sweat in fibrocystic disease of the pancreas. In: The American journal of the medical sciences. Band 225, Nummer 1, Januar 1953, ISSN 0002-9629, S. 67–70, PMID 13007698.
- ↑ L. E. Gibson, R. E. Cooke: A test for concentration of electrolytes in sweat in cystic fibrosis of the pancreas utilizing pilocarpine by iontophoresis. In: Pediatrics. Band 23, Nummer 3, März 1959, ISSN 0031-4005, S. 545–549, PMID 13633369.
- ↑ P. M. Quinton: Chloride impermeability in cystic fibrosis. In: Nature. Band 301, Nummer 5899, Februar 1983, ISSN 0028-0836, S. 421–422, PMID 6823316.
- ↑ R. G. Knowlton, O. Cohen-Haguenauer u. a.: A polymorphic DNA marker linked to cystic fibrosis is located on chromosome 7. In: Nature. Band 318, Nummer 6044, 1985 Nov 28-Dec 4, ISSN 0028-0836, S. 380–382, PMID 2999611.
- ↑ J. M. Rommens, M. C. Iannuzzi u. a.: Identification of the cystic fibrosis gene: chromosome walking and jumping. In: Science. Band 245, Nummer 4922, September 1989, ISSN 0036-8075, S. 1059–1065, PMID 2772657.
- ↑ W. K. Lemna, G. L. Feldman u. a.: Mutation analysis for heterozygote detection and the prenatal diagnosis of cystic fibrosis. In: The New England journal of medicine. Band 322, Nummer 5, Februar 1990, ISSN 0028-4793, S. 291–296, doi:10.1056/NEJM199002013220503, PMID 2296270. (Volltext frei zugänglich)