Calciumformiat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Calciumformiat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C2H2CaO4 | |||||||||||||||
| Kurzbeschreibung |
farbloser, fast geruchloser Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 130,11 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,02 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt |
>380 °C (Zersetzung)[3] | |||||||||||||||
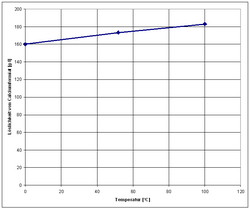
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Calciumformiat ist eine chemische Verbindung aus der Gruppe der Formiate, also das Calciumsalz der Ameisensäure mit der Konstitutionsformel Ca(HCOO)2.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Calciumformiat kommt sehr selten in Form des Minerals Formicait vor.[5]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]

Calciumformiat kann durch Reaktion von Kohlenmonoxid mit Calciumhydroxid[6]
oder Reaktion von Formaldehyd mit einer Calciumverbindung in wässriger Lösung (zum Beispiel Calciumhydroxid oder Calciumperoxid) gewonnen werden.[7] Es entsteht auch als Beiprodukt bei der Herstellung von Polyolen (zum Beispiel Trimethylolpropan).[8]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Calciumformiat ist farbloser, fast geruchloser Feststoff. Es ist das Calciumsalz der Ameisensäure. Es kristallisiert im orthorhombischen Kristallsystem in der Raumgruppe Pcab (Raumgruppen-Nr. 61, Stellung 2) mit den Gitterparametern a = 1016,8 pm, b = 1340,7 pm und c = 627,8 pm. In der Elementarzelle befinden sich acht Formeleinheiten.[10]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Calciumformiat wird zur Erzeugung von Ameisensäure, als Hilfsmittel in der Gerberei, als Abbindebeschleuniger für zementgebundene Baustoffe, als Hilfsmittel zur Aufarbeitung von Ölemulsionen, zur Herstellung von Silierhilfsmitteln und Additiven für die Tierernährung verwendet.[11] Die Verbindung wurde früher auch als Lebensmittelzusatzstoff (Konservierungsstoff E238) eingesetzt, ist aber seit 1998 nicht mehr zugelassen.[12]
Weblinks[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Register of Feed Additives pursuant to Regulation (EC) No 1831/2003. (pdf) Annex I: List of additives. In: Europäische Kommission. European Union, 2021, S. 91, abgerufen am 21. November 2021.
- ↑ Hermann Römpp: Chemie Lexikon. 5. Auflage. Franckh'sche Verlagsbuchhandlung, W. Keller & Co., Stuttgart 1962.
- ↑ a b c d e f Eintrag zu Calciumformiat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Richard J. Lewis, Sr.: Hawley's Condensed Chemical Dictionary. 15. Auflage. Wiley-Interscience, 2007, ISBN 978-0-471-76865-4 (englisch).
- ↑ mineralienatlas.de: Formicait
- ↑ Ullmann's Enzyklopädie der Organischen Chemie
- ↑ Patentanmeldung EP0510375A1: Verfahren zur Herstellung von Calciumformiat. Angemeldet am 27. März 1992, veröffentlicht am 28. Oktober 1992, Anmelder: Degussa, Erfinder: Peter Werle et al.
- ↑ runyoutech.com: Calciumformate.
- ↑ H. Stanley: The Solubility of Some Salts of the Lower Fatty Acids. In: The Chemical News. 1904, 89, S. 193. Volltext.
- ↑ N. Burger, H. Fuess, S. A. Mason: Neutron diffraction of [alpha]-calcium formate at 100 and 296 K. In: Acta Cryst. 1977, B33, S. 1968–1970, doi:10.1107/S0567740877007444.
- ↑ Chemische Fabrik Kalk: Anwendungen Calciumformiat.
- ↑ bdsoft: Calciumformiat als Lebensmittelzusatzstoff.

