Oxalsäure
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
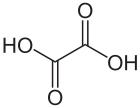
| ||||||||||
| Allgemeines | ||||||||||
| Name | Oxalsäure | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C2H2O4 | |||||||||
| Kurzbeschreibung |
farb- und geruchloser, kristalliner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | ||||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte | ||||||||||
| Schmelzpunkt | ||||||||||
| Sublimationspunkt | ||||||||||
| pKS-Wert | ||||||||||
| Löslichkeit |
mäßig in Wasser (90–100 g·l−1 bei 20 °C)[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| MAK |
Schweiz: 1 mg·m−3 (gemessen als einatembarer Staub)[7] | |||||||||
| Toxikologische Daten | ||||||||||
| Thermodynamische Eigenschaften | ||||||||||
| ΔHf0 |
−829,9 kJ/mol[9] | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Oxalsäure (systematischer Name Ethandisäure und historisch: Kleesäure[10] und Acidum oxalicum) ist die einfachste Dicarbonsäure. Ihre Salze heißen Oxalate (systematisch: Ethandioate). Oxalsäure ist auch ein Reduktionsmittel und kann daher quantitativ durch Titration mit einem Oxidationsmittel wie Kaliumpermanganat bestimmt werden, dabei entsteht Kohlenstoffdioxid als Oxidationsprodukt.
Geschichte
Oxalsäure wurde 1769 durch Johann Christian Wiegleb im Sauerklee (Oxalis acetosella, daher der Name) als Kaliumsalz entdeckt und war daher erst unter dem Namen Kleesäure bekannt. 1776 konnte sie in größeren Mengen durch Carl Wilhelm Scheele und Torbern Olof Bergman durch Oxidation von Zucker mit Salpetersäure hergestellt werden, was noch keine Synthese, sondern der Abbau eines Naturstoffes war. (Auf dieses Verfahren geht auch der historische Name Zuckersäure, die heute als Glucarsäure bezeichnet wird, zurück.) Oxalsäure wurde dann 1824 erstmals von Friedrich Wöhler künstlich aus anorganischen Grundstoffen hergestellt (synthetisiert durch Verseifung von Dicyan, (CN)2).[11]

Vorkommen
Oxalsäure und ihr Kaliumsalz kommen in größeren Mengen in Rhabarber (180–765 mg/100 g Frischgewicht, Stiele) und anderen Knöterichgewächsen (Polygonaceen) vor wie z. B. Sauerampfer, das meiste davon in den Blättern, weshalb nur der Stiel des Rhabarbers nach dem Kochen zum Verzehr geeignet ist. Auch Sternfrüchte (Averrhoa carambola) enthalten viel Oxalsäure (40–1000 mg/100 g Frischsubstanz). In ähnlichen Mengen kommt Oxalsäure aber auch im namensgebenden Sauerklee (Oxalis), Mangold (110–940 mg/100 g Frischgewicht), Spinat (120–1330 mg/100 g Frischgewicht), Petersilie (0–185 mg/100 g Frischgewicht), Kakao (338–480 mg/100 g), Schokolade (80–200 mg/100 g) und Roten Rüben (17–329 mg/100 g Frischgewicht) vor. Ferner wird Oxalsäure von vielen Pilzen ausgeschieden; ihre Produktion wird durch alkalische Reaktion der Nährlösung gefördert.[12][13]
Vorkommen in Nahrungsmitteln
| Pflanze | Oxalsäure (g/100 g)[14] |
|---|---|
| Amaranth | 1.09 |
| Spargel | 0.13 |
| grüne Bohne | 0.36 |
| rote Beete (Blätter) | 0.61 |
| Brokkoli | 0.19 |
| Rosenkohl | 0.36 |
| Kohl | 0.10 |
| Karotte | 0.50 |
| Kassave | 1.26 |
| Blumenkohl | 0.15 |
| Sellerie | 0.19 |
| Chicoree | 0.2 |
| Schnittlauch | 1.48 |
| Blattkohl | 0.45 |
| Koriander | 0.01 |
| Zuckermais | 0.01 |
| Gurke | 0.02 |
| Aubergine | 0.19 |
| Endivie | 0.11 |
| Knoblauch | 0.36 |
| Grünkohl | 0.02 |
| Gartensalat | 0.33 |
| Okra | 0.05 |
| Zwiebel | 0.05 |
| Petersilie | 1.70 |
| Pastinak | 0.04 |
| Erbse | 0.05 |
| Paprika | 0.04 |
| Kartoffel | 0.05 |
| Portulak | 1.31 |
| Radieschen | 0.48 |
| Rhabarberblätter | 0.52[15] |
| Steckrübe | 0.03 |
| Spinat | 0.97 |
| Kürbisse | 0.02 |
| Süßkartoffel | 0.24 |
| Tomate | 0.05 |
| Speiserübe | 0.21 |
| Speiserübenlätter | 0.05 |
| Brunnenkresse | 0.31 |
Gewinnung und Darstellung
Heutzutage wird Oxalsäure durch rasches Erhitzen von Natriumformiat auf 360 °C hergestellt.
Das erhaltene Natriumoxalat wird mit Calciumhydroxid zunächst in das schwerlösliche Calciumoxalat überführt:
Daraus wird durch Zugabe von Schwefelsäure das Endprodukt Oxalsäure freigesetzt; als Nebenprodukt entsteht Calciumsulfat:
Die weltweite Produktion von Oxalsäure und ihren Estern liegt bei 140.000 Tonnen pro Jahr.

Eigenschaften
Chemische Eigenschaften
Oxalsäure ist durch die Nachbarstellung der Carboxygruppen eine starke Säure. Beim Erhitzen über 150 °C zerfällt sie unter Bildung von Kohlenstoffmonoxid, Kohlenstoffdioxid und Wasser. Die Zersetzung erfolgt in zwei Schritten über die Bildung von Ameisensäure:
In ähnlicher Weise zerfällt Oxalsäure in konzentrierter Schwefelsäure sofort zu Kohlenstoffmonoxid, Kohlenstoffdioxid und Wasser. Oxalsäure kristallisiert aus wässrigen Lösungen mit zwei Molekülen Kristallwasser zum Oxalsäure-Dihydrat ((COOH)2 · 2 H2O). Oxalsäure und ihre löslichen Salze sind gesundheitsschädlich.
Verwendung
Oxalsäure kann zur Entfernung von Rostflecken oder als Bleichmittel verwendet werden.
In der Imkerei wird Oxalsäure als Winterbehandlung zur Bekämpfung der Varroamilbe eingesetzt. Sie wird als 3,5-prozentige wässrige Zuckerlösung auf die Bienen geträufelt oder gesprüht. Für Imker, die Oxalsäure gegen Varroose verwenden, bestehen Gefahren beim Kontakt mit Oxalsäure.[16]
Im analytischen Labor wird das Dihydrat der Oxalsäure als Urtitersubstanz für die Manganometrie verwendet. Weiterhin dient sie als Urtitersubstanz zur exakten Gehaltbestimmung von alkalischen Maßlösungen, etwa von Natronlauge. Durch die Bildung eines schwer löslichen Calcium-Salzes ist es außerdem zur gravimetrischen Bestimmung von Calcium-Ionen als Calciumoxalat von Bedeutung.
Im Fichtelgebirge wurde aus Sauerklee gewonnene Oxalsäure zum Bleichen von Quarz (Bergkristall) benutzt, welcher hier vorwiegend unter der Stadt Weißenstadt vorkommt.
In der Steinverarbeitung wird Oxalsäure (Kleesalz) zum Glanzpolieren von Marmor verwendet.
In der Holzbearbeitung dient Oxalsäure als mildere Bleiche (im Vergleich zum Wasserstoffperoxid) für Holz, wird aber vor allem zur Entfernung von reaktiv hervorgerufenen Flecken verwendet, die auf eine Reaktion von Gerbsäuren (als Inhaltsstoffe des Holzes) mit Metallionen schwarze Flecken im Holz verursacht wurden, beispielsweise durch Kontakt von gerbsäurehaltigen Hölzern mit eisernen Werkzeugen.[17][18]
In der Arzneistoff-Chemie wird Oxalsäure als Salzbildner eingesetzt. Durch Protonierung basischer Amine entstehen so Oxalate.
Biologische Bedeutung
Oxalsäure ist in höherer Konzentration gesundheitsschädlich, kommt in geringer Konzentration aber in Lebensmitteln wie Tee (insbesondere schwarzer Tee und Pfefferminztee, siehe auch Vorkommen) und in Wurzeln und Rinden zahlreicher Pflanzen als unlösliches Calciumoxalat[3] vor. Calciumoxalat entsteht in der Natur häufig beim Absterben von Pflanzenzellen. Es kann unter polarisiertem Licht in Form von hellen rechteckigen Kristallen erkannt werden (besonders einfach in braunen Zwiebelschalen). Nierensteine bestehen meist aus Calciumoxalat und Harnsäure, die Steinbildung wird aber durch Zitronensäure, welche in Früchten vorkommt, verhindert.
Da Oxalsäure die Resorption (Aufnahme) von Eisen im Darm erschwert, sollte man bei einer Eisentherapie, z. B. im Rahmen einer Eisenmangelanämie, mit dem Verzehr stark oxalsäurehaltiger Lebensmittel zurückhaltend sein und diese auch nicht gleichzeitig mit der Einnahme von Eisentabletten zu sich nehmen. Nach Aufnahme von Oxalsäure kommt es im betroffenen Gewebe zu einer Verarmung an Calcium, in schweren Fällen kann dies eine Schädigung des Herzens zur Folge haben. Nach Aufnahme von größeren Dosen kann es zu Lähmungserscheinungen kommen, in jedem Fall (auch bei leichten Vergiftungen) kommt es zu Nierenschäden durch verstopfte Nierentubuli. Die letale Dosis (LDLo beim Menschen, oral) wird mit 600 mg pro kg Körpergewicht[19] angegeben.
Literatur
- Heinz G. O. Becker: Organikum: organisch-chemisches Grundpraktikum. 23. Auflage. Wiley-VCH, Weinheim 2009, ISBN 978-3-527-32292-3.
- Hans Günther Schlegel: Allgemeine Mikrobiologie. 8. Auflage. Thieme, Stuttgart/New York 2007, ISBN 978-3-13-444608-1.
Einzelnachweise
- ↑ a b c d e f Eintrag zu Oxalsäure in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ a b c W. Riemenschneider, M. Tanifuji: Oxalic Acid in Ullmann's Encyclopedia of Industrial Chemistry, 2012 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, doi:10.1002/14356007.a18_247.pub2.
- ↑ a b Eintrag zu Oxalsäure. In: Römpp Online. Georg Thieme Verlag
- ↑ a b c David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-406.
- ↑ a b chem.wisc.edu: pKa Data, Compiled by R. Williams (PDF, 78 kB).
- ↑ Eintrag zu Oxalic acid im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA) Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte
- ↑ Eintrag in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-21.
- ↑ Lexikoneintrag von 1857 zu "Kleesäure"
- ↑ Burckhard Frank: 250 Jahre Chemie in Göttingen. In: Hans-Heinrich Voigt (Hrsg.): Naturwissenschaften in Göttingen. Eine Vortragsreihe. Vandenhoeck + Ruprecht Gm, Göttingen 1988, ISBN 3-525-35843-1 (Göttinger Universitätsschriften. Band 13), S. 72 (eingeschränkte Vorschau in der Google-Buchsuche und eingeschränkte Vorschau in der Google-Buchsuche)
- ↑ Hans Günther Schlegel: Allgemeine Mikrobiologie. 8. Auflage. Thieme, Stuttgart/New York 2007, ISBN 978-3-13-444608-1.
- ↑ C. Wehmer: Ueber Oxalsäure-Bildung durch Pilze. In: Justus Liebigs Annalen der Chemie, 269, 2–3, 1892, S. 383–389, doi:10.1002/jlac.18922690214.
- ↑ All data not specifically annotated is from Agriculture Handbook No. 8-11, Vegetables and Vegetable Products, 1984. ("Nutrient Data : Oxalic Acid Content of Selected Vegetables". ars.usda.gov)
- ↑ GW Pucher, AJ Wakeman, HB Vickery: The organic acids of rhubarb (Rheum hybridium). III. The behavior of the organic acids during culture of excised leaves. In: Journal of Biological Chemistry. 126. Jahrgang, Nr. 1, 1938, S. 43 (jbc.org).
- ↑ Varroabehandlung mit Oxalsäure (PDF), Arbeitsblatt 334, Landesbetrieb Landwirtschaft, Hessen, Bieneninstitut Kirchhain.
- ↑ David Charlesworth: Furniture-making Techniques, Vol. 2. Guild of Master Craftsmen Publications Ltd., Lewes (East Sussex, UK) 2001, ISBN 1-86108-295-9. (Seite 86)
- ↑ Declan O'Donoghue: The Complete Book of Woodworking. Lyons Press, London (UK) 2001, ISBN 1-59228-177-X. (Seite 94)
- ↑ Yakkyoku (1980). In: Pharmacy. Bd. 31, S. 959.
Weblinks
- Chemie verstehen: Oxalsäure






