Poliomyelitis
| Klassifikation nach ICD-10 | |
|---|---|
| A80.0 | Akute paralytische Poliomyelitis durch Impfvirus |
| A80.1 | Akute paralytische Poliomyelitis durch importiertes Wildvirus |
| A80.2x | Akute paralytische Poliomyelitis durch einheimisches Wildvirus |
| A80.3 | Sonstige und nicht näher bezeichnete akute paralytische Poliomyelitis |
| A80.4 | Akute nichtparalytische Poliomyelitis |
| A80.9 | Akute Poliomyelitis, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |
Poliomyelitis (von altgriechisch πολιός poliós, deutsch ‚grau, weißlich‘ und μυελός myelós, deutsch ‚Mark‘),[1][2] oder Poliomyelitis acuta, kurz Polio, deutsch (spinale) Kinderlähmung, Polioerkrankung oder Heine-Medin-Krankheit genannt,[3] ist eine von Polioviren vorwiegend im Kindesalter hervorgerufene Infektionskrankheit. Die ursprüngliche Bezeichnung leitet sich von den Entdeckern des Virus, Jakob von Heine und Karl Oskar Medin, ab. Sie befällt Motoneurone und kann zu schwerwiegenden, bleibenden Lähmungen führen. Diese betreffen häufig die Extremitäten. Der Befall der Atemmuskulatur ist tödlich, als Reaktion führte dieser Krankheitsverlauf zur Entwicklung der ersten maschinellen Beatmungsverfahren. Auch Jahre nach einer Infektion kann die Krankheit wieder auftreten.
Das Virus wird meist durch Schmierinfektion (Urin oder Stuhl) übertragen, aber auch Tröpfcheninfektionen sind möglich. Es kann sich nur im Menschen (und einigen Affenarten) vermehren und nur von Mensch zu Mensch übertragen werden.[4]
Seit den 1950er Jahren sind Impfstoffe gegen Polio verfügbar. Die Erkrankungszahlen sind seitdem stark rückläufig. Große Gesundheitsorganisationen, allen voran die WHO, arbeiten seit Jahren auf die Ausrottung von Polio hin.[5] Es gibt allerdings immer wieder Rückschläge. So verbreitet sich Polio (Stand Anfang 2020) in Afghanistan und Pakistan. In der Ukraine erkrankten im Jahr 2015 zwei Kinder, obwohl Europa bereits 2002[6] als komplett frei von Polio erklärt worden war. Im September 2022 wurde im US-Bundesstaat New York der Notstand ausgerufen, nachdem das Virus im Abwasser von vier Bezirken sowie in New York City nachgewiesen worden war (siehe unten).
Nachdem in Afrika vier Jahre lang kein neuer Fall von Wild-Poliomyelitis aufgetreten war, erklärte die WHO Afrika am 25. August 2020 für „Wild-Polio-frei“.[7] Unabhängig von Wild-Polioviren zirkulieren hier jedoch vom Lebendimpfstoff abgeleitete Polioviren (cVDPVs), eine Folge un- bzw. unterimmunisierter Populationen mit geringen hygienischen Standards. Daher schätzte die WHO am 1. September 2020 das Risiko der Ausbreitung von cVDPVs in Zentralafrika und im Horn von Afrika als „hoch“ ein.[8] Mehr als ein Dutzend Länder Afrikas, darunter Angola, Kongo, Nigeria und Sambia kämpfen weiterhin gegen diese Erkrankung.[9]
Vorkommen[Bearbeiten | Quelltext bearbeiten]

Überwiegend sind Kinder im Alter von drei bis acht Jahren betroffen, nur gelegentlich erkranken auch Erwachsene. Für diese Viruserkrankung gibt es keine ursächliche Behandlung. Aufgrund der konsequenten Impfung gilt Polio heute in Deutschland offiziell als „ausgerottet“.
Poliomyelitis wurde klinisch erstmals im 18. Jahrhundert von dem englischen Arzt Michael Underwood (1736–1820) beschrieben.[10] Genauer dargestellt wurde die Krankheit vom Schwarzwälder Orthopäden Jakob Heine, der 1840 ein Buch mit dem Titel Beobachtungen über Lähmungszustände der unteren Extremitäten und deren Behandlung herausgab.[11] Was er beschrieb, nannte er in der zweiten Auflage von 1860 Spinale Kinderlähmung. Der schwedische Arzt und Forscher Karl Oskar Medin (1847–1927), der den epidemischen Charakter der Krankheit erkannte, knüpfte an die Erkenntnisse Heines an. Daher rührt die weitere Bezeichnung der Kinderlähmung als Heine-Medin-Krankheit.
Nach heutigen Erkenntnissen existierte Poliomyelitis bis 1880 als endemische Krankheit. Erst ab etwa 1880 trat diese Infektionskrankheit in epidemischer Form auf, die jährlich tausende Menschen betraf. Vor allem Kinder starben daran oder litten dauerhaft an körperlichen Folgeschäden. Ab etwa 1910 traten in Europa und den Vereinigten Staaten regionale Epidemien im Turnus von etwa fünf bis sechs Jahren auf. Zu den bekanntesten Opfern zählt der US-amerikanische Präsident Franklin D. Roosevelt, der die Forschung nach einem Impfstoff während seiner Präsidentschaft wesentlich förderte. Als Fortschritt in der Erforschung eines Impfstoffes gilt die Einführung der Viruskultur durch J. F. Enders im Jahre 1952. Darauf aufbauend entwickelte Jonas Salk 1954 einen inaktivierten (Tot-)Impfstoff. Dieser wirkte jedoch unzureichend. Der von Albert Sabin entwickelte abgeschwächte Lebendimpfstoff ermöglichte ab 1960 eine Poliobekämpfung. Hierdurch sank die Zahl der Poliofälle von jährlich mehreren 100.000 auf etwa 1.000 pro Jahr.[12]
2010 kam es zu einem schweren Ausbruch in Tadschikistan, der auch nach Russland verschleppt wurde. Am 5. Mai 2014 erklärte die Weltgesundheitsorganisation (WHO) Poliomyelitis-Ausbrüche in Kamerun, Pakistan und dem bürgerkriegserschütterten Syrien sowie die von dort erfolgte Verbreitung nach Äquatorialguinea, Afghanistan und in den Irak zu einem „außerordentlichen Ereignis“, das dringend koordinierte Maßnahmen erfordere, um ein weltweites Wiederaufleben der Erkrankung zu verhindern.[13][14]
Anfang September 2015 meldete die WHO zwei Fälle von Polio bei Kindern im Südwesten der Ukraine. Es besteht ein hohes Risiko, dass sich die Krankheit dort verbreitet, da nur 50 % der Kinder gegen Kinderlähmung geimpft sind. Wegen besserer Impfquoten besteht wenig Risiko für die Nachbarländer Rumänien, Polen, Ungarn und die Slowakei.[15] Im August 2019 wurde Nigeria als letzter afrikanischer Staat offiziell als frei von Poliomyelitis erklärt. Weltweit werden aus dem Endemie-Großraum Afghanistan und Pakistan Neuerkrankungen gemeldet. Dort gab es 2018 33 Fälle, zu diesen kamen in Pakistan 2019 (Stand: Anfang Oktober) 72 neue Fälle hinzu.[16] Im Sommer 2022 wurde das Polio-Virus im Abwasser von London und New York City sowie mehreren benachbarten Countys nachgewiesen. New York City rief daher im September den Katastrophenfall aus, um Bemühungen zur raschen Erhöhung der niedrigen Impfquote zu unterstützen.[17][18][19]
Erreger[Bearbeiten | Quelltext bearbeiten]

Der Erreger dieser Erkrankung ist das Poliovirus. Es ist ein unbehülltes Virus mit einzelsträngiger RNA positiver Polarität (ss(+)RNA) von ca. 30 Nanometer Durchmesser, das zur Gattung Enterovirus der Familie Picornaviridae gehört. Es sind drei Serotypen bekannt: Typ 1 („Brunhilde“[4]), der als am stärksten lähmungsverursachend gilt und zur epidemischen Ausbreitung neigt; er wurde nach einer damals infizierten Schimpansin namens Brunhilde benannt. Daneben gibt es noch Typ 2 („Lansing“[4]) sowie Typ III („Leon“[4]), die seit Jahren nicht mehr nachgewiesen wurden und inzwischen von der WHO als ausgerottet erklärt wurden.[20] Zwischen den drei Erregertypen gibt es keine Kreuzimmunität. Das heißt, eine Infektion mit einem der drei Typen schützt nicht vor einer weiteren Infektion mit einem der beiden anderen Typen. Außer dem Menschen werden auch ein paar Menschenaffen befallen; die Übertragung beim Menschen erfolgt durch andere Menschen.
Übertragungswege[Bearbeiten | Quelltext bearbeiten]
Weil das Virus sich im Magen-Darm-Trakt vermehrt, wird es durch die fäkal-orale Route übertragen. Das Risiko einer Infektion ist hoch, wenn die Nahrung mit Viren kontaminiert ist oder wenn die allgemeine Hygiene ungenügend ist. Weil Polioviren in kaltem Wasser lange konserviert werden, kann in Ländern der gemäßigten Klimazone auch das Trinkwasser eine Infektionsquelle sein. Forscher aus Schweden haben das schon in den 1940er Jahren vermutet.[21] Das würde erklären, warum die Stadt New York besonders schwer getroffen wurde. Dort gab es in den Jahren 1931, 1935 und 1944 Epidemien mit 59,1 bzw. 28,5 bzw. 24,6 gemeldeten Fällen pro 100.000 Einwohner. Im Gegensatz dazu wurden im gleichen Zeitraum in London im Mittel nur 2 Fälle pro 100.000 Einwohner. gemeldet.[22] Während in London das Trinkwasser aus Grundwasser gewonnen wurde, kam es in New York aus Stauseen in den Bergen nördlich der Stadt,[23] wo die New Yorker im Sommer oft das Wochenende oder die Ferien verbrachten. Das könnte auch erklären, warum die Epidemien immer im Sommer auftraten.[24]
Epidemiologie[Bearbeiten | Quelltext bearbeiten]
Der Erreger ist außer in den Polargebieten weltweit anzutreffen. Durch eine konsequente Durchführung von Impfmaßnahmen ist das häufige Auftreten der Erkrankung auf Gebiete in Asien zurückgedrängt worden. Seit der Ausrufung des WHO-Eradikationsziels 1988 ist die Zahl der Fälle von damals noch jährlich 350.000 in 125 Ländern weltweit um 99 % gesunken, und nur die drei Länder Afghanistan, Pakistan und Nigeria waren bis dahin nie erregerfrei.[25] In Deutschland erfolgte die letzte Ansteckung mit Polio 1990. Die letzten eingeschleppten Infektionen wurden 1992 registriert. In den USA gab es im Jahr 1979 in den Bundesstaaten Iowa, Wisconsin, Missouri und Pennsylvania einen Ausbruch ausschließlich unter den strenggläubigen Amischen. Ein erneuter Ausbruch wurde im Oktober 2005 ebenfalls nur bei Anhängern dieser Glaubensgemeinschaft in Minnesota gemeldet. In Westeuropa ereignete sich die letzte Polio-Epidemie im Jahr 1992 in den Niederlanden. Dort waren Mitglieder fundamentalistisch-calvinistischer Gemeinden betroffen, die Impfungen aus religiösen Gründen ablehnen.

Das verstärkte Auftreten von Polio nach 2003 in Nigeria – einem Land, das bis vor 2003 als praktisch poliofrei galt – kann eindeutig auf eine in jenem Jahr von Ibrahim Datti Ahmed, Arzt und Präsident des Obersten Scharia-Rats in Nigeria, ausgegebene Fatwa zurückgeführt werden.[26] Das Gutachten Ahmeds behauptete, Polio-Impfungen seien eine „Verschwörung“ seitens der USA und der UN gegen den muslimischen Glauben und würden dazu dienen, die Muslime zu „sterilisieren“. In den folgenden Jahren nahmen die Polio-Fälle in Nigeria daher wieder zu und verbreiteten sich von dort aus in andere Länder. Noch zehn Jahre später wurden im nigerianischen Kano Mitarbeiter des Gesundheitsdienstes, die an Impfprogrammen mitwirkten, durch mutmaßlich der islamistischen Terrorgruppe Boko Haram angehörende Motorradschützen ermordet.[27] In Somalia wurden 2013 bereits 174 Fälle nachgewiesen, 2012 waren es null.[25] 2020 erklärte die Weltgesundheitsorganisation (WHO) den afrikanischen Kontinent als poliofrei.[28]
Die WHO will in den nächsten Jahrzehnten das Poliovirus, ähnlich wie in den 1970er Jahren die Pocken, weltweit ausrotten; der Erreger scheint dazu geeignet, da er sich praktisch nicht verändert und faktisch nur den Menschen als Reservoir hat. Unabdingbar für das Gelingen dieses Vorhabens ist allerdings eine nicht nachlassende Impfbereitschaft weltweit, da das Virus umweltstabil ist und quasi „ausgehungert“ werden muss, so dass es keinen Wirt mehr findet. Eine möglichst hohe weltweite Immunisierungsrate über Jahre ist dafür zwingend notwendig. 2007 gab es weltweit 1310 Fälle von Poliomyelitis durch Wildviren. Im Jahr 2008 war das Virus nur noch in Nigeria, Indien, Pakistan und Afghanistan endemisch.[29][30] Bis Mitte 2015 gelang es, die Neuinfektionen auf zwei Länder zu begrenzen; Neuinfektionen traten bisher nur in Pakistan und Afghanistan auf. Ein Land gilt als „poliofrei“, wenn drei Jahre lang keine Neuinfektionen aufgetreten sind.[31] Von den drei Typen des Polio-Wildvirus ist Typ 2 (WPV2) bereits seit 1999 nicht mehr nachgewiesen. Nach Angabe der GPEI wurde der Wildtyp 3 zuletzt im November 2012 nachgewiesen.[32] 2015 wurde Typ 2 durch die WHO als ausgerottet erklärt. Daher wurde für die weiteren Impfprogramme inzwischen auch ein bivalenter Impfstoff ohne Immunisierung gegen Typ 2 entwickelt. Am Welt-Poliotag am 24. Oktober 2019 erklärte die WHO auch Typ 3 für ausgerottet.[33]
Das Virus wird unter schlechten hygienischen Bedingungen durch kotverschmutzte Hände oder Gegenstände übertragen und über den Verdauungstrakt aufgenommen (fäkal-orale Schmierinfektion oder Kontaktinfektion). Es kommt aber auch zu Übertragungen durch Tröpfcheninfektion.[34] Die Ansteckungsfähigkeit setzt offensichtlich schon wenige Stunden nach der Infektion ein. Im Rachen (Tröpfcheninfektion) hält sie eine, im Kot drei bis sechs Wochen an. Die Inkubationszeit beträgt 7–14 (3–35) Tage.[34][35]
Pathogenese[Bearbeiten | Quelltext bearbeiten]
Das Poliovirus wird meist durch den Mund in den Körper aufgenommen und vermehrt sich anschließend im Darm. Von dort aus befällt es zunächst die lokalen Lymphknoten und verteilt sich nach Vermehrung über die Blutbahn (Virämie). Dabei gelangt es als neurotropes Virus bevorzugt in diejenigen Nervenzellen im Vorderhorn des Rückenmarks (α-Motoneurone), die mit ihren Fortsätzen die quergestreifte Muskulatur erreichen und steuern. Als Reaktion auf die Infektion wandern körpereigene Abwehrzellen (Leukozyten) ins Rückenmark ein, wobei eine Entzündung die Nervenzellen letztlich zerstört. Die Folgen sind mehr oder weniger ausgeprägte, ungleichmäßig verteilte schlaffe Lähmungen, vorwiegend an den Beinen. Der Berührungssinn bleibt dabei erhalten.
Neben dem Befall des Rückenmarks ist bei der paralytischen Verlaufsform fast immer auch das Gehirn selbst mitbetroffen, so dass exakterweise von einer Poliomyeloencephalitis gesprochen werden müsste. Vor allem im Bereich des Kleinhirns, der Brücke und des verlängerten Marks treten regelmäßig Einwanderungen von Entzündungszellen (entzündliche Infiltrate) und Nervenzelluntergänge auf. Diese führen aber nur selten zu eigenen Symptomen. Lediglich die den spinalen Vorderhornzellen analogen Neurone in den Hirnnervenkernen des IX. und X. Hirnnerven sind häufiger betroffen. Durch den Befall dieser Zellen kommt es zur gefürchteten bulbären Form, bei der die Kehlkopffunktion (Sprechen und Atmung) oder das Schlucken beeinträchtigt sein kann. Solche Lähmungen können schon innerhalb weniger Stunden nach Befall des Nervensystems auftreten.
Krankheitsverlauf, Symptome[Bearbeiten | Quelltext bearbeiten]
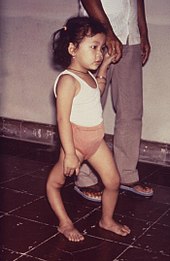
In rund 72 Prozent der Fälle[36] verläuft die Infektion asymptomatisch (ohne Krankheitsanzeichen), so dass auch von keinem Krankheitsverlauf gesprochen werden kann.[35] Stattdessen kommt es – vom Infizierten unbemerkt – zur Bildung von Antikörpern und damit zu einer sogenannten stillen Feiung. Bei 4–8 % der Infizierten gibt es vorübergehende, unspezifische Symptome.
Abortive Poliomyelitis[Bearbeiten | Quelltext bearbeiten]
Nach einer Inkubationszeit von 6–9 Tagen kommt es zu einer etwa dreitägigen Erkrankung mit Fieber, Halsschmerzen, Abgeschlagenheit, oft Durchfall und Erbrechen.[34] Die Viren vermehren sich stark in den Darmepithelzellen, es werden zwischen 106 und 109 infektiöse Viren pro Gramm Stuhl ausgeschieden.[37] Zudem kommt es auch kurz nach Infektion zu einer Vermehrung in den Rachenschleimhautzellen, was eine im Vergleich zur fäkal-oralen schwächere Übertragung durch Tröpfcheninfektion ermöglicht. Solange die Viren ausgeschieden werden, ist man infektiös.[37]
Bei mehr als drei Vierteln[34] der Erkrankten heilt diese abortive Poliomyelitis (abortiv für „abgekürzt, abgeschwächt verlaufend“) folgenlos aus. Die Zellen des Zentralnervensystems (ZNS) werden dabei nicht infiziert.
Infektion mit ZNS-Beteiligung[Bearbeiten | Quelltext bearbeiten]
Bei etwa 5–10 Prozent der symptomatischen Patienten[34] kommt es jedoch zu einer Beteiligung des Zentralnervensystems, bei der die oben geschilderten Symptome das Prodromalstadium (Vorstadium) der Erkrankung darstellen. Nach einer fieber- und beschwerdefreien Phase von etwa einer Woche entwickeln diese Patienten eine nichteitrige Hirnhautentzündung (aseptische Meningitis), bei der Lähmungen (Paralysen) der Muskulatur fehlen (nichtparalytische Poliomyelitis). Diese Form der Hirnhautentzündung ist durch einen erneuten Fieberanstieg auf 39 °C, Kopfschmerzen und Nackensteifigkeit charakterisiert. Wird die Rückenmarksflüssigkeit (das Nervenwasser, der Liquor cerebrospinalis) untersucht, findet der Arzt darin eine Erhöhung der Zellzahl und eine geringe Erhöhung der Eiweißkonzentration.
Nur bei etwa 1 Prozent der Infizierten kommt es zur Entwicklung der paralytischen Poliomyelitis, der schwersten Form des Krankheitsbildes, die als „klassische Kinderlähmung“ gefürchtet wird. Dies kann auch nach einer fieber- und beschwerdefreien Latenzzeit von etwa 2–12 Tagen geschehen, in der sich die Symptome der Meningitis zunächst bessern, es somit zu einem zweiphasigen (biphasischen) Verlauf kommt (der Krankheitsablauf kann in zwei Phasen eingeteilt werden). Charakteristisch für den plötzlichen Beginn der paralytischen Form ist eine „Morgenlähmung“ des noch am Vorabend gesunden Kindes. Die Lähmungen sind schlaff (im Gegensatz zur spastischen Lähmung bei Schädigung der motorischen Hirnrinde oder der Pyramidenbahn), asymmetrisch verteilt, bevorzugen die Muskulatur der Oberschenkel und sind oft mit erheblichen Schmerzen verbunden. Wenn die zugehörigen Segmente des Rückenmarks beteiligt sind, können aber auch die Muskulatur von Rumpf, Zwischenrippenräumen, Harnblase, Mastdarm oder sogar das Zwerchfell betroffen sein. Viel seltener sind die Ursprungsgebiete der Hirnnerven (Hirnnervenkerne) betroffen. Bei dieser bulbären Form kommt es unter hohem Fieber zu Schluckstörungen oder Atem- und Kreislaufregulationsstörungen. Diese ernste Verlaufsform ist mit einer hohen Sterblichkeit belastet. Jede zusätzliche Belastung beispielsweise in Form von körperlicher Anstrengung oder banalen Eingriffen wie beispielsweise Injektionen in einen Muskel oder Mandelentfernung besonders im Anfangsstadium der Erkrankung erhöht das Risiko, dass später Lähmungen auftreten.[34] Für die Gesamtheit der Erkrankten, bei denen Lähmungen auftreten, liegt die Sterblichkeit (Letalität) bei etwa 2–20 %.
Spätkomplikationen[Bearbeiten | Quelltext bearbeiten]
Normalerweise bilden sich die Symptome innerhalb eines Jahres zurück, jedoch können Lähmungen, Durchblutungs- und Hauternährungsstörungen als Dauerschaden zurückbleiben. Auch Gelenkschäden aufgrund der Lähmungen und der veränderten Statik wie Skoliose der Wirbelsäule und Fußdeformitäten stellen bleibende Beeinträchtigungen dar. Ein gebremstes Längenwachstum einzelner betroffener Extremitäten kann das Kind im Wachstum zum Invaliden machen. Nach Entfieberung ist zunächst kein weiteres Fortschreiten der Lähmungen zu erwarten. Teilweise erst Jahre oder Jahrzehnte nach der Infektion tritt aber noch das Post-Poliomyelitis-Syndrom als Spätfolge auf. Dessen Symptome zeigen sich in extremer Müdigkeit, Muskelschmerzen und Muskelschwund in neuen und früher schon betroffenen Muskeln, Atem- und Schluckbeschwerden. Diese Spätkomplikation scheint eher die Regel als die Ausnahme zu sein.[34]
Diagnostik[Bearbeiten | Quelltext bearbeiten]
Klinisch lenkt der doppelgipfelige Fieberverlauf spätestens beim Auftreten der Lähmungen den Verdacht auf das Vorliegen einer Poliomyelitis. Das Virus kann aus dem Stuhl, aus Rachenspülwasser und aus dem Hirnwasser angezüchtet werden. Auch der molekularbiologische Nachweis von Virus-Erbinformation (RNA) mittels der Polymerase-Kettenreaktion (PCR) ist möglich. Bei fehlendem Erregernachweis können im Serum spezifische Antikörper gegen die Polioviren die Diagnose absichern.
Differentialdiagnose[Bearbeiten | Quelltext bearbeiten]
Während der ersten Krankheitsphase muss die Poliomyelitis von anderen fieberhaften Infektionen durch andere Erreger abgegrenzt werden. Symptome einer Meningitis, auch mit auftretenden Lähmungen, können auch durch andere Erreger der Gruppe der Enteroviren wie Coxsackie- und Echoviren sowie die Frühsommer-Meningoenzephalitis verursacht werden. Bei bulbärer Verlaufsform stellt die in unseren Breiten ebenfalls selten gewordene Diphtherie eine wichtige Differenzialdiagnose dar. Das Guillain-Barré-Syndrom ist im Gegensatz zur Poliomyelitis durch symmetrische, von den Füßen immer weiter aufsteigende Lähmungen gekennzeichnet. Fieber und Nackensteife als Zeichen einer Hirnhautentzündung fehlen.
Behandlung[Bearbeiten | Quelltext bearbeiten]
Da keine ursächliche antivirale Therapie existiert, beschränkt sich die Behandlung auf symptomatische Maßnahmen. Dazu gehören Bettruhe mit Sicherstellung einer sorgfältigen Pflege, korrekte Lagerung und physikalische Therapie. Die auftretenden Schmerzen können außer durch Schmerzmittel und entzündungshemmende Mittel auch mit feuchtwarmen Packungen um die betroffenen Partien gelindert werden.[34] Beim geringsten Verdacht auf das Vorliegen der bedrohlichen bulbären Verlaufsform mit Auftreten von Schluck- oder Atemstörungen muss frühzeitig eine intensivmedizinische Überwachung und Behandlung sichergestellt werden. Zur Nachbehandlung gehört neben einer angemessenen Krankengymnastik gegebenenfalls auch die Versorgung mit orthopädischen Hilfsmitteln. Dadurch kann noch bis zu zwei Jahre nach der akuten Erkrankung eine Verbesserung der Beweglichkeit erreicht werden.[34] Eventuell kommen auch kosmetische Operationen wie zum Beispiel eine Wadenplastik infrage.
Orthese als Hilfsmittel zum Gehen[Bearbeiten | Quelltext bearbeiten]

Bei Lähmungen, Längendifferenzen und Deformationen der unteren Extremitäten kann es zu Behinderungen beim Gehen mit Kompensationsmechanismen kommen, die zu einer starken Beeinträchtigung des Gangbildes führen. Hierbei können Orthesen in das Therapiekonzept einbezogen werden.[38] Moderne Materialien und Funktionselemente ermöglichen heute die gezielte Anpassung der Orthese an die Anforderungen, die sich aus dem Gangbild des Patienten ergeben. Standphasensicherungsgelenke sperren das Kniegelenk in den frühen Standphasen und geben das Kniegelenk bei Einleitung der Schwungphase zur Kniebeugung frei. Mit Standphasensicherungsgelenken kann auf diese Weise trotz mechanischer Sicherung gegen ungewollte Kniebeugung ein natürliches Gangbild erreicht werden. Häufig werden in diesen Fällen auch gesperrte Kniegelenke eingesetzt, die zwar eine gute Sicherungsfunktion haben, allerdings die Kniebeugung beim Gehen in der Schwungphase nicht freigeben. Das Kniegelenk bleibt in der Schwungphase mechanisch blockiert. Patienten mit gesperrten Kniegelenken müssen das Bein auch in der Schwungphase in steifer Haltung nach vorne schwingen. Das gelingt nur, wenn der Patient kompensatorische Mechanismen entwickelt, zum Beispiel durch Anhebung des Körperschwerpunktes in der Schwungphase (Duchenne-Hinken) oder durch seitliches Ausschwingen des Orthesenbeins (Zirkumduktion).[39]
Vorbeugung[Bearbeiten | Quelltext bearbeiten]

Impfung mit Lebendimpfstoff (OPV)[Bearbeiten | Quelltext bearbeiten]

Zur Vorbeugung ist eine prophylaktische Impfung möglich und von der STIKO allgemein empfohlen. Im Jahr 1960 (DDR und West-Berlin) bzw. 1962 (Westdeutschland) wurde zunächst die Poliomyelitis-„Schluckimpfung“ (orale Polio-Vakzine, OPV) mit abgeschwächten Erregern (attenuierter Lebendimpfstoff) eingeführt.[37] Bereits 1965, nur wenige Jahre nach Beginn der ersten Impfkampagnen, hatte sich die Zahl der im Bundesgebiet erfassten Erkrankungen auf weniger als 50 Neuerkrankungen reduziert, im Vergleich zu den 4.670 gemeldeten Neuerkrankungen im Jahr 1961 war das ein Rückgang um 99 %.[40] Die letzten beiden einheimischen Erkrankungen durch Polio-Wildviren traten in Deutschland in den Jahren 1986 und 1990 auf, die letzten beiden importierten Fälle wurden 1992 erfasst (aus Indien und Ägypten).[40][37] In Österreich erkrankten zwischen 1946 und 1961 an die 13.000 Kinder an Polio und 1.500 von ihnen starben. Seit 1961 verliefen nur mehr sechs Fälle tödlich, zuletzt 1973 (Stand 2010).[41]
Aufschlussreich ist in diesem Zusammenhang die zeitversetzte Abnahme der Erkrankungen in BRD und DDR nach Einführung der Polio-Impfung 1960 (DDR) oder 1962 (BRD). Die Anzahl der gemeldeten Erkrankungen betrug nach den Meldezahlen des damaligen Bundesseuchengesetzes bzw. des Gesetzes zur Verhütung und Bekämpfung übertragbarer Krankheiten beim Menschen der DDR:[42]
| Jahr | 1957 | 1958 | 1959 | 1960 | 1961 | 1962 | 1963 | 1964 | 1965 | 1966 |
|---|---|---|---|---|---|---|---|---|---|---|
| BRD | 2.402 | 1.750 | 2.114 | 4.198 | 4.673 | 296 | 241 | 54 | 48 | 17 |
| DDR | 1.596 | 958 | 958 | 126 | 4 | 2 | 5 | 0 | 1 | 2 |

Risiken der OPV[Bearbeiten | Quelltext bearbeiten]
Nach Impfung mit den zwar abgeschwächten, doch lebens- und vermehrungsfähigen Viren werden diese einige Zeit lang mit dem Stuhl ausgeschieden.[44] Unter ungünstigen hygienischen Verhältnissen oder engem Körperkontakt können sich ungeimpfte Kontaktpersonen über eine Schmierinfektion bzw. Kontaktinfektion anstecken (Impfpoliomyelitis). Das führt im günstigen Fall zu einer ungeplanten weiteren Durchimpfung der Bevölkerung.[44] Es können aber auch nach mehrmaliger Vermehrung und Passage von Impfviren verschiedene Mutationen zur virulenten Form der Viren erfolgen.[44] Der Erreger wird in solchen Fällen als circulating vaccine-derived poliovirus (zirkulierende, vom Impfstoff abgeleitete Polioviren, cVDPV) bezeichnet.[45] Eine Nummer kennzeichnet dabei, um welchen der drei möglichen, rückmutierten Typen es sich handelt. Damit cVDPVs entstehen können, bedarf es mindestens 12 Monate in einer un- oder unterimmunisierten Population (eine ausreichend immunisierte Bevölkerung wäre gegen cVDPVs oder Polio-Wildviren geschützt). Dies kann dann zu kleinen Ausbrüchen und lokal begrenzten Epidemien führen, wie 2000/01 in der Dominikanischen Republik und auf Haiti,[46] 2019 auf den Philippinen[47] oder 2020 im Sudan.[8] Nach einer Ansteckung mit cVDPVs kann es zu klinischen Symptomen führen – inklusive Lähmungserscheinungen. Diese Symptome kann man dabei nicht von denen unterscheiden, die von Polio-Wildviren ausgelöst werden; dies vermag nur eine Laboranalyse.[48] Bis 2015 wurden über 90 % der untersuchten cVDPVs dem Typ 2 zugeordnet (cVDPV2). Da der Polio-Wildvirus Typ 2 bereits 1999 ausgerottet war, wurde ab April 2016 bei Standardimmunisierungsprogrammen dem ehemals trivalenten OPV-Impfstoff die Typ-2-Komponente entfernt.[44]
Wenn die attenuierten Impfviren spontan zu virulenten Varianten mutieren, kann eine ernste, jedoch extrem seltene Nebenwirkung (ca. 1 pro 2,7 Millionen Dosen des Impfstoffs) auftreten: die sogenannte Vakzin-assoziierte paralytische Poliomyelitis, VAPP, also mit der Impfung verknüpfte Poliofälle.[45][37]
Die Impfung mit Polio-Lebendimpfstoff wird daher vom Robert Koch-Institut nicht mehr empfohlen, sofern das Wild-Virus nicht erneut auftritt.[49] In Deutschland trat die letzte mit dem Impfvirus in Zusammenhang gebrachte Poliomyelitis bei einer Frau mit Antikörpermangelsyndrom[37] im Jahr 2000 auf.[40] Es handelte sich aber nicht um eine klassische VAPP, da die Erkrankte bereits 1998 mit OPV geimpft worden war.
In Deutschland wird seit 1998 routinemäßig ein reines IPV-Schema angewendet. Der Grund für die Abkehr von der OPV war „die Verunsicherung der impfenden Kollegen durch die gerichtliche Behandlung von Impfschadensfällen“.[50] Das individuelle Interesse an einer absolut risikolosen Impfung erhielt damit Vorrang vor dem von der WHO verfolgten Ziel der globalen Ausrottung der Krankheit. Ein Team aus der Schweiz vertritt „die These, dass die alleinige Anwendung der IPV in immer mehr Ländern, die sich das leisten können, das Gelingen der gesamten WHO-Kampagne zur Ausrottung der Poliomyelitis in Frage stellt“.[51]
Impfung mit Totimpfstoff (IPV)[Bearbeiten | Quelltext bearbeiten]
In Europa erfolgen deshalb Impfungen gegen Poliomyelitis seit 1998 mit einem Totimpfstoff (nach Jonas Salk), der nicht geschluckt, sondern gespritzt wird (inaktivierte Polio-Vakzine, IPV). Die geringere Wirksamkeit der IPV gegenüber der OPV spielt keine Rolle, sofern das Wild-Virus nicht erneut vermehrt auftritt. Zudem gelten Wildpoliovirus Typ 2 und Wildpoliovirus Typ 3 als ausgerottet, so dass eine Ansteckung nur noch mit dem Typ 1 sowie den cVDPVs erfolgen könne.[52] Mit IPV geimpfte Personen erwerben allerdings keinen sicheren Schutz vor der Aufnahme von Polio-Wildviren über den Darm etwa aus kontaminiertem Trinkwasser. Sie können sich daher weiter mit diesen Viren infizieren und sie unbemerkt ausscheiden und dadurch als asymptomatische Keimträger an Dritte weiterverbreiten.[53] Das ergab beispielsweise die Untersuchung des Ausbruchs einer Polio-Epidemie in Israel im Jahr 2013, bei der 26 der 28 infizierten Personen Polioimpfungen entsprechend den Empfehlungen erhalten hatten.[54]
Rotary International und Polio[Bearbeiten | Quelltext bearbeiten]

Im Kampf gegen Poliomyelitis fördert Rotary International verschiedene Projekte.[55] 1985 dehnte Rotary International das Programm unter dem Namen PolioPlus weiter aus. PolioPlus wird durchgeführt in Zusammenarbeit mit der Weltgesundheitsorganisation (WHO), dem Kinderhilfswerk der Vereinten Nationen (UNICEF), den Gesundheitsbehörden der USA (CDC) und den nationalen Gesundheitsministerien. Nach jüngsten Schätzungen wird Rotary bis zur endgültigen Ausrottung des Virus ca. 1,2 Milliarden US-Dollar aufgewendet haben.[56] Die Poliokampagne profitierte zuletzt von einer Partnerschaft, die Rotary International mit der Bill & Melinda Gates Foundation eingegangen ist. Die Stiftung spendete allein 355 Mio. US-Dollar.[56] Auch die Gewinne des Rotary nahestehenden Vereins „Deckel drauf“, welcher von 2014 bis 2019 Kunststoffschraubverschlüsse schwerpunktmäßig bei Privatpersonen sammelte und die Einnahmen in die Polioimpfung steckte, wurden durch die Bill & Melinda Gates Foundation verdreifacht.
Isolierung[Bearbeiten | Quelltext bearbeiten]
Patienten, die an Poliomyelitis erkrankt sind oder bei denen eine Ausscheidung von Polioviren vermutet wird, sollten zum Schutz von anderen Patienten und Personal isoliert werden. Das Personal sollte bei der Pflege Schutzkittel und Handschuhe tragen.[34]
Geschichte und geographische Verbreitung[Bearbeiten | Quelltext bearbeiten]




Die endemische Phase der Poliomyelitis[Bearbeiten | Quelltext bearbeiten]
Poliomyelitis ist eine seit vielen Jahrhunderten bekannte Krankheit. Anders als bei Grippe, Pocken und Pest sind jedoch bis gegen Ende des 19. Jahrhunderts keine großen Poliomyelitis-Epidemien bekannt. Die frühesten bekannten Hinweise auf Poliomyelitis sprechen daher von Einzelfällen und nicht von Krankheitsausbrüchen, die zu einer Vielzahl von Kranken führten.
Als ältester Hinweis auf eine Polio-Erkrankung gilt eine ägyptische Steintafel aus der Zeit der 18. Dynastie (15. Jahrhundert v. Chr.) Sie zeigt einen jungen Mann, der wahrscheinlich eine Priesterfunktion innehatte, mit einem deformierten Bein und einer Krücke.
Sowohl Hippokrates als auch Galen haben in ihren Schriften Klumpfuß-Deformationen beschrieben, die an die Krankheitsbilder erinnern, die für an Kinderlähmung Erkrankte charakteristisch sind. Auch sie sprechen jedoch von Einzelfällen. Ähnliches gilt für die Schriften, die aus dem Mittelalter überliefert sind. Eine größere Anzahl von Fällen ist aus dem 17. und 18. Jahrhundert bekannt. Zu den mutmaßlichen Opfern einer Polio-Erkrankung zählt der Schriftsteller Walter Scott, der im Alter von 18 Monaten erkrankte und ab diesem Zeitpunkt lahmte.[57]
Ab etwa der Mitte des 19. Jahrhunderts trat Polio in Westeuropa und in den Vereinigten Staaten in einer solchen Form auf, dass es bei mehreren Erkrankten zu bleibenden Schäden kam. Betroffen waren ein Dorf an der französischen Küste, eine britische Stadt in Nottinghamshire und zwei ländliche Gemeinden im US-amerikanischen Bundesstaat Louisiana und in Schweden. In jedem dieser Orte kam es zu Dutzenden von Fällen mit Folgeschäden. Betroffen waren immer junge Kinder, und die Fälle ereigneten sich immer im Sommer.[58]
Die vermehrten Krankheitsfälle führten dazu, dass Polio etwa zur gleichen Zeit erstmals gegenüber anderen Erkrankungen wissenschaftlich abgegrenzt wurde. 1838 berichtete Jakob von Heine auf der Naturforscherversammlung zu Freiburg von akuten Lähmungen der Beine bei Kindern. Zwei Jahre darauf beschrieb er das Krankheitsbild unter dem Namen Spinale Kinderlähmung in einer Monographie und grenzte es erstmals als eigenständig ab. Andere Autoren bezeichneten sie in der Folge als wesentliche Lähmung oder atrophische Kinderlähmung. Jean Louis Prévost und Edmé Vulpian beschrieben 1865 die pathologisch-anatomischen Veränderungen der Vorderhornzellen. Adolf Kußmaul unterstrich die anatomische Lokalisation der Erkrankung in der grauen Substanz des Rückenmarks und schlug 1874 erstmals den Namen Poliomyelitis acuta anterior vor. Adolf von Strümpell erkannte die Krankheit 1884 als Infektionskrankheit.
Poliomyelitis als Epidemie[Bearbeiten | Quelltext bearbeiten]
Während es sich zuvor meist um Einzelfälle gehandelt hatte, breitete sich die Kinderlähmung erst gegen Ende des 19. Jahrhunderts in bedrohlichem Umfang aus. Als es 1887 im Raum Stockholm zu einer Häufung von Krankheitsfällen kam, wurde die „infantile Paralyse“, wie die Poliomyelitis (acuta anterior) seinerzeit genannt wurde, von dem Kinderarzt Karl Oskar Medin als epidemische Krankheit eingestuft. Die erste wissenschaftlich beschriebene Polio-Epidemie in den Vereinigten Staaten war 1894 die Otter-Valley-Epidemie.[58] Der Landarzt Charles Caverley wertete während dieser Epidemie 123 Fälle aus, von denen knapp 50 Prozent schnell und ohne Folgeschäden wieder gesund wurden. Seine Befunde wiesen aber auch darauf hin, dass Polio wesentlich häufiger auftrat, als man bislang vermutet hatte. Ivar Wickman bestätigte wenige Jahre später mit detaillierten klinischen und epidemiologischen Studien die noch umstrittene Hypothese, dass Polio durch Körperkontakt übertragen wird. Anschauungsmaterial lieferte ihm vor allem die große schwedische Epidemie im Jahr 1905 mit insgesamt 1.031 registrierten Fällen. Am Beispiel des kleinen Kirchspiels Trästena in der heutigen Gemeinde Töreboda zeigte er, dass Personen mit großer Kontaktfläche leichter Opfer der Krankheit wurden. Innerhalb von nur sechs Wochen hatten sich 49 Kinder neu infiziert. Er machte zunächst die Beobachtung, dass sich die Krankheit entlang der Straßen und der Eisenbahnlinie ausbreitete. Nach wochenlangen Feldstudien gelang Wickman der Nachweis, dass die öffentliche Schule des Ortes eine wichtige Rolle bei der Streuung der von ihm so genannten Heine-Medinschen Krankheit spielte.[59] Im Herbst 1908 starb Ferdinand Sauerbruchs erstes Kind, eine Tochter, einige Monate nach ihrer Geburt in Marburg an der zu dieser Zeit in Hessen aufgekommenen Kinderlähmung.[60] Im selben Jahr[61] gelang es Karl Landsteiner und Erwin Popper, Affen mit dem Poliomyelitisvirus zu infizieren, und sie beschrieben ein neurotropes, filtrierbares Virus. Damit war der Beweis für die infektiöse Natur der epidemischen Kinderlähmung und die Virusnatur des Erregers erbracht. 1910 entdeckten Constantin Levaditi und der Mikrobiologe Juste Arnold Netter (1855–1936) Poliomyelitis-Antikörper im Serum[62] und es folgte die Entdeckung, dass Serum von Rekonvaleszenten aus großen Poliomyelitis-Epidemien in Skandinavien und den Vereinigten Staaten das Virus neutralisieren kann (Neutralisationsreaktion). Aber erst 1939 wurde die Differenzierung in drei verschiedenen Serotypen von Charles Armstrong bestätigt.


In Europa und den Vereinigten Staaten wurden regionale Epidemien in einem Turnus von etwa 5–6 Jahren beobachtet, während es in den Intervallen immer wieder zu sporadischen Fällen kam. Einer der ersten größeren Ausbrüche war die Polio-Epidemie, die sich 1916 in den Oststaaten der Vereinigten Staaten ereignete. In ihrer Folge starben mehr als 6.000 Menschen. Größere Ausbrüche gab es in Europa beispielsweise 1932 in Deutschland mit 3.700 Fällen und 1934 in Dänemark mit 4.500 Fällen, wobei jeweils nur die paralytischen Verlaufsformen registriert wurden.[63] Zu den Opfern des Sommers 1921 zählte der junge Franklin D. Roosevelt. Es wird heute zwar nicht ausgeschlossen, dass Franklin D. Roosevelt am Guillain-Barré-Syndrom litt.[64] Er selbst und seine Ärzte gingen jedoch bis zu seinem Lebensende von einer Polio-Erkrankung aus. Roosevelt, der sich sehr für die Bekämpfung der Polio-Erkrankung engagierte, gründete am 3. Januar 1938 die National Foundation for Infantile Paralysis. Ziel der Wohltätigkeitsorganisation, die heute die Bezeichnung March of Dimes trägt, war es, Geld für die Forschung und für die Versorgung von Polio-Opfern zu sammeln.
In Kanada begann die Erfassung der Krankheitsfälle ab 1924, die jährlichen Zahlen schwankten von 113 Fällen (1926) bis zu knapp 4.000 Fällen (1937).[65] Jedoch kann nicht ausgeschlossen werden, dass in dieser Periode auch alle Fälle zugeordnet wurden, die eine Polio-ähnliche Symptomatik aufwiesen. Ab 1949 wurden ausschließlich paralytische Formen der Erkrankung erfasst. In den 1950er Jahren kam es in Kanada zu zwei Epidemien: einer mit Peak um 1953 und einer weiteren, kleineren 1959.[65]
In Asien und Afrika ist bis etwa 1950 über Poliomyelitis nur ganz vereinzelt berichtet worden; die Erkrankten waren in der Regel Angehörige einer weißen Minderheit, die in eigenen Häusern und Wohnvierteln abgesondert von den Einheimischen lebte. Auch in einer Einheit von US-Marines, die 1946 bei Tientsin in China stationiert war, brach eine Polio-Epidemie aus.[66] Diese und andere Indizien lassen vermuten, dass die Poliomyelitis ihren Ursprung in Nordamerika und Europa hatte und von dort über die ganze Welt verbreitet wurde.[67]
Die Nachbehandlung der Krankheit wurde zu Beginn des 20. Jahrhunderts vor allem mit einer Fixierung aller gelähmten Gliedmaßen durchgeführt. Diese Methode wurde ab den 1930er Jahren von der australischen Krankenschwester Elizabeth Kenny grundsätzlich in Frage gestellt; die Autodidaktin erzielte große, aber zu ihrer Zeit höchst umstrittene Erfolge mit Wärmebehandlung und physikalischer Therapie sowie Massagen. Das Kenny-Verfahren wurde trotz anfänglicher Opposition in die medizinische Therapie übernommen und auch bei akuten Fällen angewendet.
Auf dem Gebiet der Behandlung führte die Entwicklung von Maßnahmen für eine künstliche Beatmung, zunächst noch in Form der eisernen Lunge, zu einem Abnehmen der gefürchteten Sterblichkeit der Poliomyelitis. Die großen Polioepidemien der 1950er Jahre zeigten jedoch schnell die praktischen Grenzen der Behandlung mit der eisernen Lunge auf; aufgrund der hohen Anschaffungs- und Betriebskosten dieser Geräte waren die Behandlungskapazitäten der Krankenhäuser begrenzt. Beispielsweise verzeichnete das Blegdamshospital in Kopenhagen im Juli 1952 täglich zwischen 50 und 30 Aufnahmen von Patienten mit Atemlähmung, dem nur eine eiserne Lunge und sechs Geräte zur Kürass-Ventilation zur Behandlung gegenüberstanden.[68] Dem dänischen Anästhesisten Björn Ibsen gelang es, eine alternative Poliobehandlungsmethode zu entwickeln, bei der die Patienten intubiert (bzw. tracheotomiert) und mit einem Beatmungsbeutel langzeitbeatmet wurden. Die Mortalitätsrate am Bledgdamshospital sank daraufhin von 87 % auf 25 %. Die Langzeitbehandlung durch positive pressure ventilation führte zwei Jahre später zur Gründung der weltweit ersten „Intensivstation“ für schwerstkranke Patienten (1953) und gehört zur heutigen Standardbehandlung bei Verdacht auf das Vorliegen der bulbären Verlaufsform.[69] Die ebenso häufigen bleibenden Lähmungen ließen sich aber weiterhin therapeutisch kaum beeinflussen, so dass erst die flächendeckende Einführung der Impfung dazu geführt hat, dass die Poliomyelitis eine historische Erkrankung zu werden beginnt.[70]
1952 ermöglichte die Einführung der Viruskultur in nichtneuralen Zellen durch die Nobelpreisträger John F. Enders, Thomas H. Weller und Frederick C. Robbins nicht nur das Ende der Tierversuche, sondern schließlich auch die Entwicklung eines inaktivierten (Tot-)Impfstoffes (IPV) durch Jonas Salk 1954. In Kanada wurde der Totimpfstoff 1955 eingeführt, zwischen April und Juni jenes Jahres wurden 800.000 Kinder immunisiert.[65] Der IPV war jedoch so schwach wirksam, so dass es in den USA und Kanada in der Folge zu einer Epidemie kam. Im Gegensatz dazu brachte 1960 der von Albert Sabin entwickelte abgeschwächte Lebendimpfstoff (OPV) den Durchbruch. Da die amerikanische Politik jedoch auf den scheinbar leichter zu handhabenden Impfstoff von Salk gesetzt hatte, sah sich Sabin gezwungen, ein großzügiges Angebot der UdSSR anzunehmen, seinen Lebendimpfstoff dort zu entwickeln; klinische Studien wurden dort 1958/1959 von Michail Tschumakow durchgeführt. Da durch diese politische Konstellation auf dem Höhepunkt des Kalten Krieges eine Umsetzung in mit den USA befreundeten Staaten nicht möglich war, übernahm die im neutralen Österreich angesiedelte Pharmafirma Immuno das sowjetische Patent und beauftragte 1957 die Bundesstaatliche Bakteriologische und Serologische Untersuchungsanstalt in Wien mit der Überarbeitung nach westlichen Standards, die bis 1958 unter der Leitung des Wiener Bakteriologen Peter Johann Kraus erfolgreich abgeschlossen wurde.
1958 wurde in den USA ein Denkmal für fünfzehn Polioforscher enthüllt, die Polio Hall of Fame.
Chronologie im Kampf gegen die Poliomyelitis[Bearbeiten | Quelltext bearbeiten]
| Zeit | Ereignis |
|---|---|
| 1400 v. Chr. | Früheste Hinweise auf eine Poliomyelitis |
| 1840 | Erste Beschreibung der Kinderlähmung durch Jakob von Heine |
| 1890 | Erste Ausbruchsbeschreibung durch K. Medin (Schweden) |
| 1908 | Poliovirus wird entdeckt (Landsteiner/Popper) |
| 1916 | Ausbruch in New York (27.000 Gelähmte, 9.000 Tote) |
| 1921 | F. D. Roosevelt erkrankt im Alter von 39 Jahren an Polio |
| 1928 | Erster Einsatz einer Eisernen Lunge |
| 1948 | Poliovirus-Typen 1–3 bestätigt |
| 1952 | Größte Polio-Epidemie in USA (57.628 Fälle) |
| 1952 | Ausbruch in Deutschland (9.500 Gelähmte, 745 Tote) |
| 1955 | Salk-Polio-Totimpfstoff (IPV) |
| 1960 | Sabin-Polio-Lebend-Impfstoff (OPV), Beginn Impfung DDR und West-Berlin |
| 1961 | Beginn Schluckimpfung in USA |
| 1962 | Einführung der Schluckimpfung in der BRD |
| 1962 | Einführung OPV in Kanada |
| 1979 | Rotary-Polio-Engagement |
| 1980 | Randbemerkung: die Welt ist pockenfrei |
| 1985 | Rotary-PolioPlus (bislang mehr als 500 Mio. US$ gespendet) |
| 1988 | Programm der Weltgesundheitsorganisation (WHO) zur Ausrottung der Kinderlähmung (Polioeradikation) |
| 1990 | Letzter Polio-Fall in Deutschland |
| 1994 | WHO-Region Amerika ist poliofrei |
| 1998 | In Deutschland wird nur noch Tot-Impfstoff empfohlen |
| 2000 | WHO-Region West-Pazifik ist poliofrei |
| 2002 | WHO-Region Europa ist poliofrei |
| 2003 | Rückschlag durch erneute Ausbreitung der Polio in West- und Zentralafrika |
| 2006 | Erfolgreiche Eindämmung der Ausbrüche durch umfassende Impfkampagnen |
| 2015 | Polio-Typ 2 gilt als weltweit ausgerottet |
| 2019 | Polio-Typ 3 gilt als weltweit ausgerottet |
| 2020 | WHO-Region Afrika ist Wild-Polio-frei |
Fälle von Polio seit 2006[Bearbeiten | Quelltext bearbeiten]
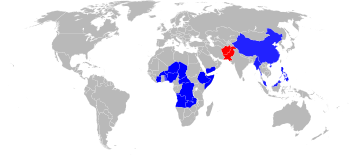
In unregelmäßigen Abständen kommt es weltweit immer wieder zu vereinzelten Ausbrüchen von Polio, die jedoch meist regional beschränkt sind.
- 2006 trat die Poliomyelitis im Norden Nigerias – einem Gebiet, in dem Poliowildviren des Typs 1 und 3 zirkulieren – in einem größeren Ausbruch auf. Die Ursache bestand in zur Impfung verwendeten attenuierten Viren des Typs 2, die durch Mutation wieder virulent wurden und sich aufgrund der lokal unzureichenden Immunität ausbreiten konnten. Laut Forschern könnten die 69 bestätigten Fälle und die Politik der Weltgesundheitsorganisation, die dies erst im September 2007 publizierte, die Ausrottung der Krankheit behindern.[71]
- Aus Tadschikistan wurden 2010 bis zum 29. Juni mehr als 643 Fälle von akuter schlaffer Lähmung gemeldet. Das entspricht etwa 75 Prozent aller weltweit gemeldeten Fälle für 2010. In 334 Fällen konnte das Poliowildvirus Typ 1 nachgewiesen werden, davon verliefen 14 tödlich. Alle Fälle traten bisher im südwestlichen Teil des Landes in der Provinz Chatlon und um die Hauptstadt Duschanbe auf. Als Reaktion auf den Ausbruch wurden mehr als drei Millionen Kinder geimpft und auch in den Nachbarländern Usbekistan und Afghanistan mit Impfkampagnen begonnen. Das ursprünglich aus Uttar Pradesh in Indien stammende Virus wurde auch nach Russland weiterverschleppt, wo bis zum 29. Juni sechs Fälle gemeldet wurden. Damit ist es erstmals seit der Zertifizierung als „poliofrei“ in der WHO-Region Europa wieder zu einer Einschleppung von Poliowildviren gekommen.[72]
- Zum 7. Dezember 2010 meldete die Weltgesundheitsorganisation im Kongo 179 Tote und 476 Gelähmte durch das Poliowildvirus Typ 1 (WPV1). Das Virus stamme vermutlich aus Indien und sei über Angola in die Republik Kongo gekommen. Im Jahr 2000 galt dort Polio als ausgerottet. Der Ausbruch Ende 2010 galt als gefährlich, da auch Ältere infiziert wurden und die Sterblichkeit mit 42 %[73] ungewöhnlich hoch war. Zudem wurden vor allem Männer angesteckt. Die Krankheit war im Kongo im Oktober 2010 ausgebrochen.[74] Nach einer neueren Analyse dieses Polioausbruches stellten Forscher fest, dass das Erbgut der in der Republik Kongo aufgetretenen Virusvariante derart verändert war, dass die nach Impfungen gegen die herkömmlichen Varianten entstandenen Antikörper diese neue Virusvariante nur schwer hatten lahmlegen können.[75]
- 2011 kam es zu mehreren Dutzend Erkrankungen in Pakistan und – infolge von Verschleppungen der Erreger – auch zu mehreren Erkrankungen im Autonomen Gebiet Xinjiang der VR China.[76] China hatte zuvor letztmals 1999 Fälle gemeldet und reagierte mit einer Massenimpfung, die in fünf Impfrunden 43 Millionen Impfdosen umfasste, und nach anderthalb Monaten wurde der letzte Fall gemeldet. China ermittelte Kosten in Höhe von etwa 26 Millionen US-Dollar für die direkte Bekämpfung des Ausbruchs.
- 2012 wurden weltweit weitere 175 Neuerkrankungen registriert, mehr als die Hälfte der Fälle in Nigeria, die übrigen in Afghanistan, Pakistan und Tschad.[77]
- 2013 erlitt die Polio-Eradikation einen Rückschlag durch den wieder erstmaligen Auftritt von Polio in Somalia bei einem 32 Monate alten Mädchen. Seit 2004 war das Land Polio-frei.[78]
- Ende Oktober 2013 waren im Bürgerkriegsland Syrien zehn Proben – von 22 Erkrankten – erstmals polio-positiv (Typ 1). Seit 15 Jahren waren in Syrien keine Polio-Fälle gemeldet worden, aufgrund der mangelhaften Impfversorgung infolge des Bürgerkrieges beginnt sich die Krankheit dort aber wieder auszubreiten.[79][80] Am 11. November identifizierte die Weltgesundheitsorganisation den unter syrischen Flüchtlingen nachgewiesenen Erreger als Abkömmling eines Virenstammes aus Pakistan, der 2012 auch in Proben aus Ägypten, den Palästinensergebieten und Israel nachgewiesen wurde.[81]
- Erst zum zweiten Mal in ihrer Geschichte verhängte die WHO im Mai 2014 konkrete Reisebeschränkungen. Das Poliovirus fand demnach seinen Weg von Pakistan nach Afghanistan und von Syrien in den Irak. Weiterhin sei Polio von Kamerun nach Äquatorialguinea gewandert. Die WHO verlangt, dass sich Bewohner von Kamerun, Syrien und Pakistan, sollten sie ausreisen wollen, zuvor impfen lassen und ein entsprechendes Zertifikat mit sich führen. Die Zahl der dokumentierten Neuansteckungen habe sich von 223 im Jahr 2012 auf 417 im Jahr 2013 erhöht.[82]
- 2014 versicherte das Weiße Haus, die CIA würde keine Impfkampagnen mehr zur Informationsbeschaffung nutzen. Die CIA hatte offenbar im Rahmen der Operation Neptune Spear im Jahr 2011 im Rahmen einer Impfkampagne die unzweifelhafte Identität der Bewohner des Anwesens Osama bin Ladens in Pakistan zu erhalten versucht. Obschon die Ablehnung alles „Westlichen“ in islamistischen Kreisen grundsätzlich viel älter ist, führte das Bekanntwerden zu einem zusätzlichen Rückschlag für die Polio-Impfkampagne.[83]
- 2015 traten in der Oblast Transkarpatien im Südwesten der Ukraine bei einem vierjährigen und einem zehn Monate alten Kind Polioerkrankungen auf. Dies sind die ersten Fälle seit 2010 in Europa. Die Weltgesundheitsorganisation gab an, dass 2014 in der Ukraine nur 49 % aller Kinder gegen Polio geimpft werden konnten, da es an Impfstoff mangelt. Bei Kindern unter einem Jahr beträgt die Impfquote nur 14,1 %.[84]
- 2022 trat in Malawi ein Fall einer vermutlich eingeschleppten Polio-Erkrankung auf.[85]
- Im Frühjahr 2022 traten in Israel mindestens 6 Fälle von Polio-Infektionen auf, darunter eine Person mit Symptomen. In drei Städten wurde das Poliovirus im Abwasser nachgewiesen, was auf unentdeckte Infektionen in diesen Städten hindeutet. Als Reaktion auf den Ausbruch leitete das israelische Gesundheitsministerium eine Impfkampagne ein.[86]
- Im Juli 2022 wurde in Rockland County, New York, eine Poliomyelitis diagnostiziert, wobei die erkrankte Person bereits im Juni Symptome aufgewiesen hatte. Im September 2022 wurde im Bundesstaat New York der Notstand ausgerufen, nachdem das Virus im Abwasser von vier Bezirken (Orange County, Rockland County, Sullivan County und Nassau County) sowie in New York City nachgewiesen wurde.[87] Im Juni 2022 wurde das Virus im Abwasser Londons nachgewiesen.[88]
Meldepflicht[Bearbeiten | Quelltext bearbeiten]
Poliomyelitis ist in Deutschland eine meldepflichtige Krankheit nach § 6 Absatz 1 des Infektionsschutzgesetzes (Meldepflicht bei Verdacht, Erkrankung und Tod). In Österreich ist Kinderlähmung eine anzeigepflichtige Krankheit gemäß § 1 Abs. 1 Epidemiegesetz 1950 (Verdachts-, Erkrankungs- und Todesfälle). In der Schweiz ist Poliomyelitis ebenfalls eine meldepflichtige Krankheit und zwar nach dem Epidemiengesetz (EpG) in Verbindung mit der Epidemienverordnung und (Anhang 1) der Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen[89] (Meldung eines klinischen Verdachts).
Trivia[Bearbeiten | Quelltext bearbeiten]
In der dritten Staffel der Fernsehserie Charité wird auf den zeitlichen Unterschied der Impfkampagnen in Ost- und West-Berlin Bezug genommen. Während in Ost-Berlin schon eine flächendeckende Impfung durchgeführt wurde, war die Impfung in West-Berlin kurz vor dem Bau der Berliner Mauer noch nicht eingeführt.
Das Bayerische Staatsministerium des Innern gab im Jahr 1973 eine Gedenkmedaille mit der Inschrift Geimpft – geschützt heraus, den sogenannten „Impftaler“.[90]
Als letzter Überlebender der Polio-Epidemie 1952 in den USA galt der 2024 im Alter von 78 Jahren verstorbene texanische Anwalt Paul Alexander. Er hatte die Eiserne Lunge bis zu seinem Tod 72 Jahre lang genutzt und damit wohl länger als jeder andere Mensch. Alexander verfasste über sein Leben eine Autobiografie mit dem Titel Three Minutes for A Dog – My Life In an Iron Lung. Zudem war Alexander Vorsitzender des Rotary Clubs in Dallas, der sich vor allem für die Eradikation von Polio einsetzt.
Siehe auch[Bearbeiten | Quelltext bearbeiten]
- Infantile Zerebralparese („Zerebrale Kinderlähmung“)
Literatur[Bearbeiten | Quelltext bearbeiten]
- Deutsche Gesellschaft für Pädiatrische Infektiologie e. V. (DGPI) (Hrsg.): Handbuch Infektionen bei Kindern und Jugendlichen. 4. Auflage. Futuramed, München 2003, ISBN 3-923599-90-0.
- Fabian Feil, Adolf Windorfer, Sabine Diedrich, Eckhard Schreier: Von der Prävention bis zur Ausrottung. WHO-Projekt der Polioeradikation und ihre Überwachung als gesundheitspolitische Herausforderung an die Medizin in Deutschland. In: Deutsches Ärzteblatt. Band 97(40), 2000, ISSN 0012-1207, S. A2598–A2599.
- Adolf Windorfer, Fabian Feil: Der Kampf gegen Poliomyelitis – Ausrottung einer Zivilisationsseuche. In: Bundesgesundheitsblatt. Band 43, 2000, S. 2–6, doi:10.1007/s001030050002.
- David M. Oshinsky: Polio: An American Story. Oxford University Press, USA 2005, ISBN 0-19-530714-3.
- Axel Karenberg: Kinderlähmung. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 750.
- Herwig Kollaritsch, Maria Paulke-Korinek: DFP-Literaturstudium – Poliomyelitis. (PDF) Abgerufen am 5. Januar 2020.
- Karl Wurm, A. M. Walter: Infektionskrankheiten. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 9–223, hier: S. 184–191.
Belletristik:
- Philip Roth: Nemesis. Hanser, München 2011, ISBN 978-3-446-23642-4.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Poliomyelitis – Informationen des Robert Koch-Instituts
- Global Polio Eradication Initiative
- The number of reported paralytic polio cases. In: Our World in Data. Abgerufen am 7. Januar 2020.
- Lars Fischer: Warum Polio wieder auflebt. In: Spektrum.de, 20. Oktober 2022.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Wilhelm Pape, Max Sengebusch (Bearb.): Handwörterbuch der griechischen Sprache. 3. Auflage, 6. Abdruck. Vieweg & Sohn, Braunschweig 1914 (zeno.org [abgerufen am 14. März 2024]).
- ↑ Wilhelm Pape, Max Sengebusch (Bearb.): Handwörterbuch der griechischen Sprache. 3. Auflage, 6. Abdruck. Vieweg & Sohn, Braunschweig 1914 (zeno.org [abgerufen am 14. März 2024]).
- ↑ Weitere Bezeichnungen: epidemische Kinderlähmung, Heine-Medinsche Krankheit und Poliomyelitis acuta.
- ↑ a b c d Thomas Schmitz, Sven Siebert: Klartext: Impfen! – Ein Aufklärungsbuch zum Schutz unserer Gesundheit. 1. Auflage. HarperCollins, 2019, ISBN 978-3-95967-884-1, S. 125.
- ↑ WHO | Global leaders support new six-year plan to deliver a polio-free world by 2018. Abgerufen am 9. Februar 2017.
- ↑ a b Polio-Impfung bei Erwachsenen. Bundeszentrale für gesundheitliche Aufklärung, abgerufen am 8. Januar 2020.
- ↑ Africa Kicks Out Wild Polio. polioeradication.org, abgerufen am 25. August 2020 (englisch).
- ↑ a b Circulating vaccine-derived poliovirus type 2 – Sudan. In: WHO. 1. September 2020, abgerufen am 4. September 2020 (englisch).
- ↑ Maria Cheng: UN says new polio outbreak in Sudan caused by oral vaccine. The Associated Press, abgerufen am 5. September 2020 (englisch).
- ↑ Horst Kremling: Historische Betrachtungen zur präventiven Heilkunde. In: Würzburger medizinhistorische Mitteilungen. Band 24, 2005, S. 222–260; hier: S. 235 f.
- ↑ J. R. Paul: A History of Poliomyelitis. Yale University Press, New Haven CT 1971, ISBN 0-300-01324-8, S. 16–18 (englisch).
- ↑ R. Aylward: Eradicating polio: today’s challenges and tomorrow’s legacy. In: Annals of Tropical Medicine and Parasitology. Band 100, Nr. 5–6, 2006, S. 401–413, doi:10.1179/136485906X97354, PMID 16899145 (englisch).
- ↑ UN agency declares global health emergency to stem potential resurgence of polio. UN News Center, 5. Mai 2014, abgerufen am 8. Mai 2014 (englisch).
- ↑ Donald G. McNeil Jr.: Polio’s Return After Near Eradication Prompts a Global Health Warning. In: The New York Times. 5. Mai 2014, abgerufen am 8. Mai 2014 (englisch).
- ↑ orf.at Erstmals seit 2010 Kinderlähmung in Europa, orf.at, 2. September 2015, abgerufen am 2. September 2015.
- ↑ World Health Organization: Weekly Report. WHO, abgerufen am 20. Oktober 2019.
- ↑ New York ruft Katastrophenfall aus. In: FAZ.net. 10. September 2022, abgerufen am 28. Januar 2024.
- ↑ https://abc7ny.com/polio-nassau-county-wastewater-vaccine/12216079/
- ↑ tagesschau.de, 15. September 2022.
- ↑ Two out of three wild poliovirus strains eradicated: Global eradication of wild poliovirus type 3 declared on World Polio Day. WHO, 24. Oktober 2019, abgerufen am 24. Oktober 2019.
- ↑ C. Kling, G. Olin, J. Fahraeus: Zur Frage der Übertragung der epidemischen Poliomyelitis durch Trinkwasser und der dabei entstandenen Immunität. In: Acta path. et microbiol. Scandinav. Band 54, 1944, S. 499.
- ↑ A. B. Sabin: Paralytic consequences of Poliomyelitis infection in different parts of the world and in different population groups. In: Amer. J. Publ. Health 41 (1951), S. 1215–1230.
- ↑ Artikel Public Works in Encycl. Britannica (1993), Vol. 26.
- ↑ H. Knolle: Übertragung der Poliomyelitis durch Trinkwasser und das Problem der Ausrottung. In: Das Gesundheitswesen 57 (1995), S. 351–354.
- ↑ a b Robert Bublak: Ohne Pauken und Trompeten zur Polio-Ausrottung. ÄrzteZeitung, 28. Oktober 2013, abgerufen am 28. Oktober 2021.
- ↑ Sharia body wants polio vaccination suspended. (Memento vom 29. Oktober 2013 im Internet Archive) In: Vaccination News. 28. Juli 2003.
- ↑ Nigeria polio vaccinators shot dead in Kano. In: BBC News, 8. Februar 2013. Abgerufen am 28. Oktober 2021.
- ↑ Kinderlähmung: WHO erklärt alle afrikanischen Länder für poliofrei. In: Der Spiegel. 25. August 2020, abgerufen am 1. September 2020.
- ↑ Centers for Disease Control and Prevention (CDC). Progress toward interruption of wild poliovirus transmission--worldwide, January 2007–April 2008. In: MMWR Morb Mortal Wkly Rep. 57(18), 9. Mai 2008, S. 489–494. PMID 18463607.
- ↑ Verbreitungskarte 2006 (Memento vom 25. September 2006 im Webarchiv archive.today) für das Poliovirus (polioeradication.org).
- ↑ Polio bleibt internationaler Notfall. tagesspiegel.de, 19. August 2015, abgerufen am 28. Oktober 2021.
- ↑ GPEI, The Virus, Abrufbar unter: polioeradication.org. Version vom 9. Juli 2013.
- ↑ Two out of three wild poliovirus strains eradicated: Global eradication of wild poliovirus type 3 declared on World Polio Day, online 24. Oktober 2019, abgerufen am 24. Oktober 2019.
- ↑ a b c d e f g h i j Deutsche Gesellschaft für Pädiatrische Infektiologie e. V. [DGPI] (Hrsg.): Handbuch Infektionen bei Kindern und Jugendlichen. 4. Auflage. Futuramed, München 2003, ISBN 3-923599-90-0.
- ↑ a b Poliomyelitis: Ratgeber Infektionskrankheiten des RKI. In: Epidemiologisches Bulletin.
- ↑ CDC: What is Polio? 20. Oktober 2021, abgerufen am 30. Januar 2022 (amerikanisches Englisch).
- ↑ a b c d e f Sabine Reiter: Poliomyelitis. In: Heinz Spiess, Ulrich Heininger, Wolfgang Jilg (Hrsg.): Impfkompendium. 8. Auflage. Georg Thieme Verlag, 2015, ISBN 978-3-13-498908-3, S. 254 ff., doi:10.1055/b-0035-127596.
- ↑ Dietrich Hohmann, Ralf Uhlig: Orthopädische Technik. Ferdinand Enke Verlag, Stuttgart 1990, ISBN 3-432-82508-0, S. 69, 518, 639.
- ↑ Frans Nollet, Cornelis Th. Noppe: Orthoses for persons with postpolio syndrome. In: John D. Hsu, John W. Michael, John R. Fisk (Hrsg.): AAOS Atlas of Orthoses and Assistive Devices. 4. Auflage. Mosby Elsevier, Philadelphia 2008, ISBN 978-0-323-03931-4, S. 411–417 (musculoskeletalkey.com).
- ↑ a b c Epidemiologisches Bulletin 7/2002 – Impfpräventable Krankheiten in Deutschland bis zum Jahr 2000. (PDF) RKI, 15. Februar 2002, abgerufen am 7. Januar 2020.
- ↑ 50 Jahre Polio-Schluckimpfung, burgenland.orf.at, 6. April 2011.
- ↑ a b Hans Philipp Pöhn, Gernot Rasch: Statistik meldepflichtiger übertragbarer Krankheiten. Robert Koch-Institut, 1. Januar 1993, S. 71–72 (rki.de [abgerufen am 7. Januar 2020]).
- ↑ Infektionsepidemiologisches Jahrbuch meldepflichtiger Krankheiten für 2018. RKI, 1. März 2019, S. 197–198, abgerufen am 7. Januar 2020.
- ↑ a b c d What is vaccine-derived polio? In: WHO. 19. April 2017, abgerufen am 4. September 2020 (englisch).
- ↑ a b Poliomyelitis und Impfstoffe zu ihrer Ausrottung – Fragen und Antworten. In: WHO. 8. April 2016, abgerufen am 4. September 2020.
- ↑ Ciro de Quadros, Mark Pallansch, Stephen Cochi, David Kilpatrick, M. Steven Oberste: Outbreak of Poliomyelitis in Hispaniola Associated with Circulating Type 1 Vaccine-Derived Poliovirus. In: Science. Band 296, Nr. 5566, 12. April 2002, ISSN 1095-9203, S. 356–359, doi:10.1126/science.1068284, PMID 11896235 (sciencemag.org [abgerufen am 31. Dezember 2018]).
- ↑ Erster Fall von Polio auf Philippinen seit Jahrzehnten, Deutsches Ärzteblatt, online 19. September 2019, Abruf am 22. September 2019.
- ↑ Poliomyelitis. In: WHO. 2. Juni 2020, abgerufen am 4. September 2020 (englisch).
- ↑ Impfempfehlungen. (PDF; 165 kB) Robert Koch-Institut.
- ↑ W. Jilg: Poliomyelitis-Impfung. Die Änderung der Impfstrategie in der Diskussion. In: Immunologie & Impfen, 1998, Nr. 1, S. 2–8.
- ↑ U. Candrian, A. Egli, H. Knolle: Die Perspektive der globalen Ausrottung der Poliomyelitis. In: Gesundheitswesen, Band 66, 2004, S. 1–6. DOI:10.1055/s-2004-812828
- ↑ Epidemiologisches Bulletin. (PDF) RKI, 22. August 2019, S. 330, abgerufen am 13. Oktober 2019.
- ↑ Robert Koch-Institut: Schutzimpfung gegen Poliomyelitis: Häufig gestellte Fragen und Antworten – OPV gegenüber IPV, Stand 8. November 2013. Abgerufen am 20. September 2019.
- ↑ ECDC: Epidemiological update: Polio virus in sewage and human faecal samples in Israel, August 2013, online 20. August 2013. Abgerufen am 20. September 2019.
- ↑ Infos zu PolioPlus auf www.rotary.org/de (Memento vom 14. Mai 2007 im Internet Archive)
- ↑ a b Bill Gates announces new US$255 million grant for ending polio (Memento vom 25. Januar 2009 im Internet Archive) auf rotary.org.
- ↑ David M. Oshinsky: Polio: An American Story. Oxford University Press, USA 2005, ISBN 0-19-530714-3, S. 10.
- ↑ a b David M. Oshinsky: Polio: An American Story. 2005, S. 11.
- ↑ Vgl. M.R. Smallman-Raynor, A.D. Cliff: Poliomyelitis – A World Geography. Emergence to Eradication. Oxford 2006, S. 99.
- ↑ Ferdinand Sauerbruch, Hans Rudolf Berndorff: Das war mein Leben. Kindler & Schiermeyer, Bad Wörishofen 1951; zitiert: Lizenzausgabe für Bertelsmann Lesering, Gütersloh 1956, S. 110.
- ↑ Werner Köhler: Infektionskrankheiten. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 667–671; hier: S. 671.
- ↑ Barbara I. Tshisuaka: Netter, Jules Arnold. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 1030 f.
- ↑ H. Kleinschmidt: Die übertragbare Kinderlähmung. S. Hirzel, Leipzig 1939.
- ↑ Armond S. Goldman, Elisabeth J. Schmalstieg, Charles F. Dreyer, Frank C. Schmalstieg, Daniel A. Goldman: Franklin Delano Roosevelt’s (FDR’s) (1882–1945) 1921 neurological disease revisited; the most likely diagnosis remains Guillain-Barré syndrome. In: Journal of Medical Biography. Band 24, Nr. 4, November 2016, S. 452–459, doi:10.1177/0967772015605738, PMID 26508622.
- ↑ a b c P. V. Varughese et al.: Eradication of indigenous poliomyelitis in Canada: impact of immunization strategies. In: Canadian Journal of Public Health = Revue Canadienne De Sante Publique. Band 80, Nr. 5, September 1989, S. 363–368, PMID 2804867.
- ↑ Albert Sabin: The epidemiology of Poliomyelitis. Problems at home and among the Armed Forces abroad. In: Journal of the American Medical Association. Band 143, 1947, S. 749–756.
- ↑ Albert Sabin: Paralytic Poliomyelitis. Old dogmas and new perspectives. In: Reviews of Infectious Diseases. Band 3, 1981, S. 543–564.
- ↑ H. C. A. Lassen: A Preliminary Report on the 1952 Epidemic of Poliomyelitis in Copenhagen. In: The Lancet. 1953; 1, S. 37–41.
- ↑ Louise Reisner-Sénélar: Der dänische Anästhesist Björn Ibsen – ein Pionier der Langzeitbeatmung über die oberen Luftwege. Dissertation. 2009, abgerufen am 27. Juli 2011.
- ↑ J.-Ch. Sournia, J. Poulet, M. Martiny (Hrsg.): Illustrierte Geschichte der Medizin (= Digitale Bibliothek. Band 53). Directmedia, Berlin 2004.
- ↑ Leslie Roberts: Vaccine-Related Polio Outbreak in Nigeria Raises Concerns. In: Science. Band 317, Nr. 5846, 28. September 2007, S. 1842, doi:10.1126/science.317.5846.1842 (englisch).
- ↑ Polio-Ausbruch in Tadschikistan – aktueller Stand. In: Epidemiologisches Bulletin. Nr. 27. Robert Koch-Institut, Berlin 12. Juli 2010, S. 259.
- ↑ Leslie Roberts: Polio Outbreak Breaks the Rules. In: sciencemag.org. 24. Dezember 2010 (englisch).
- ↑ Florian Rötzer: Explosive und tödliche Polio-Epidemie im Kongo. In: heise.de. 24. Dezember 2010.
- ↑ Jan Felix Drexlera, Gilda Grardb, Alexander N. Lukashev u. a.: Robustness against serum neutralization of a poliovirus type 1 from a lethal epidemic of poliomyelitis in the Republic of Congo in 2010. In: PNAS 2. September 2014, Band 111, Nr. 35, S. 12889–12894, doi:10.1073/pnas.1323502111.
- ↑ In: Nature. Band 477, 2011, S. 135, doi:10.1038/477136a.
- ↑ Polio setback. In: Nature. Band 491, Nr. 7426, 2012, S. 642.
- ↑ Wild poliovirus in somalia. In: WHO.int. 11. Mai 2013 (englisch).
- ↑ Polio in the Syrian Arab Republic. In: WHO.int. 29. Oktober 2013 (englisch).
- ↑ WHO warnt vor globaler Ausbreitung. „Großes Risiko“ für Nachbarländer. In: ORF.at. 29. Oktober 2013.
- ↑ Stephanie Nebehay: Polio virus strain in Syria confirmed as being from Pakistan – WHO. Reuters.com, 11. November 2013; abgerufen am 11. November 2013 (englisch).
- ↑ Dan Bilefsky, Rick Gladstone: Polio Spreading at Alarming Rates, World Health Organization Declares. 5. Mai 2014; abgerufen am 5. Mai 2014.
- ↑ Impfterror aus Angst vor der CIA, Tages-Anzeiger, 20. August 2015.
- ↑ Polio in two Ukrainian children first occurrence of disease in Europe since 2010. In: The Guardian, 2. September 2015, abgerufen am 3. September 2015.
- ↑ Erster Poli-Ausbruch seit Jahren in Afrika. tagesschau.de, 18. Februar 2022, abgerufen am 30. März 2022.
- ↑ Polio: Israel will mit Impfkampagne Ausbruch bekämpfen. In: Der Spiegel. 5. April 2022, ISSN 2195-1349 (spiegel.de [abgerufen am 5. April 2022]).
- ↑ Polio hat in New York den Katastrophennotstand ausgerufen, nachdem weitere Polioviren gefunden wurden. In: allnewspress.com. 10. September 2022, abgerufen am 10. September 2022.
- ↑ New York: Katastrophenalarm wegen Polio. In: tagesschau.de. 10. September 2022, abgerufen am 10. September 2022.
- ↑ Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen vom 1. Dezember 2015. Stand 1. Februar 2020. Bundeskanzlei, abgerufen am 13. März 2020.
- ↑ Maren Biederbick: Impftaler. Deutsches Medizinhistorisches Museum.