Technetium(IV)-chlorid
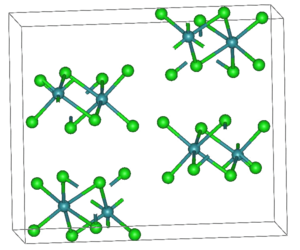
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Tc4+ _ Cl− | ||||||||||
| Kristallsystem | ||||||||||
| Allgemeines | ||||||||||
| Name | Technetium(IV)-chlorid | |||||||||
| Andere Namen |
Technetiumtetrachlorid | |||||||||
| Verhältnisformel | TcCl4 | |||||||||
| Kurzbeschreibung |
roter Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 240,71 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Siedepunkt | ||||||||||
| Gefahren- und Sicherheitshinweise | ||||||||||
 Radioaktiv | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Technetium(IV)-chlorid, meist auch Technetiumtetrachlorid, (TcCl4) ist eine anorganische Verbindung der Elemente Technetium und Chlor.
Darstellung
[Bearbeiten | Quelltext bearbeiten]Technetium(IV)-chlorid kann durch Reaktion von Technetium(VII)-oxid mit Tetrachlorkohlenstoff oder Technetium mit Chlor gewonnen werden.[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Technetium(IV)-chlorid ist ein feuchtigkeitsempfindlicher roter Feststoff.[3] In Wasser löst es sich unter hydrolytischer Zersetzung, in Salzsäure unter Bildung von [TcCl6]2−. Technetium(IV)-chlorid hat eine orthorhombische Kristallstruktur mit der Raumgruppe Pbca (Raumgruppen-Nr. 61) und den Gitterparametern a = 603 pm, b = 1165 pm und c = 1406 pm.[4]
Doppelhexahalogenide können durch Reaktion mit Salzen anorganischer oder organischer Kationen hergestellt werden.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Technetium(IV)-chlorid bei webelements.com .
- ↑ Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Catherine E. Housecroft: Inorganic chemistry. [Hauptbd.] Pearson Education, 2005, ISBN 0-13-039913-2, S. 669 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1600.
- ↑ Anton P. Novikov, Karim A. Zagidullin, Mikhail A. Volkov, Konstantin E. German, Iurii M. Nevolin, Mikhail S. Grigoriev: Influence of the organic cation on the formation of hexahalotechnetates: X-ray, thermal and comparative analyses of non-covalent interactions. In: Dalton Transactions. Band 52, Nr. 46, 28. November 2023, S. 17538–17547, doi:10.1039/D3DT03235C.

