Nirmatrelvir
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
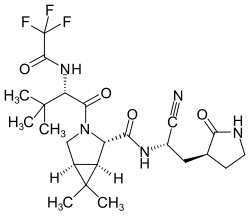
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Nirmatrelvir[1] | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C23H32F3N5O4 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus |
Hemmung der viralen 3C-like-Protease (3CLpro) | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 499,53 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Nirmatrelvir (Entwicklungsname: PF-07321332) ist eine niedermolekulare chemische Verbindung mit antiviraler Wirkung zur Behandlung von COVID-19. Die Substanz wirkt als Proteaseinhibitor und hemmt in vitro das Enzym 3-Chymotrypsin-like Protease (3CLpro), das zu den wichtigsten in Coronaviren vorkommenden Endopeptidasen zählt.
Nirmatrelvir wurde – in Kombination mit Ritonavir, unter dem Handelsnamen Paxlovid – von dem Pharmaunternehmen Pfizer klinisch entwickelt.[3] Am 22. Dezember 2021 erhielt das Kombinationsmedikament in den USA eine Notfallzulassung,[4] am 31. Dezember 2021 in Großbritannien und am 28. Januar 2022 in der EU eine (zunächst bedingte) Zulassung. Es ist das erste zugelassene COVID-19-Mittel, das oral verabreicht werden kann.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Im April 2021 stellte Pfizer das Molekül auf einer Tagung der American Chemical Society vor.[5] Die Struktur enthält als biologisch aktiven Teil („warhead“) eine Nitrilgruppe, die mit dem Cystein-Rest der katalytischen Diade im aktiven Zentrum der 3CLpro reagiert. Die Struktur wurde durch entsprechende chemische Modifikationen für eine orale Verabreichung optimiert.[6] Die orale Gabe als Kapsel oder Tablette ermöglicht die Behandlung von SARS-CoV-2-Infizierten in der Frühphase, wenn die Viruslast besonders hoch ist, aber noch kaum Symptome auftreten und eine Hospitalisierung nicht oder noch nicht erforderlich ist.[7]
In den bisherigen klinischen Studien wird Nirmatrelvir zusammen mit einer geringen Dosis des bereits für die antiretrovirale Therapie zugelassenen HIV-Proteaseinhibitors Ritonavir verabreicht. Die gleichzeitige Verabreichung trägt dazu bei, den Abbau von Nirmatrelvir zu verlangsamen, damit es im Körper für längere Zeit in höheren Konzentrationen aktiv bleiben kann, um so die Bekämpfung des Virus zu unterstützen.[8] Ritonavir ist ein Inhibitor des Cytochrom-P450-Systems in der Leber.
Hintergrund[Bearbeiten | Quelltext bearbeiten]
Die 3-Chymotrypsin-like protease (3CLpro; auch: Nichtstrukturprotein 5, nsp5) ist beteiligt an der posttranslationalen Verarbeitung verschiedener Polypeptide und an der Produktion von 16 Nichtstrukturproteinen des SARS-CoV-2 („Corona-Virus“). Diese Nichtstrukturproteine spielen eine grundlegende Rolle bei der Replikation, Transkription und Virusrekombination während einer Infektion. Die Hemmung von Proteasen blockiert die Freisetzung von Nichtstrukturproteinen und unterdrückt die Reifung und Infektiosität von SARS-CoV-2. Infolgedessen ist 3CLpro als Hauptprotease von SARS-CoV-2 ein attraktives Ziel für die Entwicklung antiviraler Wirkstoffe gegen COVID-19.[9]

Klinische Prüfung[Bearbeiten | Quelltext bearbeiten]
In drei ersten Phase-1-Studien wurde PF-07321332 ausschließlich intravenös verabreicht,[10][11][12] ebenso in einer Phase-3-Studie mit hospitalisierten Patienten (250 mg pro Tag über 5 Tage).[13] Von Juli bis September 2021 wurden drei Phase-3-Studien aufgelegt, in denen nicht hospitalisierte mit SARS-CoV-2 Infizierte PF-07321332 in Kombination mit Ritonavir als orale Gabe erhalten (alle 12 Stunden für fünf Tage):[14][15][16]
- EPIC-HR (Evaluation of Protease Inhibition for COVID-19 in High-Risk Patients),
- EPIC-SR (Evaluation of Protease Inhibition for COVID-19 in Standard-Risk Patients) und
- EPIC-PEP (Evaluation of Protease Inhibition for COVID-19 in Post-Exposure Prophylaxis)
EPIC-HR[Bearbeiten | Quelltext bearbeiten]
Am 5. November 2021 veröffentlichte Pfizer erste Ergebnisse der Studie EPIC-HR. Danach hat Nirmatrelvir/Ritonavir „bei den meisten ambulanten Risikopatienten mit kurzer Symptomdauer einen schweren Verlauf mit Hospitalisierung oder Tod verhindert“. In der Patientengruppe, die innerhalb von drei Tagen nach dem Auftreten von Symptomen PF-07321332 in Kombination mit Ritonavir erhielt, wurde nur bei 3 von 389 Patienten (0,8 %) eine Hospitalisierung notwendig. In der Placebogruppe mit 385 Patienten dagegen waren es 27 Patienten (7,0 %). Während es in der Verumgruppe keinen Todesfall gab, waren es in der Placebogruppe sieben. Bei einem zweiten Studienarm, der die Behandlung mit PF-07321332 bzw. Placebo auf bis zu 5 Tage nach Beginn erster Symptome erweiterte, gab es in der Verumgruppe ebenfalls keinen Todesfall und in der Placebogruppe zehn. Nur 6 von 607 Patienten (1,0 %) in der Verumgruppe mussten hospitalisiert werden, in der Placebogruppe 41 von 612 (6,7 %).[17]
Im Dezember 2021 informierte Pfizer, dass die finalen Daten der EPIC-HR-Studie mit 2246 erwachsenen Hochrisikopatienten die Zwischenergebnisse vom November bestätigten: Demzufolge senkt die fünftägige Gabe von Paxlovid (Nirmatrelvir + Ritonavir) beginnend innerhalb von drei Tagen nach Symptombeginn das Risiko eines Krankenhausaufenthalts im Vergleich zu Placebo um 89 %. Begann die Behandlung innerhalb von fünf Tagen nach Symptombeginn (sekundärer Endpunkt), so war das Risiko eines Krankenhausaufenthalts um 88 % gegenüber Placebo erniedrigt. In beiden Studienarmen trat kein Todesfall in der Verumgruppe auf. In der Patientengruppe im Alter von 65 Jahren oder älter, einer der Bevölkerungsgruppen mit dem höchsten Risiko für Krankenhausaufenthalt oder Tod, betrug die relative Risikoreduktion für eine Krankenhauseinweisung 94 %. In der EPIC-HR-Studie wurde auch eine starke Reduktion der Viruslast, die an 499 Patienten untersucht wurde, festgestellt.[18] Auch gegen die neue Omikron-Variante soll das Medikament wirksam sein.[19]
Nebenwirkungen
Aus den Studien ergaben sich als mögliche Nebenwirkungen von Paxlovid ein beeinträchtigter Geschmackssinn, Durchfall, Bluthochdruck und Muskelschmerzen (Myalgien). Die Anwendung von Paxlovid bei Menschen mit unkontrollierter oder nicht diagnostizierter HIV-1-Infektion kann zu einer HIV-1-Arzneimittelresistenz führen. Ritonavir kann zudem Leberschäden verursachen.[20][21][22]
EPIC-SR[Bearbeiten | Quelltext bearbeiten]
Ferner berichtete Pfizer im Dezember 2021 auch über Zwischenergebnisse aus der laufenden EPIC-SR-Studie, in der Paxlovid an ungeimpften COVID-19-Patienten mit Standardrisiko (d. h. geringem Risiko für Krankenhausaufenthalt oder Tod) sowie an geimpften COVID-19-Patienten mit Risikofaktoren für einen schweren Verlauf untersucht wird. Hier vermochte das Mittel Krankenhauseinweisungen um 70 % (sekundärer Endpunkt) zu reduzieren. Ebenso wie bei der EPIC-HR-Studie wurde eine stärkere Verminderung der Viruslast beobachtet als in der Placebogruppe. Der neue primäre Endpunkt – selbstberichtete, anhaltende Linderung aller Symptome an vier aufeinanderfolgenden Tagen im Vergleich zu Placebo – wurde hingegen nicht erreicht.[18]
Studienlage[Bearbeiten | Quelltext bearbeiten]
Autoren von Cochrane Deutschland befassen sich in einem regelmäßigen systematischen Review mit der Studienlage zu Paxlovid. Alle zwei Monate werden die Recherchen aktualisiert und auf der Plattform Open Science Framework (OSF) öffentlich gemacht. In der in der Cochrane Library veröffentlichte Publikation vom November 2023 berichten sie über die Auswertung von zwei bis zum Stichtag abgeschlossenen Studien.[23]
Rebound-Effekt[Bearbeiten | Quelltext bearbeiten]
Bei einigen Probanden wurde im Anschluss an eine Behandlung, nach einem zunächst negativen Virustest und zwischen zwei und acht Tagen nach der anfänglichen Genesung, in Nasen-Rachen-Abstrichen ein erneuter Anstieg von SARS-CoV-2-RNA oder ein Wiederauftreten von COVID-19-Symptomen beobachtet („Rebound“). Er stand nicht in Zusammenhang mit schweren Verläufen. Rebound-Effekte traten ebenfalls in der Placebo-Gruppe auf.[24][25]
Auch im klinischen Alltag wurde nach der Behandlung mit Paxlovid wiederholt ein Rebound-Effekt beobachtet. Bei den betroffenen Patienten trat einige Tage nach Ende der Behandlung erneut die typische COVID-19-Symptomatik auf und es kam zu einem erneuten Anstieg der Viruslast mit positivem PCR-Test. Unter den Betroffenen waren auch geimpfte und geboosterte Patienten.[26]
Der Verlauf der Erkrankung im Falle eines Rebound ist in der Mehrheit der gemeldeten Fälle mild und bedarf meist keiner weiteren Behandlung, jedoch liegen hierzu nur wenige Daten vor. Deshalb hat die amerikanische Zulassungsbehörde FDA den Hersteller Pfizer mit einer weiteren Studie als Bedingung für die Zulassung von Paxlovid beauflagt. Diese randomisierte kontrollierte Studie[27] wird mit Patienten durchgeführt, die nach einer Behandlung mit Paxlovid einen Rebound erleiden, um insbesondere eine nachfolgende, zweite Gabe von Paxlovid zu untersuchen.[28]
Unerwünschte Wirkungen[Bearbeiten | Quelltext bearbeiten]
Nirmatrelvir ist zwar für die antivirale Wirksamkeit gegen SARS-CoV-2 ausschlaggebend, doch es benötigt einen Wirkverstärker (sogenannten „Booster“), der therapeutisch wirksame Nirmatrelvir-Spiegel über einen ausreichenden Zeitraum ermöglicht. Die gleichzeitige Gabe des aus der HIV-Therapie bekannten CYP3A4-Hemmers Ritonavir hemmt den CYP3A4/5-vermittelten Abbau von Nirmatrelvir. Dadurch bleibt Nirmatrelvir in höheren Konzentrationen und länger im Körper erhalten. Durch die starke Ritonavir-vermittelte CYP3A4-Hemmung kann es unter der Anwendung von Paxlovid zu schweren unerwünschten Wirkungen kommen, wenn gleichzeitig Arzneimittel mit stark CYP3A-abhängiger Clearance angewendet werden.[29] Betroffen sind insbesondere Patienten, die gleichzeitig bestimmte Immunsuppressiva (Tacrolimus, Ciclosporin, Everolimus oder Sirolimus) einnehmen, die eine schmale therapeutische Breite haben. Es sind schwerwiegende und möglicherweise tödliche Nebenwirkungen möglich, worauf der Pharmakovigilanz-Ausschuss (PRAC) der Europäischen Arzneimittelagentur (EMA) und Hersteller Anfang 2024 erneut verwiesen.[30][31]
Zulassung[Bearbeiten | Quelltext bearbeiten]
Die Europäische Arzneimittelagentur (EMA) gab am 16. Dezember 2021, nachdem Pfizer die endgültigen Daten einer klinischen Studie zur Wirksamkeit der Arzneimittelkombination Paxlovid (bestehend aus Nirmatrelvir-Tabletten mit 150 mg und Ritonavir-Tabletten mit 100 mg Wirkstoff[32]) vorgestellt hatte, eine Handreichung zum Einsatz von Paxlovid heraus. Diese sollte den Einsatz des Medikaments erleichtern, bereits bevor es offiziell zugelassen sei.[32] Demzufolge konnten die Tabletten „zur Behandlung von Erwachsenen mit COVID-19 eingesetzt werden, die keinen zusätzlichen Sauerstoff benötigen und bei denen ein erhöhtes Risiko eines schweren Krankheitsverlaufs besteht“.[33][34] Das offizielle Zulassungsverfahren für die EU begann am 10. Januar 2022.[35] Am 28. Januar 2022 erfolgte die (zunächst noch bedingte) Zulassung,[36][37] nachdem die Europäische Arzneimittelagentur am Tag zuvor eine entsprechende Empfehlung[38] ausgesprochen hatte.
In Deutschland kaufte das Bundesministerium für Gesundheit (BMG) Ende 2021 eine Million Packungen Paxlovid.[39] Aus diesen Beständen konnten Hausärzte und Pflegeeinrichtungen von August 2022[40] bis Ende Februar 2024[41] im Bedarfsfall Paxlovid direkt an Patienten abgeben und zu diesem Zweck entsprechende Mengen aus der Apotheke beziehen und vorrätig halten. Seit Mitte Januar 2024 ist das Mittel auch auf dem üblichen Vertriebsweg im Verkehr.[41]
Die U.S. Food and Drug Administration (FDA) erteilte am 22. Dezember 2021 eine Notfallzulassung für die Gabe von Paxlovid an Hochrisikopatienten mit nachgewiesener SARS-CoV-2 Infektion.[42] Die US-Regierung hatte zu dem Zeitpunkt bereits 10 Millionen Dosen des Medikaments bestellt,[19] für die sie 5,3 Milliarden US-Dollar (530 $ pro Packung) bezahlte.[43] Am 6. Juli 2022 erlaubte die FDA die rezeptfreie Abgabe von Paxlovid durch Apotheken unter der Voraussetzung, dass Patienten eine Krankenakte sowie Liste von eingenommenen Medikamenten vorlegen.[44] Im Mai 2023 wurde Paxlovid in den USA regulär zugelassen.[45]
Die britische Arzneimittelbehörde MHRA ließ Paxlovid am 31. Dezember 2021 bedingt zu für den Einsatz bei Menschen über 18 Jahren mit milden bis moderaten Symptomen, die ein Risiko für einen schweren Verlauf haben.[46][47]
In der Schweiz wurde Paxlovid im Juni 2022 befristet für zwei Jahre zur Behandlung erwachsener COVID-19-Patienten zugelassen.[48]
Patentstreit[Bearbeiten | Quelltext bearbeiten]
Im Juni 2022 reichte das US-amerikanische Biotechnologieunternehmen Enanta Pharmaceuticals in Bezug auf Paxlovid eine Patentverletzungsklage gegen Pfizer ein. Laut der beim Bezirksgericht von Massachusetts eingereichten Klage verstoße das in Paxlovid enthaltene Nirmatrelvir gegen das US-Patent Nr. 11.358.953, das die US-Patentbehörde Enanta Anfang des Monats Juni 2022 erteilt hatte. Das Patent beruht auf einem im Juli 2020 eingereichten Antrag, in dem die von Enanta-Wissenschaftlern entwickelten Coronavirus-Proteaseinhibitoren beschrieben wurden.[49][50]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ INN Recommended List 88, World Health Organisation (WHO), 11. Oktober 2022.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ S. Siebenand: Pfizers Paxlovid punktet. In: Pharmazeutische Zeitung. 5. November 2021 (pharmazeutische-zeitung.de).
- ↑ AFP: Anti-Covid-Pille erhält Notfallzulassung in den USA. In: FAZ.net. 22. Dezember 2021, abgerufen am 23. Dezember 2021.
- ↑ B. Halford: Pfizer unveils its oral SARS-CoV-2 inhibitor. In: Chemical & Engineering News. 7. April 2021, abgerufen am 14. Juli 2021.
- ↑ K. Vandyck, J. Deval: Considerations for the discovery and development of 3-chymotrypsin-like cysteine protease inhibitors targeting SARS-CoV-2 infection. In: Current Opinion in Virology. Nr. 49, 2021, S. 36–40, doi:10.1016/j.coviro.2021.04.006.
- ↑ D. Hüttemann: Oraler Proteasehemmer gegen Corona geht in klinische Prüfung. In: www.pharmazeutische-zeitung.de. 3. April 2021.
- ↑ Pfizer’s Novel COVID-19 Oral Antiviral Treatment Candidate Reduced Risk of Hospitalization or Death by 89 % in Interim Analysis of Phase 2/3 EPIC-HR Study. Pressemitteilung von Pfizer vom 5. November 2021.
- ↑ J. C. Ferreira, W. M. Rabeh: Biochemical and biophysical characterization of the main protease, 3-chymotrypsin-like protease (3CLpro) from the novel coronavirus SARS-CoV 2. In: Scientific Reports. Nr. 10. Nature, 2020, doi:10.1038/s41598-020-79357-0.
- ↑ Klinische Studie (Phase I): Single Ascending Dose Study of Intravenous Infusion of PF 07304814 in Healthy Adult Participants bei Clinicaltrials.gov der NIH
- ↑ Klinische Studie (Phase I): First-In-Human Study To Evaluate Safety, Tolerability, And Pharmacokinetics Following Single Ascending And Multiple Ascending Doses of PF-07304814 In Hospitalized Participants With COVID-19. bei Clinicaltrials.gov der NIH
- ↑ Klinische Studie (Phase I): Study to Investigate the Mass Balance, Metabolism, and Excretion of [14C]-PF-07304814 in Healthy Participants bei Clinicaltrials.gov der NIH
- ↑ Klinische Studie (Phase III): ACTIV-3: Therapeutics for Inpatients With COVID-19 bei Clinicaltrials.gov der NIH
- ↑ Klinische Studie (Phase III): A Study of PF-07321332/Ritonavir in Non hospitalized High Risk Adult Participants With COVID-19 bei Clinicaltrials.gov der NIH
- ↑ Klinische Studie (Phase III): A Study of PF-07321332/Ritonavir in Non-hospitalized Low-Risk Adult Participants With COVID-19 bei Clinicaltrials.gov der NIH
- ↑ Klinische Studie (Phase III): A Post-Exposure Prophylaxis Study of PF-07321332/Ritonavir in Adult Household Contacts of an Individual With Symptomatic COVID-19 bei Clinicaltrials.gov der NIH
- ↑ rme: COVID-19: Neuer Proteaseinhibitor verhindert Hospitalisierung oder Tod in Phase-2/3-Studie. In: aerzteblatt.de. 5. November 2021, abgerufen am 6. November 2021.
- ↑ a b Pfizer Announces Additional Phase 2/3 Study Results Confirming Robust Efficacy of Novel COVID-19 Oral Antiviral Treatment Candidate in Reducing Risk of Hospitalization or Death. Pressemitteilung Pfizer, 14. Dezember 2021, abgerufen am 18. Dezember 2021.
- ↑ a b Spencer Kimball: FDA authorizes Pfizer's Covid treatment pill, the first oral antiviral drug cleared during the pandemic. 22. Dezember 2021, abgerufen am 23. Dezember 2021 (englisch).
- ↑ Coronavirus (COVID-19) Update: FDA Authorizes First Oral Antiviral for Treatment of COVID-19 FDA, 22. Dezember 2021.
- ↑ Tagesschau-Beitrag zu Paxlovid, abgerufen am 23. Dezember 2021.
- ↑ E. Mahase: News Covid-19: Pfizer’s paxlovid is 89 % effective in patients at risk of serious illness, company reports. BMJ 2021, doi:10.1136/bmj.n2713
- ↑ Nirmatrelvir in Kombination mit Ritonavir (Paxlovid®) bei COVID-19 | Cochrane Deutschland. In: cochrane.de. 5. Dezember 2023, abgerufen am 22. Februar 2024.
- ↑ COVID-19 rebound after Paxlovid treatment, Centers for Disease Control and Prevention (CDC), 24. Mai 2022.
- ↑ Labelling Paxlovid, Pfizer (Fact Sheet, Stand Juli 2022), abgerufen am 4. August 2022.
- ↑ Zieschang, M.; Dicheva-Radev, S.; Dormann, H.; Graafen, S.: Rebound-Phänomen nach Einnahme von Paxlovid™. In: AkdÄ (Hrsg.): Arzneiverordnung in der Praxis. Band 49, Nr. 4, Dezember 2022, S. 100–202 (dcgma.org [PDF; 2,9 MB; abgerufen am 10. Januar 2023]).
- ↑ Klinische Studie (Phase 2): A Study to Learn About a Repeat 5-Day Treatment With the Study Medicines (Called Nirmatrelvir/Ritonavir) in People 12 Years Old or Older With Return of COVID-19 Symptoms and SARS-CoV-2 Positivity After Finishing Treatment With Nirmatrelvir/Ritonavir bei Clinicaltrials.gov der NIH
- ↑ Emergency Use Authorization (EUA) for Paxlovid. Center for Drug Evaluation and Research Review Memorandum. FDA, 5. August 2022, abgerufen am 10. Januar 2023.
- ↑ S. Siebenand: Paxlovid im Porträt. In: pharmazeutische-zeitung.de. 4. Februar 2022, abgerufen am 10. Februar 2024.
- ↑ Meeting highlights from the Pharmacovigilance Risk Assessment Committee (PRAC) 5-8 February 2024, EMA vom 9. Februar 2024, abgerufen am 9. Februar 2024
- ↑ Pfizer: Rote-Hand-Brief zu Paxlovid (Nirmatrelvir, Ritonavir): Arzneimittelwechselwirkungen mit bestimmten Immunsuppressiva, einschließlich Tacrolimus. BfArM, 21. März 2024, abgerufen am 21. März 2024.
- ↑ a b Covid-19-Mittel von Pfizer: EMA empfiehlt Paxlovid bereits vor der Zulassung, www.pharmazeutische-zeitung.de, 16. Dezember 2021.
- ↑ EMA issues advice on use of Paxlovid (PF-07321332 and ritonavir) for the treatment of COVID-19. 16. Dezember 2021, abgerufen am 18. Dezember 2021.
- ↑ EMA unterstützt Einsatz von Paxlovid für Notfälle. In: aerzteblatt.de. 17. Dezember 2021, abgerufen am 18. Dezember 2021.
- ↑ EMA receives application for conditional marketing authorisation for Paxlovid (PF-07321332 and ritonavir) for treating patients with COVID-19 European Medicines Agency, 10. Januar 2022.
- ↑ Eintrag EU/1/22/1625 im Union Register of medicinal products for human use. 28. Januar 2022.
- ↑ Paxlovid – EPAR, Europäische Arznimiettelagentur (EMA), 28. Januar 2022.
- ↑ Deutscher Ärzteverlag GmbH, Redaktion Deutsches Ärzteblatt: Europäische Arzneimittelagentur empfiehlt Marktzulassung für Paxlovid. 27. Januar 2022, abgerufen am 28. Januar 2022.
- ↑ dpa, Reuters, Ivana Sokola: Covid-Medikament: Bundesregierung kauft eine Million Packungen Paxlovid. In: zeit.de. 28. Dezember 2021, abgerufen am 22. Februar 2024.
- ↑ Paxlovid an Arztpraxen – so geht die Abrechnung, Deutsche Apothekerzeitung, 25. August 2022.
- ↑ a b K. Sucker-Sket: BMG-Bekanntmachung: Letzter Anschub für Paxlovid-Vorräte des Bundes. In: deutsche-apotheker-zeitung.de. 5. Januar 2024, abgerufen am 22. Februar 2024.
- ↑ Frequently Asked Questions on the Emergency Use Authorization for Paxlovid for Treatment of COVID-19. FDA, 22. Dezember 2021, abgerufen am 22. Dezember 2021 (englisch).
- ↑ tagesschau.de, 4. Januar 2022.
- ↑ Office of the Commissioner: Coronavirus (COVID-19) Update: FDA Authorizes Pharmacists to Prescribe Paxlovid with Certain Limitations. 7. Juli 2022, abgerufen am 11. Juli 2022 (englisch).
- ↑ Drug Approval Package: PAXLOVID. In: accessdata.fda.gov. 23. Juni 2023, abgerufen am 22. Februar 2024 (englisch).
- ↑ Oral COVID-19 antiviral, Paxlovid, approved by UK regulator, Pressemitteilung MHRA, 31. Dezember 2021.
- ↑ UK medicines regulator approves second Covid antiviral pill, BBC News, 31. Dezember 2021.
- ↑ Swissmedic lässt Paxlovid für Covid-19-Patientinnen und -Patienten zu. In: Swissmedic. 15. Juni 2022, abgerufen am 18. Oktober 2022.
- ↑ Enanta Pharmaceuticals Files Patent Infringement Suit Against Pfizer, Pressemitteilung Enanta vom 21. Juni 2022, abgerufen am 23. Juni 2022
- ↑ D. Mass. Patent Litigation Update, June 2023. In: finnegan.com. 16. August 2023, abgerufen am 11. Februar 2024 (englisch).