Cyclohepten
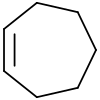
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cyclohepten | ||||||||||||||||||
| Summenformel | C7H12 | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 96,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
0,82 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
114 °C[1] | ||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (50 mg·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,458 (20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||

Cyclohepten ist eine chemische Verbindung aus der Gruppe der ungesättigten cyclischen Kohlenwasserstoffe. Die Verbindung kommt in einer cis- und einer trans-Form vor, wobei die trans-Form instabil ist und sich über −40 °C in die cis-Form umwandelt.[3] Die trans-Form ist der kleinste bekannte Ring mit einer trans-Doppelbindung.[4]
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Cyclohepten kann durch Ringerweiterung unter Nutzung der Demjanow-Umlagerung aus Aminomethylcyclohexan gewonnen werden.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Cyclohepten ist eine farblose bis gelbliche Flüssigkeit, die praktisch unlöslich in Wasser ist.[1] Sie homopolymerisiert nicht, bildet aber mit Ethen Copolymere.[6]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Die Dämpfe von Cyclohepten bilden mit Luft ein explosionsfähiges Gemisch (Flammpunkt ca. 9 °C).[1]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j Eintrag zu Cyclohepten in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. März 2014. (JavaScript erforderlich)
- ↑ Datenblatt Cycloheptene, 97% bei Sigma-Aldrich, abgerufen am 8. März 2014 (PDF).
- ↑ M. E. Squillacote, J. DeFellipis, Q. Shu: How stable is trans-cycloheptene? In: J. Am. Chem. Soc.. 127, 2005, S. 15983–15988, PMID 16277543.
- ↑ Jonathan Clayden, Nick Greeves, Stuart Warren: Organic Chemistry. Oxford University Press, 2012, ISBN 0-19-927029-5, S. 679 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eberhard Breitmaier, Günther Jung: Organische Chemie. 7. vollst. Überarb. u. erw. Auflage 2012: Grundlagen. Georg Thieme Verlag, 2014, ISBN 3-13-159987-1, S. 117 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ JohnJr. Boor: Ziegler-Natta Catalysts Polymerizations. Elsevier, 2012, ISBN 0-323-14341-5, S. 580 (eingeschränkte Vorschau in der Google-Buchsuche).
