Palbociclib
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
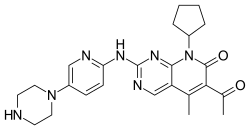
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Palbociclib | |||||||||||||||||||||
| Andere Namen |
6-Acetyl-8-cyclopentyl-5-methyl-2-{[5-(piperazin-1-yl)pyridin-2-yl]amino}pyrido[2,3-d]pyrimidin-7(8H)-on | |||||||||||||||||||||
| Summenformel | C24H29N7O2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
Antineoplastikum | |||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 447,53 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Palbociclib ist ein Arzneistoff zur Behandlung bestimmter Formen des Brustkrebses. Er ist der erste Vertreter der neuen Wirkstoffklasse der Cyclin-abhängige Kinase-Inhibitoren und ist bei peroraler Gabe wirksam.
Wirkungsmechanismus
[Bearbeiten | Quelltext bearbeiten]Palbociclib bewirkt durch die Hemmung der cyclin-abhängigen Kinasen CDK4 und CDK6 eine verringerte Zellproliferation während des Übergangs von Phase G1 zu S des Zellzyklus.
Pharmakokinetik
[Bearbeiten | Quelltext bearbeiten]Nach oraler Gabe treten maximale Plasmakonzentrationen nach 6 bis 12 Stunden auf. Die absolute Bioverfügbarkeit nach oraler Gabe liegt bei durchschnittlich 46 %. Palbociclib wird größtenteils (etwa 85 % in-vitro) an Plasmaproteine gebunden. Die Ausscheidung erfolgt über die Faeces (durchschnittlich 74 %) und über den Urin (durchschnittlich 17 %).[2]
Die mittlere Eliminationshalbwertszeit beträgt circa 28,8 Stunden.
Anwendungsgebiete
[Bearbeiten | Quelltext bearbeiten]Palbociclib ist in den USA[3] (beschleunigtes Break Through Therapy-Verfahren) und der EU[4] als Ibrance für die Behandlung des HR-positiven, HER2-negativen, lokal fortgeschrittenen oder metastasierten Brustkrebses zugelassen. Es muss dabei mit Aromatase-Hemmern oder Fulvestrant, die als Hormontherapie zur Krebsbehandlung verwendet werden, kombiniert werden.[2]
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Als häufigste Nebenwirkungen wurden Infektionen, Verringerung der Anzahl weißer und roter Blutkörperchen sowie der Blutplättchen, Müdigkeit, Appetitverlust, Entzündungen im Mund und an den Lippen, Übelkeit, Erbrechen, Durchfall, Hautausschlag und Haarausfall beobachtet.[2]
Präparatenamen
[Bearbeiten | Quelltext bearbeiten]Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Datenblatt PD 0332991 isethionate ≥98% (HPLC) bei Sigma-Aldrich, abgerufen am 26. November 2016 (PDF).
- ↑ a b c Ibrance: Zusammenfassung der Merkmale des Arzneimittels.
- ↑ Drugs@FDA: FDA Approved Drug Products – Ibrance (Palbociclib)
- ↑ Community register of medicinal products for human use