PTCDA
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
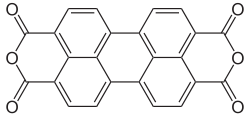
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | PTCDA | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C24H8O6 | |||||||||||||||
| Kurzbeschreibung |
dunkelroter Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 392,32 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
3,4,9,10-Perylentetracarbonsäuredianhydrid (PTCDA) ist ein Pigment, das in der Entwicklung organischer Halbleiter-Bauelemente verwendet und von der Farbmittel-Industrie für kommerzielle Anwendungen hergestellt wird.
Struktur
[Bearbeiten | Quelltext bearbeiten]Es basiert in seiner molekularen Struktur auf dem polycyclischen aromatischen Kohlenwasserstoff Perylen. Von der Kristallstruktur[5] sind zwei Modifikationen bekannt (alpha und beta).[6] Die zweidimensionale Struktur von PTCDA-Schichten, die sich durch Molekularstrahlepitaxie erzeugen lässt, wurde auf verschiedenen Substraten mittels Rastertunnelmikroskopie eingehend untersucht, darunter Graphit, Molybdändisulfid (MoS2)[7], Kupfer[8] und Silber.[9] Neben diesen metallischen Substraten wurde auch die Epitaxie auf verschiedenen Isolatoroberflächen wie NaCl[10][11], KCl[12][13] und KBr[14] untersucht.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
PTCDA ist ein planares Molekül mit einem zweidimensional konjugierten π-Elektronensystem, welches über das gesamte Perylengerüst delokalisiert ist.[15] Das Anhydrid ist ein organischer Halbleiter (n-Leiter)[16] aus der Gruppe der zweidimensional kondensierten Ringsysteme.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Als organischer Halbleiter lässt sich PTCDA z. B. für die Herstellung von organischen Feldeffekttransistoren[17] verwenden. Derivate der PTCDA lassen sich als Schicht in organischen Solarzellen[18] einsetzen oder dienen als Adsorbat zur Sensibilisierung von Titandioxid-Solarzellen für sichtbares Licht.[19] PTCDA eignet sich zudem als Photokatalystor zur Sauerstoff-Produktion aus Wasser mittels Sonnenenergie.[20]
Als Pigment wird PTCDA vor allem in hochwertigen Industrie-Lacken, insbesondere im Automobil-Bereich, eingesetzt.[21]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Datenblatt Perylene-3,4,9,10-tetracarboxylic dianhydride bei Sigma-Aldrich, abgerufen am 5. November 2018 (PDF).
- ↑ a b Eintrag zu Perylen-3,4,9,10-tetracarbonsäuredianhydrid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 28. März 2014.
- ↑ a b c Chun Ming Jiao, Bing Jun Li, Si Li Yi, Qing Xu: Synthesis and Photoelectric Properties of Donor-Acceptor-Donor Molecule Containing Perylene Diimide. In: Asian Journal of Chemistry. 26. Jahrgang, Nr. 23, 2014, S. 8049–8052, doi:10.14233/ajchem.2014.17040 (englisch).
- ↑ a b Eintrag zu Perylen-3,4:9,10-tetracarbonsäuredianhydrid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. November 2022. (JavaScript erforderlich)
- ↑ T. Ogawa et al.: 3,4:9,10-Perylenetetracarboxylic dianhydride (PTCDA) by electron crystallography. In: Acta Cryst. B55, 1999, S. 123–130.
- ↑ H. P. Wagner et al.: Exciton emission in PTCDA films and PTCDA/ Alq3 multilayers. In: Physical Review B 70, 2004, S. 235201.
- ↑ C. Ludwig et al.: STM investigations of PTCDA and PTCDI on graphite and MoS2. A systematic study of epitaxy and STM image contrast. In: Z. Phys. B 93, 1994, S. 365–373.
- ↑ Wagner et al.: The initial growth of PTCDA on Cu(111) studied by STM in J. Phys.: Condens. Matter 19, 2007, S. 056009, doi:10.1088/0953-8984/19/5/056009.
- ↑ Ikonomov et al.: Highly ordered thin films of perylene-3,4,9,10-tetracarboxylic acid dianhydride (PTCDA) on Ag(100) in Surface Science 602, 2008, S. 2061.
- ↑ Burke et al., Phys. Rev. Lett. 100, 186104 (2008).
- ↑ Le Moal et al., Phys. Rev. B 82, 045301 (2010).
- ↑ Dienel et al., Adv. Mater. 20, 959 (2008).
- ↑ Müller et al., Surface Science 605,1090 (2011).
- ↑ Kunstmann et al., Phys. Rev. B 71, 121403 (2005).
- ↑ T. Ertl. In: Alkalimetall-Dotierung von Perylentetracarbonsäuredianhydrid (PTCDA), Dissertation, 2001, S. 15.
- ↑ R. Hudej, G. Bratina: Electronic transport in perylenetetracarboxylic dianhydride: The role of In diffusion. In: J. Vac. Sci. Technol. A 20, Nr. 3, 2002, S. 797–801 (2002).
- ↑ A. Dodabalapur et al.: Molecular Orbital Energy Level En-gineering in Organic Transistors. In: Advanced Materials 8, Nr. 10, 1996, S. 853–855.
- ↑ C. W. Tang: Two-layer organic photovoltaic cell. In: Appl. Phys. Lett. 48, Nr. 2, 1986, S. 183–185.
- ↑ S. Ferrere, B. A. Gregg: New perylenes for dye sensitization of TiO2. In: New J. Chem. 26, 2002, S. 1155–1160.
- ↑ C. A. Linkous, D. K Slattery: Solar photocatalytic hydrogen production from water using a dual bed photosystem (PDF; 86 kB). In: Proceedings of the 2000 Hydrogen Program Annual Review, Volume I.
- ↑ W. Herbst, K. Hunger: Industrielle Organische Pigmente. Herstellung, Eigenschaften, Anwendung. 2. Aufl., Wiley-VCH, Weinheim 1995, ISBN 3-527-28744-2.