Low-Barrier Hydrogen Bond

Ein Low-Barrier Hydrogen Bond (LBHB, deutsch: Wasserstoffbrückenbindung mit geringer Energiebarriere[1]) ist eine spezielle Art der Wasserstoffbrückenbindung. LBHB können auftreten, wenn der pKa-Wert der beiden Heteroatome genau übereinstimmt, wodurch das Wasserstoffatom zwischen ihnen gleichmäßiger genutzt werden kann. Dieser Wasserstoffaustausch führt zur Bildung besonders kurzer, starker Wasserstoffbrückenbindungen.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]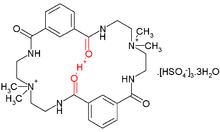
Standard-Wasserstoffbrückenbindungen sind länger und das Proton gehört eindeutig zu einem der Heteroatome. Wenn der pKa-Wert der Heteroatome genau übereinstimmt, wird ein LBHB in einem kürzeren Abstand (≈ 2,55 Å) möglich. Wenn der Abstand weiter abnimmt (< 2,29 Å), wird die Bindung als single-well- oder short-strong hydrogen bond charakterisiert.[4]
Proteine
[Bearbeiten | Quelltext bearbeiten]Low-barrier hydrogen bonds treten in hydrophoben Umgebungen von Proteinen auf.[5] Mehrere Aminosäurereste wirken in einem Ladungsübertragungssystem (auch Protonenrelais genannt) zusammen, um die pKa-Werte der beteiligten Reste zu steuern. LBHB kommen auch auf der Oberfläche von Proteinen vor, sind aber aufgrund ihrer Nähe zu Wasser und den gegensätzlichen Anforderungen starker Salzbrücken an Protein-Protein-Grenzflächen instabil.[5]
Enzymkatalyse
[Bearbeiten | Quelltext bearbeiten]Es wurde vorgeschlagen, dass low-barrier hydrogen bonds für die Enzymkatalyse unter zwei Umständen relevant sind.[6] Erstens könnte ein LBHB in einem Ladungsübertragungssystem innerhalb eines aktiven Zentrums einen katalytischen Rest aktivieren (z. B. zwischen einer Säure und Base innerhalb einer katalytischen Triade). Zweitens könnte sich während der Katalyse die Bildung eines LBHB bilden, um einen Übergangszustand zu stabilisieren (z. B. mit einem Substratübergangszustand in einem Oxyanion-Loch). Diese beiden Mechanismen sind umstritten, wobei theoretische und experimentelle Beweise dahingehend zwiegespalten sind, ob sie überhaupt auftreten.[7][8]
Seit den 2000er-Jahren herrscht allgemeiner Konsens darüber, dass LBHB nicht von Enzymen zur Unterstützung der Katalyse verwendet werden.[8][9] Es wurde jedoch im Jahr 2012 vorgeschlagen, dass LBHB an der Bindung von Phosphaten gegenüber von Arsenaten im Phosphat-Transportsystem (trotz arsenatreicher Umgebung) beteiligt ist.[10] Dieser Befund könnte auf die Möglichkeit hinweisen, dass LBHB in sehr seltenen Fällen eine katalytische Rolle bei der Auswahl der Ionengröße spielen.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Donald Voet, Judith G. Voet, Charlotte W. Pratt: Lehrbuch der Biochemie. 3. Auflage. John Wiley & Sons, Weinheim 2019, ISBN 978-3-527-34286-0, S. 427.
- ↑ G. Gilli, P. Gilli: Towards an unified hydrogen-bond theory. In: Journal of Molecular Structure. Band 552, Nr. 1, 26. September 2000, S. 1–15, doi:10.1016/S0022-2860(00)00454-3.
- ↑ Victor W. Day, Md. Alamgir Hossain, Sung Ok Kang, Douglas Powell, Gerald Lushington, Kristin Bowman-James: Encircled Proton. In: Journal of the American Chemical Society. Band 129, Nr. 28, 2007, S. 8692, doi:10.1021/ja0724745.
- ↑ B. Schiøtt, B. B. Iversen, G. K. Madsen, F. K. Larsen, T. C. Bruice: On the electronic nature of low-barrier hydrogen bonds in enzymatic reactions. In: Proceedings of the National Academy of Sciences. Band 95, Nummer 22, Oktober 1998, S. 12799–12802, doi:10.1073/pnas.95.22.12799, PMID 9788994, PMC 23598 (freier Volltext).
- ↑ a b H. Ishikita, K. Saito: Proton transfer reactions and hydrogen-bond networks in protein environments. In: Journal of the Royal Society, Interface. Band 11, Nr. 91, Februar 2014, S. 20130518, doi:10.1098/rsif.2013.0518, PMID 24284891, PMC 3869154 (freier Volltext) (Review).
- ↑ W. W. Cleland, P. A. Frey, J. A. Gerlt: The low barrier hydrogen bond in enzymatic catalysis. In: Journal of Biological Chemistry. Band 273, Nr. 40, Oktober 1998, S. 25529–25532, doi:10.1074/jbc.273.40.25529, PMID 9748211 (Review).
- ↑ E. L. Ash, J. L. Sudmeier, E. C. De Fabo, W. W. Bachovchin: A low-barrier hydrogen bond in the catalytic triad of serine proteases? Theory versus experiment. In: Science. Band 278, Nr. 5340, November 1997, S. 1128–1132, doi:10.1126/science.278.5340.1128, PMID 9353195.
- ↑ a b C. N. Schutz, A. Warshel: The low barrier hydrogen bond (LBHB) proposal revisited: the case of the Asp. His pair in serine proteases. In: Proteins. Band 55, Nr. 3, Mai 2004, S. 711–723, doi:10.1002/prot.20096, PMID 15103633.
- ↑ A. Warshel, P. K. Sharma, M. Kato, Y. Xiang, H. Liu, M. H. Olsson: Electrostatic basis for enzyme catalysis. In: Chemical Reviews. Band 106, Nr. 8, August 2006, S. 3210–3235, doi:10.1021/cr0503106, PMID 16895325 (Review).
- ↑ M. Elias, A. Wellner, K. Goldin-Azulay, E. Chabriere, J. A. Vorholt, T. J. Erb, D. S. Tawfik: The molecular basis of phosphate discrimination in arsenate-rich environments. In: Nature. Band 491, Nr. 7422, November 2012, S. 134–137, doi:10.1038/nature11517, PMID 23034649.