„Salamander-Alkaloide“ – Versionsunterschied
| [gesichtete Version] | [ungesichtete Version] |
Jü (Diskussion | Beiträge) K + Photo |
→Vertreter: Die Anzahl der bekannten Salamander-Alkaloide wurde nach neusten Forschungsergebnissen aktualisiert. Quelle: https://pubs.acs.org/doi/10.1021/acs.jnatprod.9b00065 |
||
| Zeile 1: | Zeile 1: | ||
[[Datei:Salamandra salamandra MHNT 1.jpg|mini|Feuersalamander (''Salamandra salamandra'')]] |
[[Datei:Salamandra salamandra MHNT 1.jpg|mini|Feuersalamander (''Salamandra salamandra'')]] |
||
Die '''Salamander-Alkaloide''' sind in der Natur vorkommende [[chemische Verbindung]]en aus der Gruppe der [[Alkaloide]]. Sie werden von Salamandern, wie dem [[Feuersalamander]] (''Salamandra salamandra'') oder dem [[Alpensalamander]] (''Salamandra atra''), als Abwehrstoffe gegen [[Bakterien]] und [[Pilze]] aus [[Hautdrüse]]n [[Sekretion|abgesondert]]. |
Die '''Salamander-Alkaloide''' sind in der Natur vorkommende [[chemische Verbindung]]en aus der Gruppe der [[Alkaloide]]. Sie werden von Salamandern, wie dem [[Feuersalamander]] (''Salamandra salamandra'') oder dem [[Alpensalamander]] (''Salamandra atra''), als Abwehrstoffe gegen Prädaturen, [[Bakterien]] und [[Pilze]] aus [[Hautdrüse]]n [[Sekretion|abgesondert]]<ref>{{Literatur |Autor=Tim Lüddecke, Stefan Schulz, Sebastian Steinfartz, Miguel Vences |Titel=A salamander’s toxic arsenal: review of skin poison diversity and function in true salamanders, genus Salamandra |Sammelwerk=The Science of Nature |Band=105 |Nummer=9-10 |Datum=2018-10 |ISSN=0028-1042 |DOI=10.1007/s00114-018-1579-4 |Seiten=56 |Online=http://link.springer.com/10.1007/s00114-018-1579-4 |Abruf=2020-11-26}}</ref>. |
||
== Vertreter == |
== Vertreter == |
||
Die Salamander-Alkaloide leiten sich strukturell vom 3-Aza-''A''-homo-5''β''-androstan ab, als sauerstofffreier Grundkörper wird [[Neosaman]] (C<sub>10</sub>H<sub>33</sub>N)<ref name="Schoepf" /> angegeben. Zu der Gruppe, die |
Die Salamander-Alkaloide leiten sich strukturell vom 3-Aza-''A''-homo-5''β''-androstan ab, als sauerstofffreier Grundkörper wird [[Neosaman]] (C<sub>10</sub>H<sub>33</sub>N)<ref name="Schoepf" /> angegeben. Zu der Gruppe, die derzeit elf Vertreter umfasst<ref>{{Literatur |Autor=Janosch Knepper, Tim Lüddecke, Kathleen Preißler, Miguel Vences, Stefan Schulz |Titel=Isolation and Identification of Alkaloids from Poisons of Fire Salamanders ( Salamandra salamandra ) |Sammelwerk=Journal of Natural Products |Band=82 |Nummer=5 |Datum=2019-05-24 |ISSN=0163-3864 |DOI=10.1021/acs.jnatprod.9b00065 |Seiten=1319–1324 |Online=https://pubs.acs.org/doi/10.1021/acs.jnatprod.9b00065 |Abruf=2020-11-26}}</ref>, gehören das [[Samandarin]] (C<sub>19</sub>H<sub>31</sub>NO<sub>2</sub>), dessen acetyliertes Analogon [[16-O-Acetylsamandarin|16-''O''-Acetylsamandarin]] und die oxidierte Verbindung [[Samandaron]] (C<sub>19</sub>H<sub>29</sub>NO<sub>2</sub><ref name="Schoepf">C. Schöpf, O. W. Möller: [https://www.researchgate.net/publication/230371130_Uber_Samandarin_und_verwandte_Alkaloide_VI_Cycloneosamandion_ein_neues_Nebenalkaloid_aus_dem_Feuersalamander_Salamandra_maculosa_Laur ''Über Samandarin und verwandte Alkaloide, VI. Cycloneosamandion, ein neues Nebenalkaloid aus dem Feuersalamander (Salamandra maculosa Laur.)'']. European Journal of Organic Chemistry 1960, 633(1):127-156, {{doi|10.1002/jlac.19606330116}}</ref>, 16-Dehydrosamandarin). Weiterhin werden |
||
[[Samanin]] (ohne die 1''α'',4''α''-Epoxy-Brücke), |
[[Samanin]] (ohne die 1''α'',4''α''-Epoxy-Brücke), |
||
[[Samandion]] (C<sub>19</sub>H<sub>29</sub>NO<sub>2</sub>)<ref name="Schoepf" />, |
[[Samandion]] (C<sub>19</sub>H<sub>29</sub>NO<sub>2</sub>)<ref name="Schoepf" />, |
||
| Zeile 18: | Zeile 18: | ||
== Biosynthese == |
== Biosynthese == |
||
Die [[Biogenese|biogenetische]] Ausgangssubstanz für die Entstehung des [[Androstan]]-Systems ist das [[Cholesterol]], als Stickstoffquelle des N-Atoms dient [[Glutamin]]. |
Die [[Biogenese|biogenetische]] Ausgangssubstanz für die Entstehung des [[Androstan]]-Systems ist das [[Cholesterol]], als Stickstoffquelle des N-Atoms dient [[Glutamin]]. Die Biosynthese der Salamander-Alkaloide setzt im [[Feuersalamander]] im Verlauf der [[Metamorphose (Zoologie)|Metamorphose]] ein<ref>{{Literatur |Autor=Eugenia Sanchez, Eliane Küpfer, Daniel J. Goedbloed, Arne W. Nolte, Tim Lüddecke |Titel=Morphological and transcriptomic analyses reveal three discrete primary stages of postembryonic development in the common fire salamander, Salamandra salamandra |Sammelwerk=Journal of Experimental Zoology Part B: Molecular and Developmental Evolution |Band=330 |Nummer=2 |Datum=2018-03 |DOI=10.1002/jez.b.22792 |Seiten=96–108 |Online=http://doi.wiley.com/10.1002/jez.b.22792 |Abruf=2020-11-26}}</ref>. |
||
== Wirkung == |
== Wirkung == |
||
| Zeile 27: | Zeile 27: | ||
* Spektrum Online Lexikon der Biochemie: [http://www.spektrum.de/lexikon/biochemie/salamander-alkaloide/5511 Salamander-Alkaloide] |
* Spektrum Online Lexikon der Biochemie: [http://www.spektrum.de/lexikon/biochemie/salamander-alkaloide/5511 Salamander-Alkaloide] |
||
* C. Schöpf, K. Koch: ''Über Samandaron und Samandaridin, Nebenalkaloide im Gift des Feuer- und Alpensalamanders''. In: Justus Liebigs Annalen der Chemie. 1942, 552 (1): 37–61, {{doi|10.1002/jlac.19425520103}} |
* C. Schöpf, K. Koch: ''Über Samandaron und Samandaridin, Nebenalkaloide im Gift des Feuer- und Alpensalamanders''. In: Justus Liebigs Annalen der Chemie. 1942, 552 (1): 37–61, {{doi|10.1002/jlac.19425520103}} |
||
*T. Lüddecke: Über das Hautgift beim Feuersalamander. Feldherpetologisches Magazin. 2019, 11: 9-16. |
|||
== Einzelnachweise == |
== Einzelnachweise == |
||
Version vom 26. November 2020, 21:23 Uhr

Die Salamander-Alkaloide sind in der Natur vorkommende chemische Verbindungen aus der Gruppe der Alkaloide. Sie werden von Salamandern, wie dem Feuersalamander (Salamandra salamandra) oder dem Alpensalamander (Salamandra atra), als Abwehrstoffe gegen Prädaturen, Bakterien und Pilze aus Hautdrüsen abgesondert[1].
Vertreter
Die Salamander-Alkaloide leiten sich strukturell vom 3-Aza-A-homo-5β-androstan ab, als sauerstofffreier Grundkörper wird Neosaman (C10H33N)[2] angegeben. Zu der Gruppe, die derzeit elf Vertreter umfasst[3], gehören das Samandarin (C19H31NO2), dessen acetyliertes Analogon 16-O-Acetylsamandarin und die oxidierte Verbindung Samandaron (C19H29NO2[2], 16-Dehydrosamandarin). Weiterhin werden Samanin (ohne die 1α,4α-Epoxy-Brücke), Samandion (C19H29NO2)[2], Cycloneosamandion (C19H29NO2)[2], Samandaridin (C21H31NO3) und Samanderon (C22H31NO2)[4][5] zu den Salamander-Alkaloiden gezählt.
-
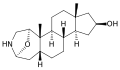
Samandarin
-
Samandaridin
Biosynthese
Die biogenetische Ausgangssubstanz für die Entstehung des Androstan-Systems ist das Cholesterol, als Stickstoffquelle des N-Atoms dient Glutamin. Die Biosynthese der Salamander-Alkaloide setzt im Feuersalamander im Verlauf der Metamorphose ein[6].
Wirkung
Samandarin zeigt beim Menschen atemhemmende Wirkung, führt zu Bluthochdruck, Herzrhythmusstörungen und Hämolyse. Es ist als Lokalanästhetikum stark wirksam, jedoch für medizinische Anwendungen aufgrund der hohen Toxizität ungeeignet.
Literatur
- Eintrag zu Salamander-Alkaloide. In: Römpp Online. Georg Thieme Verlag
- Spektrum Online Lexikon der Biochemie: Salamander-Alkaloide
- C. Schöpf, K. Koch: Über Samandaron und Samandaridin, Nebenalkaloide im Gift des Feuer- und Alpensalamanders. In: Justus Liebigs Annalen der Chemie. 1942, 552 (1): 37–61, doi:10.1002/jlac.19425520103
- T. Lüddecke: Über das Hautgift beim Feuersalamander. Feldherpetologisches Magazin. 2019, 11: 9-16.
Einzelnachweise
- ↑ Tim Lüddecke, Stefan Schulz, Sebastian Steinfartz, Miguel Vences: A salamander’s toxic arsenal: review of skin poison diversity and function in true salamanders, genus Salamandra. In: The Science of Nature. Band 105, Nr. 9-10, Oktober 2018, ISSN 0028-1042, S. 56, doi:10.1007/s00114-018-1579-4 (springer.com [abgerufen am 26. November 2020]).
- ↑ a b c d C. Schöpf, O. W. Möller: Über Samandarin und verwandte Alkaloide, VI. Cycloneosamandion, ein neues Nebenalkaloid aus dem Feuersalamander (Salamandra maculosa Laur.). European Journal of Organic Chemistry 1960, 633(1):127-156, doi:10.1002/jlac.19606330116
- ↑ Janosch Knepper, Tim Lüddecke, Kathleen Preißler, Miguel Vences, Stefan Schulz: Isolation and Identification of Alkaloids from Poisons of Fire Salamanders ( Salamandra salamandra ). In: Journal of Natural Products. Band 82, Nr. 5, 24. Mai 2019, ISSN 0163-3864, S. 1319–1324, doi:10.1021/acs.jnatprod.9b00065 (acs.org [abgerufen am 26. November 2020]).
- ↑ Lou Feierabend: Zu dumm für Verkehr, zu klug für den Osten. In: Welt Online, 6. Juni 2007, abgerufen am 29. Dezember 2016.
- ↑ Robert Lücke: Von Regenmollis und Feuermolchen. In: Naturgucker-Magazin, abgerufen am 29. Dezember 2016.
- ↑ Eugenia Sanchez, Eliane Küpfer, Daniel J. Goedbloed, Arne W. Nolte, Tim Lüddecke: Morphological and transcriptomic analyses reveal three discrete primary stages of postembryonic development in the common fire salamander, Salamandra salamandra. In: Journal of Experimental Zoology Part B: Molecular and Developmental Evolution. Band 330, Nr. 2, März 2018, S. 96–108, doi:10.1002/jez.b.22792 (wiley.com [abgerufen am 26. November 2020]).