Ameisensäure-n-butylester
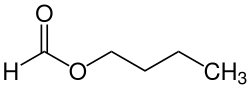
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Ameisensäure-n-butylester | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C5H10O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit alkoholartigem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 102,13 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[2] | ||||||||||||||||||
| Dichte |
0,92 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
106 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Brechungsindex |
1,389 (20 °C)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Ameisensäure-n-butylester ist eine chemische Verbindung aus der Gruppe der Carbonsäureester.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Ameisensäure-n-butylester wurde in frischen Äpfeln, Erdbeeren, Moltebeeren, Sherry und Parmesan nachgewiesen.[3]
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Ameisensäure-n-butylester kann durch azeotrope Destillation von Ameisensäure und n-Butylalkohol mit Isopropylformiat oder durch Kochen von n-Butylalkohol und Formamid in Gegenwart von Zinkchlorid, Zinksulfat oder Quecksilber(II)-chlorid gewonnen werden.[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ameisensäure-n-butylester ist eine leicht entzündbare, leicht flüchtige, farblose Flüssigkeit mit alkoholartigem Geruch, die in Wasser hydrolysiert.[2] In geringerer Konzentration besitzt die Verbindung einen fruchtigen, pflaumenartigen Geruch und einen entsprechenden Geschmack.[3]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Ameisensäure-n-butylester wird als Aromastoff verwendet.[6] Die Verbindung wird auch als möglicher Biokraftstoff untersucht.[7] Sie wird auch selten als Lösungsmittel für Fette, Öle, Cellulosenitrat, einige Celluloseether und Celluloseester, außerdem für viele natürliche und synthetische Bindemittel verwendet.[8]
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Die Dämpfe von Ameisensäure-n-butylester können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 18 °C, Zündtemperatur 265 °C) bilden.[2]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu BUTYL FORMATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 19. September 2021.
- ↑ a b c d e f g h i j k Eintrag zu Ameisensäure-n-butylester in der GESTIS-Stoffdatenbank des IFA, abgerufen am 11. Dezember 2018. (JavaScript erforderlich)
- ↑ a b c d George A. Burdock: Fenaroli's Handbook of Flavor Ingredients. CRC Press, 2016, ISBN 978-1-4200-9086-4, S. 205 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt Butyl formate, ≥97%, FG bei Sigma-Aldrich, abgerufen am 11. Dezember 2018 (PDF).
- ↑ Eintrag zu Butylformiat im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 30. Dezember 2018. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ EU: DURCHFÜHRUNGSVERORDNUNG (EU) Nr. 872/2012 DER KOMMISSION vom 1. Oktober 2012 zur Festlegung der Liste der Aromastoffe gemäß der Verordnung (EG) Nr. 2232/96 des Europäischen Parlaments und des Rates, zur Aufnahme dieser Liste in Anhang I der Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates sowie zur Aufhebung der Verordnung (EG) Nr. 1565/2000 der Kommission und der Entscheidung 1999/217/EG der Kommission, abgerufen am 11. Dezember 2018
- ↑ Stijn Vranckx, Joachim Beeckmann u. a.: An experimental and kinetic modelling study of n-butyl formate combustion. In: Combustion and Flame. 160, 2013, S. 2680, doi:10.1016/j.combustflame.2013.06.012.
- ↑ Eintrag zu Butylformiat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 11. Dezember 2018.

