Hell-Volhard-Zelinsky-Reaktion
Die Hell-Volhard-Zelinsky-Reaktion oder auch Zelinsky-Reaktion ist eine Namensreaktion in der organischen Chemie. Bei dieser nach Carl Magnus von Hell (1849–1926) (Veröffentlichung 1881),[1] Jacob Volhard und Nikolaj Dimitrievic Zelinskij (Erweiterung der Reaktion 1887) benannten Reaktion wird ein Wasserstoffatom am α-Kohlenstoffatom einer Carbonsäure durch ein Halogen (zumeist Brom) ersetzt.[2][3][4]
Übersichtsreaktion
[Bearbeiten | Quelltext bearbeiten]Dabei wird die Carbonsäure mit einem Halogen und einer katalytischen Menge eines Phosphorhalogenids versetzt. Es entsteht eine α-Halogencarbonsäure. Wenn man z. B. Brom und katalytische Mengen PBr3 einsetzt, erhält man eine α-Bromcarbonsäure (2-Bromcarbonsäure):[5]
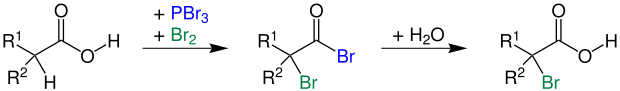
R1 = Alkylgruppe; R2 = Wasserstoff, Alkylgruppe[1]
Mechanismus
[Bearbeiten | Quelltext bearbeiten]Der Mechanismus wird hier anhand der Reaktion einer Carbonsäure mit Phosphor(III)-bromid und Brom veranschaulicht:[6]
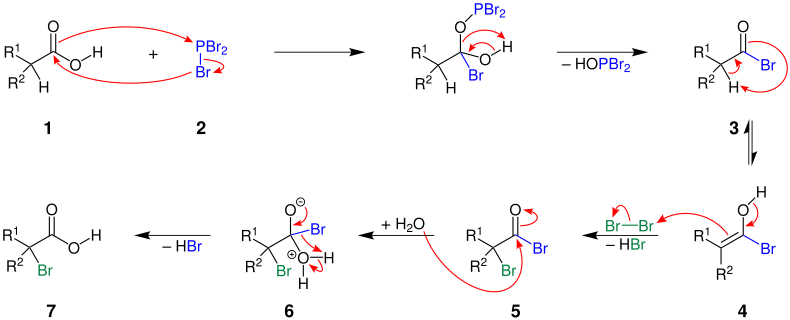
R1 = Alkylgruppe; R2 = Wasserstoff, Alkylgruppe[1]
Die Carbonsäure 1 reagiert mit Phosphortribromid (2) über einen Zwischenschritt zu einem Carbonsäurebromid 3. Dieses tautomerisiert zur Enolform 4. Bei der Reaktion mit Brom bildet sich unter Abspaltung von Bromwasserstoff ein α-Bromcarbonsäurebromid 5. Die Carbonylgruppe in 5 wird nun von einem Wassermolekül angegriffen. Über die Zwischenstufe 6 entsteht die α-Bromcarbonsäure 7 – wobei Bromwasserstoff abgespalten wird.[7][8]
Anwendungen
[Bearbeiten | Quelltext bearbeiten]Aus α-Halogencarbonsäure lassen sich diverse Derivate herstellen:
- α-Hydroxysäuren durch eine Reaktion mit Natriumhydroxid
- α-Aminosäuren durch eine Reaktion mit Ammoniak
- Malonsäurederivate durch Reaktion mit Natriumcyanid und anschließender Hydrolyse des Nitrils
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Literatur
[Bearbeiten | Quelltext bearbeiten]- H. Beyer, W. Walter: Lehrbuch der Organischen Chemie. 23. überarb. und aktualisierte Auflage. S. Hirzel Verlag, Stuttgart/Leipzig 1998, ISBN 3-7776-0808-4.
- L. Kürti, B. Czakó: Stratigic Applications of Named Reactions in Organic Synthesis. Elsevier Academic Press, Amsterdam 2005, ISBN 978-0-12-429785-2 S. 200.
- Reinhard Brückner, Reaktionsmechanismen: organische Reaktionen, Stereochemie, moderne Synthesemethoden, 3. Aufl., aktualisiert und überarb., korr. Nachdr. Spektrum Akad. Verl, Berlin 2007, ISBN 3-8274-1579-9, S. 494.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Eintrag in www.organische-chemie.ch
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Z. Wang: Comprehensive Organic Name Reactions and Reagents, 3 Volume Set. John Wiley & Sons, Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 1371 f.
- ↑ C. Hell: Ueber eine neue Bromirungsmethode organischer Säuren. In: Ber. Dtsch. Chem. Ges. Band 14, 1881, S. 891–893, doi:10.1002/cber.188101401187.
- ↑ J. Volhard: Ueber Darstellung α-bromirter Säuren. In: Justus Liebigs Ann. Chem. Band 242, Nr. 1–2, 1887, S. 141–163, doi:10.1002/jlac.18872420107.
- ↑ N. Zelinsky: Ueber eine bequeme Darstellungsweise von α-Brompropionsäureester. In: Ber. Dtsch. Chem. Ges. Band 20, Nr. 1, 1887, S. 2026, doi:10.1002/cber.188702001452.
- ↑ Michael B. Smith: March's Advanced Organic Chemistry. Wiley & Sons, 7. Auflage, 2013, ISBN 978-0-470-46259-1, S. 672–673.
- ↑ Reinhard Brückner: Reaktionsmechanismen: organische Reaktionen, Stereochemie, moderne Synthesemethoden. 3. Aufl., aktualisiert und überarb., korr. Nachdr. Spektrum Akad. Verl, Berlin 2007, ISBN 3-8274-1579-9, S. 494.
- ↑ L. Kürti, B. Czakó: Stratigic Applications of Named Reactions in Organic Synthesis. Elsevier Academic Press, Amsterdam 2005, ISBN 978-0-12-429785-2, S. 200.
- ↑ T. Laue, A. Plagens: Namens- und Schlagwortreaktionen der Organischen Chemie. Teubner Verlag, 2006, ISBN 3-8351-0091-2, S. 182–184.

