Mignonac-Reaktion
Die Mignonac-Reaktion ist in der Chemie eine Synthese-Methode zur Herstellung von primären Aminen 2. Dabei werden Aldehyde 1a (R1 = Organylrest; R2 = H) oder Ketone 1b (R1,R2 = Organylrest) in flüssigem Ammoniak katalytisch hydriert.[1]
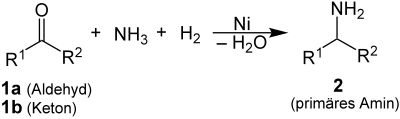
Als Lösungsmittel dient absolutes Ethanol, als Katalysator Nickel.[2]
Analog lassen sich auch sekundäre Amine darstellen:
R2-CHO + H2N-R1 --> R2-CH(OH)-NH-R1 --> R2-CH=N-R1 + H2O
R2-CH=N-R1 + H2 --> R2-CH2-NH-R1.
Atomökonomie[Bearbeiten | Quelltext bearbeiten]
Eine alternative Methode zur Herstellung von primären Aminen ist die Gabriel-Synthese, deren Atomökonomie ist im Vergleich zur Mignonac-Reaktion jedoch sehr schlecht. Bei der Mignonac-Reaktion entsteht als einziges Koppelprodukt Wasser. Deshalb ist die Mignonac-Reaktion deutlich wirtschaftlicher und ressourchenschonender als die Gabriel-Synthese.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Georges Mignonac: Nouvelle méthode générale de préparation des amines à partir des aldéhydes ou des cétones, Compt. Rend. 1921, 172, S. 223–226.
- ↑ The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals, 14. Auflage (Merck & Co., Inc.), Whitehouse Station, NJ, USA, 2006; S. ONR-62, ISBN 978-0-911910-00-1.