Kresolrot
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||
| Allgemeines | ||||||||||
| Name | Kresolrot | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C21H18O5S | |||||||||
| Kurzbeschreibung |
grünes bis dunkelrotes kristallines Pulver[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 382,43 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
| |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Kresolrot ist ein Triphenylmethanfarbstoff und gehört zur Gruppe der Sulfonphthaleine. Es findet Verwendung als pH-Indikator. Sein Phthalein-Analogon ist das o-Kresolphthalein. Durch Bromierung kann das Bromkresolpurpur dargestellt werden.
Eigenschaften
Es liegen zwei Farbumschlagspunkte vor:[4][5]
- pH 0,2–1,8: Farbänderung von Rot nach Gelb
- pH 7,0–8,8: Farbänderung von Gelb nach Violett
Kresolrot enthält zwei Hydroxygruppen und einen wenig stabilen Sultonring. Im wässrigen Medium wird dieser Ring gespalten, und nach einer Umlagerung entsteht die chinoide gelb gefärbte Form des Farbstoffs. Im stark saurem Milieu (pH < 1,8) wird das chinoide System protoniert, die Lösung wird dadurch rot. Im basischen Milieu (pH = 7,0–8,8) wird die Hydroxygruppe deprotoniert und die Lösung färbt sich violett.[6]
| Spezies | H2In | HIn− | In2− |
|---|---|---|---|
| Struktur |  |
 |
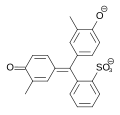
|
| pH | < 1,8 | 2,0–7,0 | > 8,8 |
| Farbe | Rot | Gelb | Violett |
Verwendung
Kresolrot wird bei Säure-Base-Titrationen als Indikator eingesetzt. Dabei wird meistens nur der zweite Umschlagsbereich (pH = 7,0–8,8) zur Indikation verwendet.
Einzelnachweise
- ↑ a b c d Datenblatt Cresol red bei Sigma-Aldrich (PDF).
- ↑ a b Datenblatt Kresolrot bei Merck.
- ↑ Eintrag zu Kresolpurpur. In: Römpp Online. Georg Thieme Verlag
- ↑ I. Kolthoff, C. Rosenblum: Acid-Base Indicators, MacMillan, New York 1937, S. 108–109.
- ↑ R. W. Sabnis: Handbook of Acid-Base Indicators, CRC Press, 2008, S. 105.
- ↑ Udo R. Kunze: Grundlagen der quantitativen Analyse, 3. Auflage, Georg Thieme Verlag, Stuttgart 1990, S. 96.
