Methylorange
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||
| Allgemeines | ||||||||||
| Name | Methylorange | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C14H14N3NaO3S | |||||||||
| Kurzbeschreibung |
orangefarbener Feststoff mit schwachem Geruch[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 327,34 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
1,28 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
schlecht in Wasser (ca. 5 g·l−1 bei 20 °C)[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Methylorange gehört zur Gruppe der Azofarbstoffe. Es ist das Natriumsalz der 4-[4-(Dimethylamino)phenylazo]benzolsulfonsäure und wird zumeist als pH-Indikator verwendet.
Darstellung
Sulfanilsäure wird mit Salpetriger Säure diazotiert und so zu 4-Benzoldiazoniumsulfonsäure umgesetzt:

Anschließend wird die 4-Benzoldiazoniumsulfonsäure mit N,N-Dimethylanilin ( grün ) gekuppelt und mit Natronlauge in das Natriumsalz überführt und ausgefällt:[4]
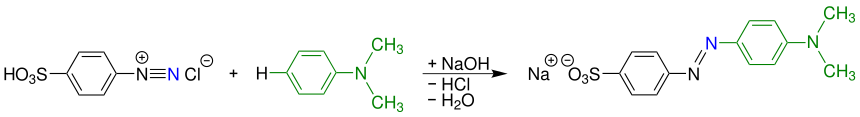
Das so erhaltene Natriumsalz – zugleich ein Azofarbstoff – ist Methylorange.
Eigenschaften
Methylorange bildet orangefarbene Kristalle.
Im stark sauren pH-Bereich ist die Azogruppe protoniert. Bei Basenzugabe deprotoniert die Gruppe im pH-Bereich 3,1 bis 4,4 und es tritt ein Farbumschlag von rot nach gelborange auf.[5]
Einzelnachweise
- ↑ a b c d e f Eintrag zu Methylorange in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ Applichem: Sicherheitsdatenblatt Methylorange (C.I. 13025), Stand: 05.August 2016, abgerufen am 12. September 2016
- ↑ Datenblatt Methylorange bei Merck
- ↑ Autorenkollektiv: Organikum. 21. Auflage. Wiley-VCH, 2001, ISBN 3-527-29985-8, S. 645.
- ↑ Indicator Reagents. In: Ullmann's Encyclopedia of Industrial Chemistry (engl.).


