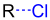Grob-Fragmentierung
 Modellhafte Darstellung der Grob-Fragmentierung anhand eines Dreiecks. |
Die Grob-Fragmentierung (auch heterolytische Fragmentierung) wird unter dem Begriff Namensreaktion der Organischen Chemie geführt.[1][2] Genauer beschreibt Cyril A. Grob (1917–2003) durch die Grob-Fragmentierung allerdings im Allgemeinen chemische Reaktionen, bei denen eine Verbindung in drei Fragmente (lat. fragmentum ‚Fraktion‘ oder ‚Bruchstück‘) zerlegt wird.[2][3][4] Nach Grob lässt sich dieses Vorgehen beispielsweise zur Strukturaufklärung nutzen.[2][3]
1967 betont Grob, dass der Begriff der Fragmentierung, chemisch gesehen, bereits eine Vielzahl unterschiedlicher Reaktionen und spezifischer Reaktionsmechanismen umfasst.[2][5] Beispielsweise treten im Rahmen einer Fragmentierung häufig Reaktionen wie die Substitution, Umlagerung oder Eliminierung auf.[5] Der hier dargestellte Inhalt deckt demnach nicht das gesamte Spektrum des Begriffs der Grob-Fragmentierung ab, sondern dient der Einführung in das Prinzip dieses Reaktionstyps.
Reaktionsprinzip
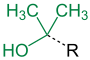
[Bearbeiten | Quelltext bearbeiten]Wie bereits erwähnt, wird im Zusammenhang mit der Grob-Fragmentierung von der Zerteilung einer organischen Verbindung in drei Fragmente gesprochen.[2][6] Der Vorgang wird hier exemplarisch an einem 3-Chlorpropylalkylether (wenn R Alkylrest) dargestellt. Ein entstehendes Fragment verlässt dabei den Ether ohne Mitnahme des bindenden Elektronenpaars.[2] Es liegt somit in der Regel als Kation (auf Produktseite in grün) vor.[2] In älterer, englischsprachiger Literatur wird dieses Fragment auch als electrofuge bezeichnet.[2] Ein weiteres Fragment spaltet sich als neutrale, ungesättigte Verbindung (auf Produktseite in schwarz) aus der Ausgangsverbindung ab, während ein drittes Fragment, meist in Form eines Anions (auf Produktseite in blau) aufgrund der Mitnahme des bindenden Elektronenpaares, aus dem Edukt hervorgeht.[2] Beim zuletzt genannten Fragment handelt es sich in älterer, englischsprachiger Literatur um das sogenannte nucleofuge.[2]

Um der Literatur entsprechend das Verständnis zu erleichtern, wird im Folgenden auf die beiden englischsprachigen Begriffe electrofuge und nucleofuge zurückgegriffen.
Reaktionsmechanismus der allgemeinen Fragmentierung
[Bearbeiten | Quelltext bearbeiten]Mechanistisch betrachtet, lässt sich das eben angeführte Beispiel folgendermaßen darstellen, wobei die Färbung der Bindungen und sonstigen Strukturen sich (wie oben) nach der Zugehörigkeit zum jeweils entstehenden Fragment richtet:

Handelt es sich bei dem hier dargestellten Rest R um ein Proton, so besteht unter Wasserstoffabspaltung die Möglichkeit, dass das electrofuge ebenfalls als neutrale Verbindung vorliegt. Dazu lässt sich nachfolgend die zweite Zeile der Tabelle und die Fragmentierung von Di-tert-butylmethanol betrachten.
Beispiele entstehender Fragmente
[Bearbeiten | Quelltext bearbeiten]Entsprechend der bisher eingeführten Färbung soll folgende Tabelle einen beispielhaften Überblick über entstehende Fragmente in Abhängigkeit spezifischer, vor der Fragmentierung vorliegender, Strukturen geben. Die mögliche Beschaffenheit der Reste R, R1 und R2 ergibt sich dabei entsprechend der Färbung gemäß der Tabelle.
Mechanistische Beispiele von Fragmentierungen
[Bearbeiten | Quelltext bearbeiten]Wie bereits verdeutlicht, lässt sich die Grob-Fragmentierung als Reaktionstypus auffassen, in welchem verschiedene Arten chemischer Reaktionen zusammenfallen.[3] Nachfolgend dienen drei exemplarische Reaktionen der Verdeutlichung der Anwendung des Reaktionsprinzips der Grob-Fragmentierung auf bestimmte chemische Reaktionen. Die Färbungen der einzelnen Strukturen erfolgt dabei wie gehabt.
Fragmentierung von Di-tert-butylmethanol
[Bearbeiten | Quelltext bearbeiten]Eine Fragmentierungsreaktion wird im Rahmen der Dehydratation und der damit einhergehenden intramolekularen Umlagerung einer Alkylgruppe von Di-tert-butylmethanol beschrieben:[6][7]

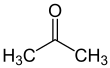
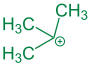
Mechanistisch betrachtet spaltet sich aus dem Alkohol (1) zunächst das Hydroxidion als nucleofuge ab, wonach die intramolekulare Alkylgruppen-Wanderung und somit die Entstehung eines tertiären Carbeniumions erfolgt.[7] Unter Abspaltung eines kleineren Carbeniumions, dem electrofuge (2), folgt die Ausbildung eines neutralen Alkens (3):[7]
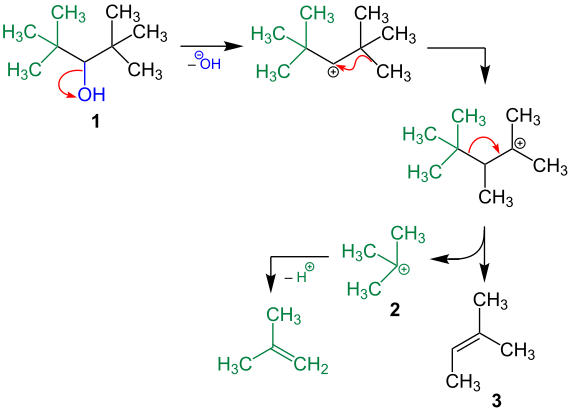
Unter Abspaltung eines Protons kann 2 im weiteren Verlauf ebenfalls zum Alken umgesetzt werden, so dass das electrofuge in diesem Fall am Ende der Reaktion ebenfalls als ungeladenes Teilchen vorliegt.
Fragmentierung von 2,3-Dibrom-3-phenylpropansäure
[Bearbeiten | Quelltext bearbeiten]Ein Vorschlag dieses Reaktionsmechanismus beschreibt zunächst die Deprotonierung des Säurederivats (4) mittels Natriumhydrogencarbonat.[6][8][9] Anschließend erfolgt über die Abspaltung von Kohlenstoffdioxid, als electrofuge, und einem Bromanion, als nucelofuge, die Bildung von cis-1-Brom-2-phenylethen.[8][9]:

1,4-Eliminierung von 1,4-Dibromcyclohexan unter Fragmentierung
[Bearbeiten | Quelltext bearbeiten]Diese 1955 von Grob beschriebene Eliminierungsreaktion wird in der Literatur als namensgebend für den Reaktionstyp der Grob-Fragmentierung ausgewiesen.[6][10] Hinsichtlich des verwendeten Dibromids läuft die Reaktion sowohl für das cis- als auch das trans-Isomer in quantitativ gleicher Ausbeute ab.[10] Nach Zusatz von Zink erfolgt der Zerfall der Verbindung (6) in Zinkbromid und Diallyl (7):[10]

Siehe auch
[Bearbeiten | Quelltext bearbeiten]Atomökonomie
[Bearbeiten | Quelltext bearbeiten]Die Atomökonomie der Grob-Fragmentierung lässt sich nicht eindeutig klassifizieren. Bezüglich des Reaktionsprinzips, der simplen Zerteilung einer Verbindung in drei Fragmente, lässt sich die Effizienz der Grob-Fragmentierung als sehr gut einstufen, insofern die Fragmentierung beispielsweise nur zur Strukturaufklärung angewendet wird. Wird mittels Fragmentierung die Synthese eines einzelnen Fragments angestrebt, so können allerdings niedermolekulare Abfälle, wie Kohlenstoffdioxid oder Halogenide, anfallen, wodurch die Effizienz der entsprechenden Reaktionen gemindert wird. Demnach sollte die Atomökonomie, abhängig von der jeweils betrachteten Reaktion, separat beurteilt werden.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Daniel Zerong Wang: Comprehensive Organic Name Reactions and Reagents. Band 1. John Wiley & Sons, Inc., Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 1279–1283, doi:10.1002/9780470638859.conrr197.
- ↑ a b c d e f g h i j Cyril. A. Grob, Peter. W. Schiess: Heterolytic Fragmentation. A Class of Organic Reactions. In: Angewandte Chemie International Edition in English. Band 6, Nr. 1, 1967, S. 1–15, doi:10.1002/anie.196700011.
- ↑ a b c Peter Schiess: Cyril A. Grob (1917–2003): Fragmentierung und Induktivität. In: Angewandte Chemie. Band 116, Nr. 34, 2004, S. 4492, doi:10.1002/ange.200461144.
- ↑ Werner Scholze-Stubenrecht (Hrsg.): Duden. Deutsches Universal-wörterbuch. 8. Auflage, Bibliographisches Institut GmbH, Berlin, 2015, ISBN 978-3-411-05508-1, S. 636.
- ↑ a b Cyril. A. Grob: Mechanisms and Stereochemistry of Heterolytic Fragmentation. In: Angewandte Chemie International Edition in English. Band 8, Nr. 8, 1969, S. 535–546, doi:10.1002/anie.196905351.
- ↑ a b c d Kathrin Prantz, Johann Mulzer: Synthetic Applications of the Carbonyl Generating Grob Fragmentation. In: Chemical Reviews. Band 110, Nr. 6, 2010, S. 3741–3766, doi:10.1021/cr900386h.
- ↑ a b c Frank C. Whitmore, E. E. Stahly: The Common Basis of Intramolecular Rearrangements. II. The Dehydration of Di-tert-butylcarbinol and the Conversion of the Resulting Nonenes to Trimethylethylene and Isobutylene. In: Journal of the American Chemical Society. Band 55, Nr. 10, 1933, S. 4153–4157, doi:10.1021/ja01337a042.
- ↑ a b Erling Grovenstein Jr., Donald E. Lee: The Stereochemistry and Mechanism of the Transformation of Cinnamic Acid Dibromide to β-Bromostyrene. In: Journal of the American Chemical Society. Band 75, Nr. 11, 1953, S. 2639–2644, doi:10.1021/ja01107a025.
- ↑ a b Stanley J. Cristol, William P. Norris: Mechanisms of Elimination Reactions. IX. The Spontaneous Decomposition of Salts of β-Halo Acids. II. trans-Cinnamic Acid Dibromide. In: Journal of the American Chemical Society. Band 75, Nr. 11, 1953, S. 2645–2646, doi:10.1021/ja01107a026.
- ↑ a b c C. A. Grob, W. Baumann: Die 1,4-Eliminierung unter Fragmentierung. In: Helvetica Chimica Acta. Band 38, Nr. 3, 1955, S. 594–610, doi:10.1002/hlca.19550380306.