Bariumchlorit
Zur Navigation springen
Zur Suche springen
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
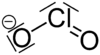
| |||||||
| Allgemeines | |||||||
| Name | Bariumchlorit | ||||||
| Summenformel | Ba(ClO2)2 | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 272,23 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Schmelzpunkt | |||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Bariumchlorit ist eine chemische Verbindung aus der Gruppe der Chlorite.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Im Labor gewinnt man es durch Reaktion von Chlordioxid mit Bariumhydroxid und Wasserstoffperoxid:[3]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Bariumchlorit ist ein Feststoff, welcher sich bei Erhitzung auf 190 °C explosionsartig zersetzt. Er kommt auch als Hydrat Ba(ClO2)2·3,5 H2O vor, welches eine monokline Kristallstruktur mit der Raumgruppe C2/c (Raumgruppen-Nr. 15) besitzt.[4]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Bariumchlorit kann zur Herstellung von Chloriger Säure oder Natriumchlorit verwendet werden.[5]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ P. G. Urben: Bretherick's handbook of reactive chemical hazards. 2006, ISBN 0-12-372563-1 (Seite 96 in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ G. Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 312.
- ↑ Barium chlorite hydrate, Ba(ClO2)2·3.5H2O Acta Cryst. (2005). C61, i49-i50 doi:10.1107/S010827010500925X
- ↑ M. Mazumdar: Rudiments of Chemistry. 1. Auflage. 2006, ISBN 81-89781-53-7 (Seite 382 in der Google-Buchsuche).
