„2-Hydroxyethanal“ – Versionsunterschied
| [gesichtete Version] | [ungesichtete Version] |
Rjh (Diskussion | Beiträge) |
Keine Bearbeitungszusammenfassung |
||
| Zeile 28: | Zeile 28: | ||
== Gewinnung und Darstellung == |
== Gewinnung und Darstellung == |
||
Es existiert eine Vielzahl an Wegen, um Glycolaldehyd darzustellen, beispielsweise durch vorsichtiges Oxidieren von [[Ethylenglycol]] mittels [[Wasserstoffperoxid]] in Gegenwart von [[Eisen(II)-sulfat]].<ref>Hans Peter Latscha, Uli Kazmaier und Helmut Alfons Klein: ''Organische Chemie: Chemie-Basiswissen II''. Springer, Berlin; 6., vollständig überarbeitete Auflage 2008, ISBN 978-3-540-77106-7 S. 217</ref> |
Es existiert eine Vielzahl an Wegen, um Glycolaldehyd darzustellen, beispielsweise durch vorsichtiges Oxidieren von [[Ethylenglycol]] mittels [[Wasserstoffperoxid]] in Gegenwart von [[Eisen(II)-sulfat]].<ref>Hans Peter Latscha, Uli Kazmaier und Helmut Alfons Klein: ''Organische Chemie: Chemie-Basiswissen II''. Springer, Berlin; 6., vollständig überarbeitete Auflage 2008, ISBN 978-3-540-77106-7 S. 217</ref> |
||
[[Datei:Reichsadler.svg|700px]] |
|||
Durch katalytische Umpolung von [[Formaldehyd]] lässt sich Glycolaldehyd aus einem C<sub>1</sub>-Baustein herstellen. Diese Reaktion ist von Bedeutung, um die C<sub>1</sub>-Rohstoffbasis (Erdgas, Kohle, Methanhydrat aus der Tiefsee) für Synthesen nutzbar zu machen.<ref>DE000004212264A1 (1992) Verfahren zur katalytischen Herstellung von Kondensationsprodukten des Formaldehyds</ref> |
Durch katalytische Umpolung von [[Formaldehyd]] lässt sich Glycolaldehyd aus einem C<sub>1</sub>-Baustein herstellen. Diese Reaktion ist von Bedeutung, um die C<sub>1</sub>-Rohstoffbasis (Erdgas, Kohle, Methanhydrat aus der Tiefsee) für Synthesen nutzbar zu machen.<ref>DE000004212264A1 (1992) Verfahren zur katalytischen Herstellung von Kondensationsprodukten des Formaldehyds</ref> |
||
Version vom 2. März 2010, 18:32 Uhr
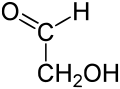
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Allgemeines | ||||||||||
| Name | 2-Hydroxyethanal | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C2H4O2 | |||||||||
| Kurzbeschreibung |
farb- und geruchloses Pulver | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 60,05 g/mol | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
leicht löslich in Wasser und Ethanol | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Glycolaldehyd ist die einfachste Verbindung der Gruppe der Hydroxyaldehyde. Er verfügt über eine Aldehyd- und eine Hydroxyl-Gruppe. Somit kann man ihn formal den Kohlenhydraten zuordnen (Aldodiose).
Vorkommen
Glycolaldehyd entsteht beim Abbau von Ethylenglycol im menschlichen Körper. Weiterhin wurde Glycolaldehyd im Weltraum nachgewiesen.[2] Es wird durch die Formose-Reaktion aus Formaldehyd gebildet und kann deshalb schon in der präbiotischen Phase der Evolution entstanden sein.
Gewinnung und Darstellung
Es existiert eine Vielzahl an Wegen, um Glycolaldehyd darzustellen, beispielsweise durch vorsichtiges Oxidieren von Ethylenglycol mittels Wasserstoffperoxid in Gegenwart von Eisen(II)-sulfat.[3]
 Durch katalytische Umpolung von Formaldehyd lässt sich Glycolaldehyd aus einem C1-Baustein herstellen. Diese Reaktion ist von Bedeutung, um die C1-Rohstoffbasis (Erdgas, Kohle, Methanhydrat aus der Tiefsee) für Synthesen nutzbar zu machen.[4]
Durch katalytische Umpolung von Formaldehyd lässt sich Glycolaldehyd aus einem C1-Baustein herstellen. Diese Reaktion ist von Bedeutung, um die C1-Rohstoffbasis (Erdgas, Kohle, Methanhydrat aus der Tiefsee) für Synthesen nutzbar zu machen.[4]

Eigenschaften
Glycolaldehyd neigt zur Dimerisierung zu 2,5-Dihydroxy-1,4-Dioxan (CAS: 23147-58-2, Smp.: 85 °C). Es reagiert weiterhin mit Propenal zu Ribose, einem essenziellen Bestandteil der Ribonukleinsäure, und gilt damit als Vorstufe zum Ursprung des Lebens.
Verwendung
Glycolaldehyd wird zur Herstellung von Polymeren, die freie Hydroxygruppen enthalten sowie als Zwischenprodukt für verschiedene Ester und Aminoalkohole verwendet.
Einzelnachweise
- ↑ a b Sicherheitsdatenblatt (Carl Roth)
- ↑ Pressemitteilung der Max-Planck-Gesellschaft
- ↑ Hans Peter Latscha, Uli Kazmaier und Helmut Alfons Klein: Organische Chemie: Chemie-Basiswissen II. Springer, Berlin; 6., vollständig überarbeitete Auflage 2008, ISBN 978-3-540-77106-7 S. 217
- ↑ DE000004212264A1 (1992) Verfahren zur katalytischen Herstellung von Kondensationsprodukten des Formaldehyds
Weblinks
- Biological Magnetic Resonance Data Bank: Glycolaldehyde