Rubidiumchlorat
Zur Navigation springen
Zur Suche springen
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
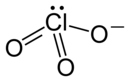
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Rubidiumchlorat | ||||||||||||
| Summenformel | RbClO3 | ||||||||||||
| Kurzbeschreibung |
weiße Prismen[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 168,92 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Dichte |
3,19 g·cm−3[2] | ||||||||||||
| Löslichkeit |
21,38 g·l−1 bei 0 °C[2] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Rubidiumchlorat ist das Rubidiumsalz der Chlorsäure mit der chemischen Zusammensetzung RbClO3.
Herstellung[Bearbeiten | Quelltext bearbeiten]
Rubidiumchlorat kann aus Rubidiumsulfat und Bariumchlorat hergestellt werden.[4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Physikalische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Die Löslichkeit von Rubidiumchlorat in Wasser nimmt mit steigender Temperatur zu und ist in untenstehender Tabelle angegeben.
| Löslichkeit von RbClO3 in Wasser[5] | ||||||||||
| Temperatur [°C] | 0 | 8 | 19,8 | 30 | 42,2 | 50 | 76 | 99 | ||
| Löslichkeit [g/l] | 21,38 | 30,7 | 53,6 | 80 | 124,8 | 159,8 | 341,2 | 628 | ||
Rubidiumchlorat kristallisiert im trigonalen Kristallsystem mit der Raumgruppe R3m (Raumgruppen-Nr. 160) und den Gitterparametern a = 608.9 pm und c = 817.4 pm, in der Elementarzelle befinden sich drei Formeleinheiten.[6]
Chemische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Beim Erhitzen zerfällt Rubidiumchlorat in Rubidiumchlorid und Sauerstoff:
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Wilhelm Steffen: Lehrbuch der reinen und technischen Chemie: Anorganische Experimental-chemie. J. Maier, 1893, S. 89. Volltext
- ↑ a b Dale L. Perry, Sidney L. Phillips: Handbook of inorganic compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 333 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ R. Abegg, F. Auerbach: "Handbuch der anorganischen Chemie". Verlag S. Hirzel, Bd. 2, 1908. S. 431.Volltext
- ↑ Aterton Seidell: "Solubilities Of Organic Compounds Vol - I", S. 1429. Volltext
- ↑ Jean D’Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-540-60035-0, S. 686 (eingeschränkte Vorschau in der Google-Buchsuche).

