Rubidiumchromat
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 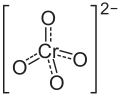
| ||||||||||
| Allgemeines | ||||||||||
| Name | Rubidiumchromat | |||||||||
| Summenformel | Rb2CrO4 | |||||||||
| Kurzbeschreibung |
gelbe Kristalle [1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 286,93 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
3,52 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
gut in Wasser (620 g·l−1 bei 0 °C[1], 736 g·l−1 bei 20 °C[2]) | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Rubidiumchromat ist das Rubidiumsalz der Chromsäure.
Herstellung
Rubidiumchromat kann aus Rubidiumcarbonat und Rubidiumdichromat hergestellt werden.
Ebenfalls möglich ist die Darstellung durch Reaktion von Rubidiumcarbonat und Chrom(VI)-oxid[4]
oder Rubidiumdichromat mit Bariumhydroxid.[4]
Eigenschaften
Rubidiumchromat ist ein gelber Feststoff mit rhombischen Kristallen, der leicht löslich in Wasser ist.[4] Die Löslichkeit nimmt mit steigender Temperatur zu: 100 g gesättigte Lösung enthalten bei 0 °C 38,27 g und bei 25 °C 43,265 g Rubidiumchromat.[2] Er kristallisiert im orthorhombischen Kristallsystem mit der Raumgruppe Pnam und den Gitterparametern a = 800,1 pm, b = 1072,2 pm und c = 607,4 pm, in der Elementarzelle befinden sich vier Formeleinheiten.[1] Diese ist isotyp mit zu der von Kaliumchromat und Kaliumsulfat.[4]
Einzelnachweise
- ↑ a b c d e Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0, S. 686 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Dale L. Perry, Sidney L. Phillips: Handbook of inorganic compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 333f. (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt Rubidium chromate bei Sigma-Aldrich (PDF).
- ↑ a b c d Georg Brauer: Handbuch der präparativen anorganischen Chemie. 3., umgearb. Auflage. Band 3. Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1525.






