Hordenin
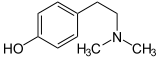
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Hordenin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C10H15NO | ||||||||||||||||||
| Kurzbeschreibung |
weißes bis hellgelbes Pulver mit Knollen[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 165,23 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Hordenin ist eine chemische Verbindung, die in vielen Pflanzen vorkommt. Hordenin gehört zu den Alkaloiden. Es entsteht biochemisch aus Tyramin.
Hordenin wurde 1894 im Kaktus Anhalonium fissuratum von Arthur Heffter entdeckt und von ihm Anhalin genannt.[2] Leger wies 1906 sein Vorkommen in Gerste (Hordeum vulgare), welche der Substanz ihren Namen gab, nach und konnte die Struktur ermitteln.[3]
Pharmakologie[Bearbeiten | Quelltext bearbeiten]
Hordenin ist ein Sympathomimetikum und aktiviert in hoher intravenöser Dosierung nikotinische Acetylcholinrezeptoren und Adrenozeptoren. Bei oraler Zufuhr (über den Verdauungstrakt) tritt diese Wirkung nicht ein. Weil es auch in geringen Mengen in Futterpflanzen wie Gerste vorkommt, nehmen Tiere Hordenin unbeabsichtigt zu sich. Bei Pferderennen kann es deswegen zu einem Dopingverdacht kommen.[4][5][6]
Darüber hinaus zeigt Hordenin eine hemmende Wirkung auf das Wachstum anderer Pflanzen.[7] Daher wird vermutet, dass diese Substanz zur Selbstverteidigung der produzierenden Pflanze dient.[8]
Unter den 13.000 verschiedenen Lebensmittelinhaltsstoffen, die von einer Forschergruppe der Universität Erlangen-Nürnberg untersucht wurden, hat der Bierinhaltsstoff Hordenin die beste Aktivität gegenüber dem Dopamin-D2-Rezeptor.[9]
Analytik[Bearbeiten | Quelltext bearbeiten]
Die zuverlässige qualitative und quantitative Bestimmung von Hordenin gelingt nach adäquater Probenvorbereitung durch Einsatz der HPLC.[10]
Literatur[Bearbeiten | Quelltext bearbeiten]
- Mann JD, Steinhart CE, Mudd SH: Alkaloids and Plant Metabolism. V. The Distribution And Formation Of Tyramine Methylpherase During Germination Of Barley. In: J Biol Chem. 238. Jahrgang, Nr. 2, Februar 1963, S. 676–681.
- Sommer, Thomas; Hübner, Harald; El Kerdawy, Ahmed; Gmeiner, Peter; Pischetsrieder, Monika; Clark, Tim: Identification of the Beer Component Hordenine as Food-Derived Dopamine D2 Receptor Agonist by Virtual Screening a 3D Compound Database. Scientific Reports (2017), 7: 44201, doi:10.1038/srep44201.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d Datenblatt Hordenine bei Sigma-Aldrich, abgerufen am 4. April 2011 (PDF).
- ↑ Arthur Heffter: Ueber zwei Cacteenalkaloïde. In: Berichte der Deutschen Chemischen Gesellschaft. Band 27, Nummer 3, 1894, S. 2975–2979 (doi:10.1002/cber.18940270362).
- ↑ Güven KC, Percot A, Sezik E: Alkaloids in marine algae. In: Mar Drugs. 8. Jahrgang, Nr. 2, 2010, S. 269–284, doi:10.3390/md8020269, PMID 20390105, PMC 2852838 (freier Volltext).
- ↑ Hapke HJ, Strathmann W: [Pharmacological effects of hordenine]. In: DTW. Dtsch. Tierarztl. Wochenschr. 102. Jahrgang, Nr. 6, Juni 1995, S. 228–232, PMID 8582256.
- ↑ Frank M, Weckman TJ, Wood T, et al.: Hordenine: pharmacology, pharmacokinetics and behavioural effects in the horse. In: Equine Vet. J. 22. Jahrgang, Nr. 6, November 1990, S. 437–441, PMID 2269269.
- ↑ Richard A. Sams: Review of Possible Sources of Exposure of Horses to Natural Products and Environmental Contaminants Resulting in Regulatory Action. In: Proceedings of the Annual Convention of the AAEP. 43. Jahrgang, 1997, S. 220–223 (ivis.org [PDF; abgerufen am 11. August 2010]).
- ↑ Lovett JV: Changing perceptions of allelopathy and biological control. In: Biol Agric Hortic. 8. Jahrgang, Nr. 2, 1991, S. 89–100.
- ↑ Lovett JV, Hoult AHC: Biological activity of barley secondary metabolites. In: Proceedings of the 7th Australian Agronomy Conference. 1993 (org.au).
- ↑ Bier macht glücklich. Friedrich-Alexander-Universität Erlangen-Nürnberg, abgerufen am 21. März 2023.
- ↑ Hoult AH, Lovett JV: Biologically active secondary metabolites of barley. III. A method for identification and quantification of hordenine and gramine in barley by high-performance liquid chromatography., J. Chem. Ecol. 1993 Oct;19(10):2245–2254, PMID 24248573.
