Phenylphosphan
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
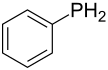
| ||||||||||
| Allgemeines | ||||||||||
| Name | Phenylphosphin | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C6H7P | |||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 110,10 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig | |||||||||
| Dichte |
1,001 g·cm−3 (15 °C)[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
160–161 °C[1] | |||||||||
| Dampfdruck |
13 hPa (40 °C)[1] | |||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[2] | |||||||||
| Brechungsindex |
1,5796 (20 °C)[3] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| MAK |
Schweiz: 0,05 ml·m−3 bzw. 0,25 mg·m−3[4] | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||
Phenylphosphin ist eine organische Phosphorverbindung bzw. ein einfach substituiertes Phosphinderivat.
Darstellung und Gewinnung
Die Synthese von Phenylphosphin gelingt durch die Reduktion von Dichlorphenylphosphin mittels Lithiumaluminiumhydrid.[5]
Eigenschaften
Phenylphosphin ist eine farblose Flüssigkeit mit unangenehmem bis ekelerregendem Geruch.[2][1] Ähnlich wie Phosphin neigt die Verbindung an der Luft zur spontanen Selbstentzündung. Sie ist somit als pyrophor anzusehen.[1] Die kontrollierte Oxidation durch Luftsauerstoff ergibt die entsprechende Phosphonsäure.[5]
Verwendung
Phenylphosphin wird in der Polymerensynthese angewendet, wo es bei einer Polyaddition mit 1,4-Divinylbenzol oder 1,4-Diisopropenylbenzol phosphorhaltige Polymere bildet. Diese besitzen bei einer Entzündung selbstverlöschende Eigenschaften. In Mischung mit brennbaren Polymeren wie Polyethylen oder Polypropylen können flammenbeständige Materialien erhalten werden.[6]
Einzelnachweise
- ↑ a b c d e f Lutz Roth, Ursula Weller-Schäferbarthold: Gefährliche Chemische Reaktionen. 41. Ergänzungslieferung, ecomed-Verlag 2003.
- ↑ a b c d e f Eintrag zu CAS-Nr. 638-21-1 in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-430.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte
- ↑ a b Leon D. Freedman, G. O. Doak: The Reduction of Benzenephosphonyl Dichloride. In: Journal of the American Chemical Society. Band 74, Nr. 13, 1. Juli 1952, S. 3414–3415, doi:10.1021/ja01133a504.
- ↑ Takatsugu Obata, Eiichi Kobayashi, Sadahito Aoshima, Junji Furukawa: Synthesis of new linear polymers containing phosphorus atom in the main chain by the radical polyaddition: Addition polymers of phenylphosphine with 1,4-divinylbenzene or 1,4-diisopropenylbenzene and their properties. In: Journal of Polymer Science Part A: Polymer Chemistry. Band 32, Nr. 3, 1994, S. 475–483, doi:10.1002/pola.1994.080320309.



