„Trichlorisocyanursäure“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Jü (Diskussion | Beiträge) K Datumskonvention |
Bot: Ein nicht mehr erreichbarer Weblink ersetzt, gemäß Botauftrag. |
||
| Zeile 59: | Zeile 59: | ||
| Jahr=1966 |
| Jahr=1966 |
||
| Seiten=115–120 |
| Seiten=115–120 |
||
| Online=[http://libgen. |
| Online=[http://libgen.io/scimag/get.php?doi=10.1007/bf00905495 PDF] |
||
| DOI=10.1007/bf00905495 |
| DOI=10.1007/bf00905495 |
||
}}</ref> |
}}</ref> |
||
Version vom 9. Oktober 2015, 15:20 Uhr
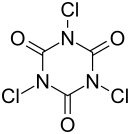
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Allgemeines | ||||||||||
| Name | Trichlorisocyanursäure | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C3Cl3N3O3 | |||||||||
| Kurzbeschreibung |
weißer Feststoff mit stechendem Geruch[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 232,41 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
2,07 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
wenig löslich in Wasser: 12 g·l−1 in Wasser (20 °C)[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Trichlorisocyanursäure (1,3,5-Trichlor-1,3,5-triazin-2,4,6-trion) bildet farblose, feuchtigkeitsempfindliche Kristalle.
Herstellung
Trichlorisocyanursäure wird durch Chlorierung von Cyanursäure bzw. Isocyanursäure hergestellt.[2]
Eigenschaften
Trichlorisocyanursäure bildet mit Wasser Hypochlorige Säure. Diese zerfällt unter Disproportionierung zu Chlorsäure und Salzsäure.
Verwendung
Trichlorisocyanursäure wird vor allem zur Langzeitchlorierung des Wassers in Swimmingpools verwendet. Dazu dienen massive, bis zu 250 g schwere Tabletten. Durch die geringe Löslichkeit wird der Wirkstoff nur langsam freigesetzt, was die Langzeitwirkung ermöglicht.
Zur Stoßchlorierung werden ähnliche, aber leicht lösliche und feinkörnige Substanzen verwendet.
Problematisch ist dabei die Anreicherung der Cyanursäure im Wasser, da dadurch die Wirksamkeit des Chlors vermindert wird. Bei höheren Konzentrationen der Cyanursäure im Badewasser (ab etwa 40 mg/l) muss die Dosierung von chlorbasierten Desinfektionsmitteln daher erhöht werden, um gleichbleibende Keimtötung zu erzielen.
Im Labor kann Trichlorisocyanursäure durch Zutropfen von verdünnter Salzsäure zur Darstellung von elementarem Chlor eingesetzt werden:
N-Chlorisocyanat kann durch Thermolyse aus Trichlorisocyanursäure gewonnen werden.[3]
Nachweis
Trichlorisocyanursäure lässt sich aufgrund ihrer oxidierenden Eigenschaften leicht nachweisen und z. B. iodometrisch bestimmen. Dazu wird eine in Wasser gelöste Probe mit Kaliumiodid versetzt und das sofort gebildete Iod mit Natriumthiosulfatlösung und Stärke als Indikator titriert.
Verwandte Verbindungen
Referenzen
- ↑ a b c d e f Eintrag zu Trichlorisocyanursäure in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich)
- ↑ Eintrag zu Trichlorisocyanursäure. In: Römpp Online. Georg Thieme Verlag
- ↑ E. Nachbaur, W. Gottardi: Darstellung und Eigenschaften von Chlorisocyanat. In: Monatshefte für Chemie. Band 97, Nr. 1, 1966, S. 115–120, doi:10.1007/bf00905495 (PDF).



