Blue-Bottle-Experiment
Unter dem Blue-Bottle-Experiment versteht man ein klassisches Schauexperiment der Chemie. In einem geschlossenen Gefäß befindet sich eine farblose Flüssigkeit und etwas Luft. Schüttelt man das Gefäß, so färbt sich die Flüssigkeit blau. Nach kurzer Zeit verschwindet die Farbe jedoch wieder. Je länger man schüttelt, desto länger bleibt die Färbung erhalten.
Chemisch gesehen ist dieser Versuch auch als Modellversuch für ein Redoxsystem verwandt mit NAD+/NADH2 möglich. Außerdem ist die Schüttelzeit proportional zur Färbungszeit (Reaktion 1. Ordnung).
Reaktion
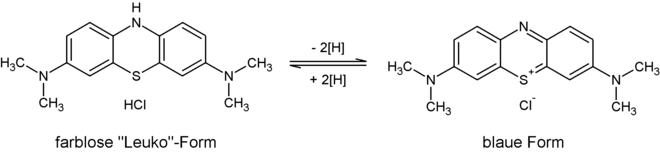
Die Reaktion zur Entfärbung beruht auf der Reduktion einer Methylenblau-Lösung zur Leuko-Form durch Glucose, die dabei zu Gluconsäure oxidiert wird.
Beim Schütteln wird das Leuko-Methylenblau durch Sauerstoff aus der Luft wieder zu farbigem Methylenblau oxidiert. Je intensiver man schüttelt, desto länger dauert die Färbung an. Bei einem ausreichenden Überschuss an Glucose kann dieses Experiment wiederholt werden, bis der Luftsauerstoff in dem verschlossenen Versuchsgefäß vollständig reduziert ist.
Weblinks
- Beschreibung auf Chemieunterricht.de, abgerufen am 15. November 2017.
- Versuchsvorschrift von der Uni Würzburg, abgerufen am 15. November 2017.
- Video: Experiment der Woche: Was ist die "Blue Bottle"?. Leibniz Universität Hannover 2011, zur Verfügung gestellt von der Technischen Informationsbibliothek (TIB), doi:10.5446/2095.