Etravirin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
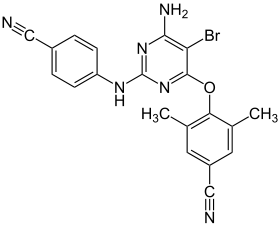
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Etravirin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C20H15BrN6O | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
Virustatikum, nichtnukleosidische Reverse-Transkriptase-Inhibitoren | |||||||||||||||||||||
| Wirkmechanismus |
nicht-kompetitive Hemmung der reversen Transkriptase | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 435,28 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Etravirin (ETV, Handelsname: Intelence®; Hersteller: Tibotec) ist ein Arzneistoff zur Behandlung HIV-infizierter Patienten im Rahmen einer HIV-Kombinationstherapie.
Etravirin gehört zur Substanzklasse der nichtnukleosidischen Reverse-Transkriptase-Inhibitoren (NNRTI).
Geschichte
[Bearbeiten | Quelltext bearbeiten]Intelence in Kombination mit anderen antiretroviralen Arzneimitteln wurde für die Therapie von Infektionen mit HIV-1 bei bereits vergeblich behandelten Patienten in den USA im Januar 2008 und in der Europäischen Union im August 2008 zugelassen.
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Etravirin gehört zur Substanzklasse der nichtnukleosidischen Reverse-Transkriptase-Inhibitoren (NNRTI). Der Wirkstoff bindet nicht-kompetitiv an die Reverse Transkriptase von HIV-I, nahe der Substratbindungsstelle für Nukleoside. Dadurch wird die katalytisch aktive Bindungsstelle blockiert. Es können nur wenige Nukleoside binden und die Polymerisation wird deutlich verlangsamt.
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Im Allgemeinen wird Etravirin gut vertragen, allerdings traten in einigen Studien die für NNRTIs typischen Nebenwirkungen Schwindel und Hautausschlag auf.[2] Die Nebenwirkungen führten aber selten zum Therapieabbruch.
Mitte 2009 gab der Hersteller bekannt, dass es zu einem Todesfall infolge eines Lyell-Syndroms sowie zu Überempfindlichkeitsreaktionen kombiniert mit Leberversagen kam.[3]
Resistenzen
[Bearbeiten | Quelltext bearbeiten]Gegenüber anderen NNRTIs hat Etravirin den Vorteil, dass es, neben einer sehr guten Wirkung gegen den Wildtyp, auch noch gegen die meisten NNRTI-resistenten Stämme gut wirksam ist. In Phase I/II Studien zeigte Etravirin seine hohe Potenz bei der Absenkung der Viruslast.[4]
Weblinks
[Bearbeiten | Quelltext bearbeiten]- AIDSMeds.com
- Neu im EAP: NNRTI Etravirin (PDF; 290 kB)
- Europäischer öffentlicher Beurteilungsbericht (EPAR) und Produktinformation zu Intelence auf der Website der Europäischen Arzneimittelagentur
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von 4-(6-Amino-5-bromo-2-(4-cyanoanilino)pyrimidin-4-yloxy)-3,5-dimethylbenzonitrile im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 10. Februar 2020.
- ↑ Kakuda 2006.
- ↑ Tibotec Therapeutics: Intelence: Important Drug Warning. (PDF; 74 kB) FDA, August 2009; abgerufen am 27. August 2009.
- ↑ B. Gruzdev, A. Rakhmanova, E. Doubovskaya u. a.: A randomized, double-blind, placebo-controlled trial of TMC125 as 7-day monotherapy in antiretroviral naive, HIV-1 infected subjects. In: AIDS, 17, 2003, S. 2487–2494. PMID 14600520.