Manganocen
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Allgemeines | ||||||||||
| Name | Manganocen | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C10H10Mn | |||||||||
| Kurzbeschreibung |
brauner kristalliner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 185,13 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
245 °C[2] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Manganocen ist eine metallorganische Verbindung des Mangans und zählt zu den Metallocenen. Der braune, oberhalb 158 °C rosafarbene Feststoff besitzt ungewöhnliche magnetische Eigenschaften.
Gewinnung und Darstellung
Manganocen lässt sich wie andere Metallocene aus Mangan(II)-chlorid und einer Cyclopentadienylverbindung, normalerweise Natriumcyclopentadienyl, herstellen. Dazu wird zunächst Cyclopentadien mit Natrium umgesetzt und deprotoniert.[3]
Durch Reaktion von Natriumcyclopentadienyl mit Mangan(II)-chlorid in Lösungsmitteln wie Tetrahydrofuran, Ethylenglycoldimethylether oder flüssigem Ammoniak entsteht dann das Manganocen.[3]
Eigenschaften
Da Mangan im Vergleich zu Eisen ein Valenzelektron weniger besitzt, besitzt auch Manganocen ein Elektron weniger als Ferrocen und erfüllt mit 17 Elektronen nicht die 18-Elektronen-Regel. Da das Mangan in einer sehr günstigen high-spin-d5-Konfiguration (jedes d-Orbital mit einem Elektron besetzt) vorliegt, kann es auch nicht zu Mn1+ reduziert werden, um die günstigen 18 Elektronen zu erhalten.[4]
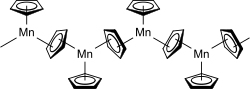
Im Festkörper liegt Manganocen in einer polymeren Struktur vor, in der jedes Mangan von drei Cyclopentadienyl-Liganden umgeben ist. Zwei der drei Liganden sind dabei mit jeweils zwei Manganzentren verbunden, während das dritte nur an ein Manganatom grenzt. Es bildet sich eine lange Kette. Die Abstände der C-Atome vom Mangan betragen bei den terminalen Liganden 242 pm, bei den verbrückten 240–330 pm.[5] Die verbrückenden Cyclopentadienyl-Liganden liegen nicht symmetrisch zwischen den Manganatomen.[6]
Unterhalb der Néel-Temperatur von 134 °C[7] ist Manganocen antiferromagnetisch. Oberhalb dieser besitzt der Komplex ein starkes magnetisches Moment mit einem Wert von 5,81 Bohrschen Magnetonen.[8]
Einzelnachweise
- ↑ Christoph Elschenbroich: Organometallchemie. 6. Auflage, Teubner, Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 452 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e Vorlage:Acros
- ↑ a b Christoph Elschenbroich: Organometallchemie. 6. Auflage, Teubner, Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 451 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Christoph Elschenbroich: Organometallchemie. 6. Auflage, Teubner, Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 468 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Christoph Elschenbroich: Organometallchemie. 6. Auflage, Teubner, Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 460 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Erwin Riedel, Ralf Alsfasser, Christoph Janiak und Thomas M. Klapötke: Moderne Anorganische Chemie. 4. Auflage, von Gruyter, 2007, ISBN 978-3-11-019060-1, S. 707.
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1619.
- ↑ Christoph Elschenbroich: Organometallchemie. 6. Auflage, Teubner, Wiesbaden 2008, ISBN 978-3-8351-0167-8, S. 455 (eingeschränkte Vorschau in der Google-Buchsuche).



