„Malolaktische Gärung“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Keine Bearbeitungszusammenfassung |
Ausgebaut; Sachen gelöscht, die nicht belegt bzw. wenig aussagekräftig waren |
||
| Zeile 1: | Zeile 1: | ||
Die '''malolaktische Gärung''' |
Die '''malolaktische Gärung''' tritt bei vielen [[Milchsäuregärung#Heterofermentative_Milchs.C3.A4ureg.C3.A4rung|heterofermentativen]] [[Milchsäurebakterien]] auf und spielt bei der [[Weinherstellung|Wein-]], Fruchsaft- und [[Champagner]]herstellung eine Rolle. Sie wird auch als biologischer Säureabbau bezeichnet. Die malolaktische Gärung ist eine sekündäre Gärung, die als Folge den Abbau von Säure im Medium hat. Sie folgt einer primären, Alkohol erzeugenden Gärung. Bei der malolaktischen Gärung [[Decarboxylierung|decarboxylieren]] bestimmte [[Milchsäurebakterien]] die [[Dicarbonsäure]] <small>L</small>-Malat (= deprotonierte From der <small>L</small>-Äpfelsäure) unter Energiegewinnung zur schwächeren [[Monocarbonsäure]] <small>L</small>-Lactat (= deprotonierte Form der <small>L</small>-[[Milchsäure]]). |
||
Der durch diese Gärung resultierende biologische Säureabbau führt bei der Weinherstellung zu einem harmonischen und ausgewogeneren Geschmacksbild - ein Effekt, der sich qualitätssteigernd auswirkt, der aber auch Risiken birgt: Säurearme [[Wein]]e sind weniger haltbar, weniger „spritzig“ und wirken nicht so frisch. |
|||
== |
== Vorkommen == |
||
Die malolaktische Gärung findet in vielen Mikroorganismen statt, die zur Energiegewinnung eine heterofermentative Gärung betreiben. Für die Weinherstellung ist ''[[Oenococcus oeni]]'' (alte Bezeichnung ''Leuconostoc oenos'') bedeutsam, ferner ''[[Lactobacillus]]'' spp. (z. B. ''[[Lactobacillus plantarum]]'') and ''[[Pediococcus]]'' spp.<ref>Zaunmüller, T. ''et al''. 2006: ''Variations in the energy metabolism of biotechnologically relevant heterofermentative lactic acid bacteria during growth on sugars and organic acids.'' In: ''Appl Microbiol Biotechnol''. '''72'''(3); 421–429; PMID 16826375; {{DOI|10.1007/s00253-006-0514-3}}</ref> |
|||
Die chemische Reaktion unter Mitwirkung der Milchsäurebakterien wird wie folgt beschrieben: |
|||
Auch [[Hefen]] können am Ende der [[Alkoholische Gärung|alkoholischen Gärung]] malolaktische Gärung betreiben. |
|||
:<math>\mathrm {\ HOOC{-}CH_2{-}CHOH{-}COOH \longrightarrow CH_3{-}CHOH{-}COOH + CO_2}</math> |
|||
== Biochemie == |
|||
=== Prozess === |
|||
Bei der malolaktischen Gärung wird der Decarboxylierung <small>L</small>-Malats zu <small>L</small>-Lactat katalysiert. Abhängig vom pH-Wert des Mediums kann Malat bzw. Lactat auch protoniert vorliegen |
|||
:<math>\mathrm {\ Malat + H^+ \xrightarrow{\text{pH 6}} \ Lactat + CO_2}</math> |
|||
:<math>\mathrm {\ HMalat + H^+ \xrightarrow{\text{pH 4}} \ HLactat + CO_2}</math> |
|||
Bei dieser Reaktion wird mit jedem Gramm abgebauter Äpfelsäure der Gesamtanteil der Säure im Wein um 0,4 g/L<sub>H<sub>2</sub>SO<sub>4</sub></sub> gesenkt. |
Bei dieser Reaktion wird mit jedem Gramm abgebauter Äpfelsäure der Gesamtanteil der Säure im Wein um 0,4 g/L<sub>H<sub>2</sub>SO<sub>4</sub></sub> gesenkt. |
||
| Zeile 26: | Zeile 32: | ||
|- |
|- |
||
|} |
|} |
||
Der Anstieg der flüchtigen Säure mit der Bildung eines Butteraromas ist auf eine Verstoffwechselung der [[Citronensäure]] und der [[Pentosen]] zu Ende der malolaktischen Gärung zurückzuführen. |
|||
=== Energiegewinnung === |
|||
[[Datei:LDH reaction.svg|300px|thumb|left|Die von der [[Lactatdehydrogenase]] (LDH) katalysierte Reaktion: Brenztraubensäure (links)wird (mit der gleichzeitigen [[Reduktion (Chemie)|Reduktion]] von [[Nicotinamidadenindinukleotid|NAD<sup>+</sup>]] zu NADH/H<sup>+</sup>) zu Milchsäure (rechts) reduziert.]] |
|||
Obwohl die chemische Reaktion seit Anfang der 1920 Jahre durch Arbeiten von Wenzel Seifert an der [[Höhere Bundeslehranstalt und Bundesamt für Wein- und Obstbau|Höheren Bundeslehranstalt und Bundesamt für Wein- und Obstbau]] in [[Klosterneuburg]] bekannt war, brauchte es noch nahezu 40 Jahre zum tieferen Verständnis der biologischen Säureabbaus. Die [[Malat-Dehydrogenase]] (MDH) ist das [[Enzym]], das die chemische Reaktion von [[Apfelsäure]] (Malat) zu [[Oxalessigsäure]] (Oxalacetat) [[Katalyse|katalysiert]]. Der Übergang zu [[Brenztraubensäure]] erfolgt über eine biochemische Decarboxylierung der Oxalessigsâure. Brenztraubensäure ist eine energiereiche [[chemische Verbindung|Verbindung]] und kann im [[Citratzyklus]] (auch ''Zitratzyklus'', ''Tricarbonsäurezyklus'' oder ''Krebs-Zyklus'' genannt) weiter abgebaut werden. Unter anaeroben Bedingungen kann sie mit Hilfe des Enzyms [[Lactatdehydrogenase]] zu [[Milchsäure]] verstoffwechselt werden (siehe [[Gärung]]). |
|||
Unter [[Standardbedingungen]] wird bei der Decarboxylierungsreaktion Energie freigesetzt. Dieser Wert ist vom pH-Wert abhängig. Bei pH 7 werden −26,5 kJ·mol<sup>−1</sup>, bei einem pH-Wert von 5,7 werden −33,9 kJ·mol<sup>−1</sup> freigesetzt.<ref>Kolb, S. ''et al''. (1992): ''Energy conservation in malolactic fermentation by Lactobacillus plantarum and Lactobacillus sake''. In: ''Arch Microbiol''. '''157'''(5); 457–463; PMID 1510572; {{DOI|10.1007/BF00249105}}</ref> In Weinen kann der pH-Wert durchaus bei 3,5 liegen, dann werden unter Standardbedingungen −46,5 kJ·mol<sup>−1</sup> erzeugt. Es ist jedoch anzumerken, dass unter ''phyiologischen'' Bedingungen Malat, Lactat und CO<sub>2</sub> nicht in einer Konzentration von 1 M vorliegen und während des Prozesses ständig Malat verbraucht wird und Lactat erzeugt wird. Daher ist der Energiegewinn unter physiologischen Bedingungen geringer.<ref>Olsen, EB. ''et al''. (1991): ''Electrogenic L-malate transport by Lactobacillus plantarum: a basis for energy derivation from malolactic fermentation''. In: ''J Bacteriol''. '''173'''(19); 6199–6206.; PMID 1917854; [http://www.ncbi.nlm.nih.gov/pmc/articles/PMC208371/pdf/jbacter00109-0275.pdf PDF] (freier Volltextzugriff, engl.)</ref> |
|||
[[Datei:Malolactic fermentation.svg|thumb|300px|Schema der Energiegewinnung bei der malolaktischen Gärung. Für Einzelheiten bitte Text beachten.]] |
|||
Die bei der Decarboxylierung freigesetzte Energie wird in Form eines [[Chemiosmotische Kopplung|Chemiosmotischen Mechanismus]] konserviert (vgl. Abbildung).<ref name="Liu">Liu, SQ. (2002): ''A review: malolactic fermentation in wine - beyond deacidification''. In: ''J Appl Microbiol''. '''92'''(4):589–601; PMID 11966898; [http://www3.interscience.wiley.com/cgi-bin/fulltext/118961772/PDFSTART PDF] (freier Volltextzugriff, engl.)</ref> Bei ''O. oeni'', der bei einem pH-Wert von 4 wächst, wird einfach protoniertes Malat (HMal<sup>1−</sup>) durch einen membranständigen Carrier (MleP) in die Zelle gebracht. Dieses wird zu Lactat decarboxyliert, welches bei pH 4 protoniert (HLac) vorliegt. Der Ausstrom aus der Zelle bei HLac erfolgt ohne Carrier. Bei ''[[Lactococcus lactis]]'' wächst unter höheren pH-Werten. Dort wird Malat (Mal<sup>2−</sup>) mit Lactat (Lac<sup>1−</sup>) durch einen Antiporter ausgetauscht. |
|||
In beiden Fällen wird im Netto eine (negative) Ladung per Austausch transportiert, was zu einer Energetisierung der Membran führt. Darüber hinaus wird im Zuge der Decarboxylierung ein Proton verbraucht, so dass auch ein [[Protonengradient]] aufgebaut werden kann. Beide Prozesse führend daher zu einem Aufbau einem [[Elektrochemischer Gradient|elektrochemischen Gradienten]] (''proton motive force''). Er wird von den Bakterien zur Aufrechterhaltung des pH-Wertes und zur Aufnahme von Nährstoffen genutzt. Jedoch reicht die bei malolaktischen Gärung freigesetzte Energie nicht als einzige Energiequelle aus, so dass die heterofermentativen Milchsäurebakterien weiterhin auf die Vergärung von [[Pentosen]] bzw. [[Hexosen]] angewiesen sind.<ref name="Liu" /> |
|||
== Geschichte == |
|||
Obwohl die chemische Reaktion seit Anfang der 1920 Jahre durch Arbeiten von Wenzel Seifert an der [[Höhere Bundeslehranstalt und Bundesamt für Wein- und Obstbau|Höheren Bundeslehranstalt und Bundesamt für Wein- und Obstbau]] in [[Klosterneuburg]] bekannt war, brauchte es noch nahezu 40 Jahre zum tieferen Verständnis der biologischen Säureabbaus. |
|||
== Literatur == |
== Literatur == |
||
| Zeile 56: | Zeile 70: | ||
| ISBN = 2-10-007302-8 |
| ISBN = 2-10-007302-8 |
||
}} |
}} |
||
== Einzelnachweise == |
|||
<references /> |
|||
[[Kategorie:Önologie]] |
[[Kategorie:Önologie]] |
||
Version vom 10. Januar 2010, 17:44 Uhr
Die malolaktische Gärung tritt bei vielen heterofermentativen Milchsäurebakterien auf und spielt bei der Wein-, Fruchsaft- und Champagnerherstellung eine Rolle. Sie wird auch als biologischer Säureabbau bezeichnet. Die malolaktische Gärung ist eine sekündäre Gärung, die als Folge den Abbau von Säure im Medium hat. Sie folgt einer primären, Alkohol erzeugenden Gärung. Bei der malolaktischen Gärung decarboxylieren bestimmte Milchsäurebakterien die Dicarbonsäure L-Malat (= deprotonierte From der L-Äpfelsäure) unter Energiegewinnung zur schwächeren Monocarbonsäure L-Lactat (= deprotonierte Form der L-Milchsäure).
Der durch diese Gärung resultierende biologische Säureabbau führt bei der Weinherstellung zu einem harmonischen und ausgewogeneren Geschmacksbild - ein Effekt, der sich qualitätssteigernd auswirkt, der aber auch Risiken birgt: Säurearme Weine sind weniger haltbar, weniger „spritzig“ und wirken nicht so frisch.
Vorkommen
Die malolaktische Gärung findet in vielen Mikroorganismen statt, die zur Energiegewinnung eine heterofermentative Gärung betreiben. Für die Weinherstellung ist Oenococcus oeni (alte Bezeichnung Leuconostoc oenos) bedeutsam, ferner Lactobacillus spp. (z. B. Lactobacillus plantarum) and Pediococcus spp.[1]
Auch Hefen können am Ende der alkoholischen Gärung malolaktische Gärung betreiben.
Biochemie
Prozess
Bei der malolaktischen Gärung wird der Decarboxylierung L-Malats zu L-Lactat katalysiert. Abhängig vom pH-Wert des Mediums kann Malat bzw. Lactat auch protoniert vorliegen
Bei dieser Reaktion wird mit jedem Gramm abgebauter Äpfelsäure der Gesamtanteil der Säure im Wein um 0,4 g/LH2SO4 gesenkt.
| Vorher (g/LH2SO4) |
Nachher (g/LH2SO4) | |
| Äpfelsäure | 3.2 | 0.5 |
| Milchsäure | 0.12 | 1.8 |
| Säure gesamt | 4.9 | 3.8 |
| Flüchtige Säure | 0.21 | 0.28 |
| Nichtflüchtige Säure | 4.7 | 3.6 |
Energiegewinnung
Unter Standardbedingungen wird bei der Decarboxylierungsreaktion Energie freigesetzt. Dieser Wert ist vom pH-Wert abhängig. Bei pH 7 werden −26,5 kJ·mol−1, bei einem pH-Wert von 5,7 werden −33,9 kJ·mol−1 freigesetzt.[2] In Weinen kann der pH-Wert durchaus bei 3,5 liegen, dann werden unter Standardbedingungen −46,5 kJ·mol−1 erzeugt. Es ist jedoch anzumerken, dass unter phyiologischen Bedingungen Malat, Lactat und CO2 nicht in einer Konzentration von 1 M vorliegen und während des Prozesses ständig Malat verbraucht wird und Lactat erzeugt wird. Daher ist der Energiegewinn unter physiologischen Bedingungen geringer.[3]
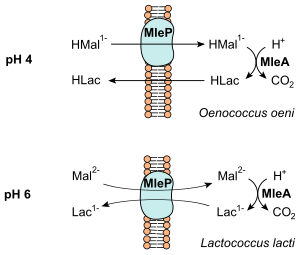
Die bei der Decarboxylierung freigesetzte Energie wird in Form eines Chemiosmotischen Mechanismus konserviert (vgl. Abbildung).[4] Bei O. oeni, der bei einem pH-Wert von 4 wächst, wird einfach protoniertes Malat (HMal1−) durch einen membranständigen Carrier (MleP) in die Zelle gebracht. Dieses wird zu Lactat decarboxyliert, welches bei pH 4 protoniert (HLac) vorliegt. Der Ausstrom aus der Zelle bei HLac erfolgt ohne Carrier. Bei Lactococcus lactis wächst unter höheren pH-Werten. Dort wird Malat (Mal2−) mit Lactat (Lac1−) durch einen Antiporter ausgetauscht.
In beiden Fällen wird im Netto eine (negative) Ladung per Austausch transportiert, was zu einer Energetisierung der Membran führt. Darüber hinaus wird im Zuge der Decarboxylierung ein Proton verbraucht, so dass auch ein Protonengradient aufgebaut werden kann. Beide Prozesse führend daher zu einem Aufbau einem elektrochemischen Gradienten (proton motive force). Er wird von den Bakterien zur Aufrechterhaltung des pH-Wertes und zur Aufnahme von Nährstoffen genutzt. Jedoch reicht die bei malolaktischen Gärung freigesetzte Energie nicht als einzige Energiequelle aus, so dass die heterofermentativen Milchsäurebakterien weiterhin auf die Vergärung von Pentosen bzw. Hexosen angewiesen sind.[4]
Geschichte
Obwohl die chemische Reaktion seit Anfang der 1920 Jahre durch Arbeiten von Wenzel Seifert an der Höheren Bundeslehranstalt und Bundesamt für Wein- und Obstbau in Klosterneuburg bekannt war, brauchte es noch nahezu 40 Jahre zum tieferen Verständnis der biologischen Säureabbaus.
Literatur
- Jancis Robinson: Das Oxford Weinlexikon. 1. Auflage. Gräfe und Unzer Verlag, München 2003, ISBN 3-7742-0914-6.
- Pascal Ribéreau-Gayon, Denis Dubourdieu, Bernard Donèche, Aline Lonvaud: Traité d'oenologie, Microbiologie du vin. Vinifications. 5. Auflage. Dunod, Éditions La Vigne, 2004, ISBN 2-10-007301-X.
- Pascal Ribéreau-Gayon, Denis Dubourdieu, Yves Glories, Alain Maujean: Traité d'oenologie, Chimie du vin. Stabilisation et traitements. 5. Auflage. Dunod, Éditions La Vigne, 2004, ISBN 2-10-007302-8.
Einzelnachweise
- ↑ Zaunmüller, T. et al. 2006: Variations in the energy metabolism of biotechnologically relevant heterofermentative lactic acid bacteria during growth on sugars and organic acids. In: Appl Microbiol Biotechnol. 72(3); 421–429; PMID 16826375; doi:10.1007/s00253-006-0514-3
- ↑ Kolb, S. et al. (1992): Energy conservation in malolactic fermentation by Lactobacillus plantarum and Lactobacillus sake. In: Arch Microbiol. 157(5); 457–463; PMID 1510572; doi:10.1007/BF00249105
- ↑ Olsen, EB. et al. (1991): Electrogenic L-malate transport by Lactobacillus plantarum: a basis for energy derivation from malolactic fermentation. In: J Bacteriol. 173(19); 6199–6206.; PMID 1917854; PDF (freier Volltextzugriff, engl.)
- ↑ a b Liu, SQ. (2002): A review: malolactic fermentation in wine - beyond deacidification. In: J Appl Microbiol. 92(4):589–601; PMID 11966898; PDF (freier Volltextzugriff, engl.)

