4-Azaphenothiazin
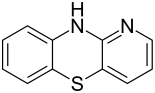
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| Allgemeines | ||||||||||
| Name | 4-Azaphenothiazin | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C11H8N2S | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 200,26 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
4-Azaphenothiazin zählt in der Chemie zur Stoffgruppe der Heterocyclen und ist ein Zwischenprodukt zur Synthese einer Vielzahl von Arzneistoffen.
Geschichte
Die erstmalige Synthese gelang im Jahre 1958 durch eine Smiles-Umlagerung mit anschließender Cyclisierung.[3]
Gewinnung und Darstellung
Durch Schmelzen von N-(Pyrid-2-yl)-anilin mit Schwefel in Gegenwart katalytischer Mengen Iod wird 4-Azaphenothiazin erhalten.[1] Alternativ kann 4-Azaphenothiazin auch ausgehend von 2-Chlorpyridin und 2-Aminothiophenol hergestellt werden.[4]
Eigenschaften
An der sekundären Aminogruppe (NH) kann 4-Azaphenothiazin durch Umsetzung mit Halogenalkanen im basischen Medium alkyliert werden. Die Umsetzung von 4-Azaphenothiazin mit Phosgen liefert 4-Azaphenothiazin-10-carbonsäurechlorid, das mit Alkoholen zu Urethanen, mit Thiolen zu Thiocarbamidsäureestern und Aminen zu Harnstoffderivaten reagiert.[5]
Verwendung
4-Azaphenothiazin dient als Edukt für die Arzneistoffe Prothipendyl (Dominal®), Isothipendyl (Andantol®) und Pipazetat (Selvigon® / Theratuss).[6][7]
Einzelnachweise
- ↑ a b W. Schuler, H. Klebe: 4-Azaphenothiazine und deren 10-Aminoalkyl-Derivate, in Liebigs Ann. 1962, 653, 172–180; doi:10.1002/jlac.19626530120.
- ↑ a b c Datenblatt 10H-PYRIDO(3,2-B)(1,4)BENZOTHIAZINE bei Sigma-Aldrich (PDF).
- ↑ H. L. Yale, F. Sowinski: 10-(Dialkylaminoalkyl)-pyrido[3,2-b][1,4]benzothiazine (1-Azaphenothiazine) and Related Compounds, in: J. Am. Chem. Soc. 1958, 80, 1651–1654; doi:10.1021/ja01540a035.
- ↑ B. Kutscher, H. R. Dieter, H.-G. Trömer, B. Bartz, J. Engel, A. Kleemann: Neue Synthese von 4-Azaphenothiazin, in: Liebigs Ann. 1995, 591–592; doi:10.1002/jlac.199519950381.
- ↑ W. Schuler, H. Klebe, A. von Schlichtegroll: Derivate der 4-Azaphenothiazin-10-carbonsäure, in: Liebigs Ann. 1964, 673, 102–112; doi:10.1002/jlac.19646730114.
- ↑ A. von Schlichtegroll, in: Arzneimittel-Forschung 1957, 7, 237.
- ↑ Wilhelm A. Schuler, Hans Klebe, Ansgar V. Schlichtegroll: Synthesen von 4-Aza-phenothiazinen, II. Derivate der 4-Aza-phenothiazin-10-carbonsäure. In: Justus Liebigs Annalen der Chemie. Band 673, Nr. 1, 4. Mai 1964, S. 102–112, doi:10.1002/jlac.19646730114 (PDF).
