Mannitolhexanitrat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
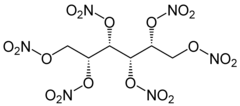
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Mannitolhexanitrat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H8N6O18 | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 452,16 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
1,604 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Mannitolhexanitrat oder auch Nitromannit ist eine chemische Verbindung aus der Gruppe der Salpetersäureester und ein selten gebrauchter Sprengstoff. Es kann sowohl als Initialsprengstoff als auch als Hauptladung verwendet werden. Aufgrund seiner geringen Stabilität wird es in Europa nicht verwendet, da man es durch andere stabilere Sprengstoffe ersetzen kann. Nur in den USA hat es eine gewisse Bedeutung als Sprengkapselfüllung erlangt. Es wird mit Ammoniumcarbonat stabilisiert und muss absolut säurefrei sein, da es sonst spontan detonieren kann.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Es wird durch die Veresterung von Mannitol mit Salpetersäure gewonnen. Hierzu wird Mannit in kalter konzentrierter Salpetersäure gelöst und danach mit konzentrierter Schwefelsäure ausgefällt.[2]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Mannitolhexanitrat bildet farblose kristalline Nadeln, die bei 112 bis 113 °C schmelzen.[2] Die Standardbildungsenthalpie ΔfH0solid beträgt −708,8 kJ·mol−1,[4] die Verbrennungsenthalpie ΔcH0solid −2936 kJ·mol−1.[4]
Explosionskenngrößen[Bearbeiten | Quelltext bearbeiten]
Mannitolhexanitrat ist ein explosionsgefährlicher Stoff. Er ist im Sprengstoffgesetz in der Liste der einheitlich explosionsgefährlichen Stoffe enthalten, für die das Gesetz in vollem Umfang gilt.[5] Wichtige Explosionskennzahlen sind:
- Explosionswärme: 5928 kJ·kg−1 (H2O (g)).[2]
- Detonationsgeschwindigkeit: 8260 m·s−1 bei der Dichte von 1,73 g·cm−3[2]
- Normalgasvolumen: 755 l·kg−1.[2]
- Spezifische Energie: 1087 kJ·kg−1[2]
- Verpuffungspunkt: 185 °C[2]
- Bleiblockausbauchung: 51 cm3·g−1[2]
- Schlagempfindlichkeit: 0,8 N·m[2], 1 N·m[6]
- Reibempfindlichkeit: 30 N[6]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Neben seiner Anwendung als Sprengstoff dient es in der Medizin als gefäßerweiterndes Mittel bei Angina pectoris.[1]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Eintrag zu Mannithexanitrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ a b c d e f g h i j k J. Köhler, R. Meyer, A. Homburg: Explosivstoffe. 10., vollst. überarb. Auflage. Wiley-VCH, Weinheim 2008, ISBN 978-3-527-32009-7.
- ↑ Eintrag zu Mannitol hexanitrate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b G. R. Handrick: Report of the study of pure explosive compounds. Part IV: Calculation of heat of combustion of organic compounds from structural features and calculation of power of high explosives. In: Report C-58247 for the Office of the Chief of Ordnance, contract DA-19-020-ORD-47 by the Arthur D. Little, Inc. Cambridge, MA, 1956, S. 467–573.
- ↑ L. Roth, U. Weller: Gefährliche Chemische Reaktionen. ecomed Verlag, 64. Ergänzungslieferung, 8/2011.
- ↑ a b Klapötke, T.M.: Energetic Materials Encyclopedia, de Gruyter, Berlin/Boston 2018, ISBN 978-3-11-044139-0, S. 281.
