Natriummetavanadat
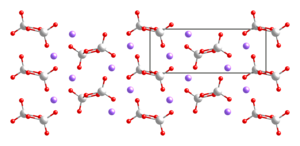
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| _ Na+ _ V5+ _ O2− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Natriummetavanadat | ||||||||||||||||||
| Verhältnisformel | NaVO3 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 121,93 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
2,85 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Wasser (210 g·l−1 bei 25 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Natriummetavanadat ist eine chemische Verbindung des Natriums mit Vanadium und Sauerstoff aus der Gruppe der Vanadate.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Natriummetavanadat kommt natürlich in dem Mineral Metamunirit vor.[5]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Natriummetavanadat kann durch Reaktion von Natriumhydroxid mit Vanadium(V)-oxid hergestellt werden.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]

Natriummetavanadat kommt in zwei verschiedenen Kristallstrukturen (alpha und beta) vor. Dabei ist bei Raumtemperatur die orthorhombische β-Struktur stabiler, während bei höheren Temperaturen die monokline α-Phase vorliegt. Zudem ist ein Dihydrat bekannt, dieses kristallisiert unterhalb von 307,75 K aus wässriger Lösung aus, geht an der Luft aber schnell unter Kristallwasserabgabe in β-Natriummetavanadat über.[6]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Natriummetavanadat wird als Zwischenprodukt bei der Gewinnung von Vanadium aus entsprechenden Erzen[7] sowie als Bestandteil von Korrosionsschutzmitteln, als Katalysator und in der Farb-, Glas- und Keramikindustrie verwendet[2].
Siehe auch[Bearbeiten | Quelltext bearbeiten]
- Natriumorthovanadat Na3VO4
Literatur[Bearbeiten | Quelltext bearbeiten]
- Catherine E. Housecroft, A. G. Sharpe: Inorganic chemistry. 3. Auflage. Pearson Education, 2007, ISBN 978-0-13-175553-6; S. 697 (eingeschränkte Vorschau in der Google-Buchsuche).
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c Datenblatt Sodium Metavanadate bei Fisher Scientific , abgerufen am 13. Februar 2014 (PDF).
- ↑ a b Datenblatt bei GfE Metalle und Materialien GmbH
- ↑ a b Eintrag zu Natriummetavanadat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Juli 2016. (JavaScript erforderlich)
- ↑ Datenblatt Sodium metavanadate bei Sigma-Aldrich, abgerufen am 14. April 2011 (PDF).
- ↑ Bericht vom U.S. Geological Survey (englisch) (PDF; 275 kB)
- ↑ K. Kato und E. Takayama: Das Entwässerungsverhalten des Natriummetavanadatdihydrats und die Kristallstruktur des β-Natriummetavanadats. In: Acta Cryst., 1984, B40, S. 102–105, doi:10.1107/S0108768184001828.
- ↑ Bericht über Vanadium bei Wissenschaft Online



