Pterin
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|

| |||||||
| Allgemeines | |||||||
| Name | Pterin | ||||||
| Andere Namen |
2-Amino-3H-pteridin-4-on | ||||||
| Summenformel | C6H5N5O | ||||||
| Kurzbeschreibung |
beigefarben bis gelber kristalliner Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 163,14 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Schmelzpunkt | |||||||
| pKS-Wert |
| ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Pterin ist ein Derivat des Pteridins und damit eine heterocyclische Verbindung. Sie tritt als Strukturelement in vielen Biomolekülen auf, so z. B. in verschiedenen Farbpigmenten von Insekten wie Xanthopterin, im Cofaktor Biopterin oder im Vitamin Folsäure.
Eigenschaften
Pterin bildet hellgelbe Kristalle. Beim Erhitzen zersetzt es sich ohne zu schmelzen. Die Verbindung zeigt zwei Säurekonstanten mit pKs1 2,20 und pKs2 7,86 (in Wasser bei 20 °C).[3] Die Löslichkeit in Wasser beträgt 0,175 g*l-1.[4]
Die Verbindung kann in zwei tautomeren Strukturen auftreten.[5]

Synthese
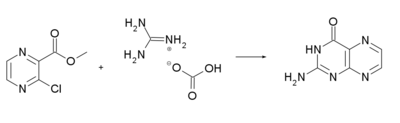
Die Herstellung von Pterin gelingt durch die Umsetzung von 3-Chlorpyrazin-carbonsäuremethylester mit Guanidiniumhydrogencarbonat.[6]
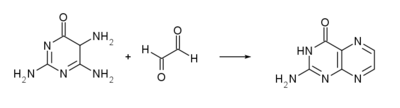
Eine andere Synthese geht von 2,4,5-Triamino-6-hydroxypyrimidin aus, das mit Glyoxal umgesetzt wird.[7]
Einzelnachweise
- ↑ a b Vorlage:Acros.
- ↑ Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.5. Georg Thieme Verlag KG, Stuttgart 2009.
- ↑ a b Pfleiderer, W.; Liedek, E.; Lohrmann, R.; Rukwied, M.: Pteridine, X. Zur Struktur des Pterins in Chem. Ber. 93 (1960) 2015–2022. doi:10.1002/cber.19600930916.
- ↑ Albert et. al.: J. Chem. Soc. 1952, 4219–4220.
- ↑ Jaramillo, P.; Coutinho, K.; Canuto, S.: Solvent Effects in Chemical Processes. Water-Assisted Proton Transfer Reaction of Pterin in Aqueous Environment in J. Phys. Chem. A 113 (2009) 12485–12495. doi:10.1021/jp903638n.
- ↑ Wood, D.: J. Chem. Soc. 1955, 1379–1380.
- ↑ Movat et. al.: J. Amer. Chem. Soc. 70 (1948) 14.