Anisaldehyd
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
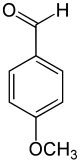
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Anisaldehyd | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H8O2 | |||||||||||||||
| Kurzbeschreibung |
gelbliche Flüssigkeit mit charakteristischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 136,15 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,12 g·cm−3 (25 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
247–249 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (2 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Brechungsindex |
1,5731[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Anisaldehyd ist eine aromatische Verbindung, leitet sich strukturell von Benzaldehyd bzw. Anisol ab und gehört zur Stoffgruppe der Methoxybenzaldehyde.
Vorkommen
In der Natur kommt Anisaldehyd in Anis, Fenchel und anderen ätherischen Ölen vor. Er wird in Pflanzen über den Shikimisäureweg synthetisiert.
Gewinnung und Darstellung
Anisaldehyd kann durch Oxidation (z. B. durch Salpetersäure oder Chromsäure) von Anethol oder 4-Methoxytoluol oder aus Anisol durch eine Vilsmeier-Reaktion gewonnen werden.
Eigenschaften
Durch Umsetzung von Anisaldehyd mit Oxidationsmitteln (z. B. Fehling- oder Silberspiegelprobe) lässt sich Anissäure (p-Methoxybenzoesäure) darstellen.
Verwendung
Anisaldehyd wird als Zwischenprodukt zur Synthese von Arzneistoffen, Duftstoffen und anderer Chemikalien verwendet.
Anisaldehyd dient in der Dünnschichtchromatographie in Form eines Sprühreagenz zum Nachweis von diversen Naturstoffklassen (insbesondere Terpenderivaten). Dazu werden 0,5 mL Anisaldehyd mit 10 mL Eisessig, 85 mL Methanol und 5 mL konz. Schwefelsäure in der angegebenen Reihenfolge gemischt. Nach dem Aufsprühen dieser Lösung auf die DC-Platte und anschließendem Erhitzen der Platte auf ca. 110 °C für 5 bis 10 Minuten färben sich die entsprechenden Zonen im Tageslicht charakteristisch.[3] Dieses Reagenz wird unter der Bezeichnung Anisaldehyd-Reagenz R im Europäischen Arzneibuch (Ph. Eur.) gelistet.[4] Das Reagenz ist nur für eine begrenzte Zeit haltbar. Beim Auftreten einer Rot-Violettfärbung ist es zu verwerfen.[3]
Sicherheitshinweise
Die Dämpfe von Anisaldehyd können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 116 °C, Zündtemperatur 220 °C)[1] bilden.
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu CAS-Nr. 123-11-5 in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b Egon Stahl, Werner Schild: Isolierung und Charakterisierung von Naturstoffen. 1. Auflage. Gustav Fischer Verlag, Stuttgart/New York 1986, ISBN 3-437-30511-5, S. 173.
- ↑ Europäisches Arzneibuch. 4.00 Auflage. Band 1. Deutscher Apotheker Verlag/Govi-Verlag – Pharmazeutischer Verlag GmbH, Stuttgart/Eschborn 2002, ISBN 3-7692-2947-9, S. 384.