Dimroth-Umlagerung

Als Dimroth-Umlagerung wird eine Umlagerungsreaktion von exo- und endo-cyclischen Heteroatomen in heterocyclischen Ringen bezeichnet. Der Begriff wurde in den 1960er Jahren zu einer Namensreaktion der organischen Chemie. Exo- und endo-cyclische Heteroatome (zumeist Stickstoffatome) wechseln hierbei ihre Position. Die Reaktion wurde zum ersten Mal im Jahr 1909 von dem deutschen Chemiker Otto Dimroth (1872–1940) beobachtet und publiziert.[1][2][3]
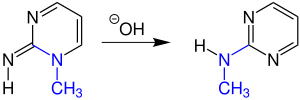
Auch 1H-1,2,3-Triazole können die Dimroth-Umlagerung eingehen.[4] Meist läuft die Reaktion bei sechsgliedrigen Ringen ab, jedoch ist sie auch an fünfgliedrigen Ringen durchführbar.[5]
Mechanismus[Bearbeiten | Quelltext bearbeiten]
Unter basischen Bedingungen reagiert ein Pyrimidinderivat zu einem umgelagerten Pyrimidinderivat. Im folgenden Beispiel hat dabei ein Stickstoffatom (genauer: NR) aus dem Ring die Position mit dem Stickstoffatom der Imingruppe gewechselt:

Das Hydroxidionen greift am Kohlenstoffatom in Position 6 des Pyrimidin-Derivats 1 an. Dabei bildet sich das Anion 2 welches zum Enol-Intermediat 3 umlagert. Durch einen [1,7]-Protonentransfer entsteht das Alkoholat 4, welches durch Elektronenumlagerung eine Carbonylgruppe ausbildet. Über eine Zwischenstufe bildet sich dann das Imidamid-Intermediat 5. Aus 5 kann sich durch erneute Elektronenpaarumlagerung dann das Amidion 6 bilden, das nun mit dem negativ geladenen Stickstoffatom einen nucleophilen Angriff auf das Kohlenstoffatom der Carbonylgruppe durchführt, wodurch sich das heterocyclische Alkoholat-Intermediat 7 bildet. Das Alkoholat 7 wird durch Wasser zum Alkohol 8 protoniert. Durch Wasserabspaltung entsteht schließlich das Pyrimidin-Derivat 9.
Beispiele[Bearbeiten | Quelltext bearbeiten]
Mit Hilfe eines Beispiels soll hier nun die breite Anwendbarkeit der Dimroth-Umlagerung verdeutlicht werden.
Durch die Dimroth-Umlagerung können auch komplexere Reste ihre Position im Molekül verändern. Exemplarisch soll dies hier anhand eines Pyrimidin-Derivates gezeigt werden, an welchem ein chlorierter Phenylrest umgelagert wird:[6]

Auch 1,2,3-Triazole können, wie bereits weiter oben erwähnt eine Dimroth-Umlagerung eingehen. Dies ist im folgenden Beispiel dargestellt. Ar bezeichnet hierbei einen Arylrest:

Die Triazole müssen eine Amino-Gruppe in der 5-Position tragen. Nach der Ringöffnung zu einer Diazo-Zwischenstufe und einer C-N-Bindungsdrehung wird ein umgelagertes Triazol erhalten.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Eugene Lieber, Tai Siang Chao, C. N. Ramachandra Rao: 1,4-Diphenyl-5-amino-1,2,3-triazole AND 4-Phenyl-5-anilino-1,2,3-triazole In: Organic Syntheses. 37, 1957, S. 26, doi:10.15227/orgsyn.037.0026; Coll. Vol. 4, 1963, S. 380 (PDF).
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Otto Dimroth: Ueber intramolekulare Umlagerungen. Umlagerungen in der Reihe des 1, 2, 3-Triazols. In: Justus Liebigs Annalen der Chemie. 364, Nr. 2, 1909, S. 183–226, doi:10.1002/jlac.19093640204.
- ↑ Otto Dimroth, Walter Michaelis: Intramolekulare Umlagerung der 5-Amino-1,2,3-triazole. In: Justus Liebigs Annalen der Chemie. 459, Nr. 1, 1927, S. 39–46, doi:10.1002/jlac.19274590104.
- ↑ Otto Dimroth: Ueber eine Synthese von Derivaten des 1.2.3-Triazols. In: Berichte der deutschen chemischen Gesellschaft. 35, Nr. 1, 1902, S. 1029–1038, doi:10.1002/cber.190203501171.
- ↑ a b Z. Wang: Comprehensive Organic Name Reactions and Reagents, 3 Volume Set. Volume 1, John Wiley & Sons, Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 906.
- ↑ Z. Wang: Comprehensive Organic Name Reactions and Reagents, 3 Volume Set. Volume 1, John Wiley & Sons, Hoboken, New Jersey 2009, ISBN 978-0-471-70450-8, S. 905.
- ↑ Reto W. Fischer and Marian Misun: Large-Scale Synthesis of a Pyrrolo[2,3-d]pyrimidine via Dakin–West Reaction and Dimroth Rearrangement. In: Organic Process Research & Development. Band 5, Nr. 6, 2001, S. 581–586, doi:10.1021/op010041v.