Amide
Amide sind stickstoffhaltige chemische Verbindungen, zu denen einerseits die Stoffgruppe der kovalenten und meist organischen Säureamide und andererseits die Stoffgruppe der ionischen und überwiegend anorganischen Metallamide zählt.
Formal betrachtet handelt es sich bei den Säureamiden um Kondensationsprodukte von Oxosäuren mit Ammoniak oder Aminen, wobei die größte Bedeutung Carbonsäureamide und Sulfonsäureamide haben.[1]
| Allgemeine Struktur von Säureamiden (Beispiele): | |
|---|---|

|
|
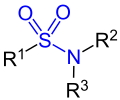
| Carbonsäureamide | Sulfonsäureamide |
| R1=Alkyl-, Arylgruppe, R2, R3=Alkyl-, Arylgruppe, Wasserstoff | |
Metallamide leiten sich von Ammoniak bzw. primären oder sekundären Aminen ab, bei denen ein Wasserstoffatom durch ein Metallatom ersetzt ist. Dabei handelt es sich meist um ein Alkalimetall wie Lithium oder Natrium.[2]
| Allgemeine Struktur von Metallamiden: |
|---|

|
| R1, R2 = Alkyl-, Arylgruppe, Wasserstoff |
Säureamide
[Bearbeiten | Quelltext bearbeiten]Einfache Säureamide
[Bearbeiten | Quelltext bearbeiten]Die einfachsten Vertreter der Säureamide sind Amidosulfonsäure und Sulfuryldiamid als Mono- und Diamid der Schwefelsäure, Nitrylamid als Amid der Salpetersäure, die Carbamidsäure und Harnstoff als Mono- und Diamid der Kohlensäure, sowie Phosphoramidsäure,[3] Phosphordiamidsäure[4] und Phosphorsäuretriamid[5] als Mono-, Di- und Triamid der Phosphorsäure.[6] Während der Harnstoff zu den organischen Verbindungen gezählt wird, sind die anderen Vertreter dieser einfachen Säureamide anorganische Verbindungen.
Carbonsäureamide
[Bearbeiten | Quelltext bearbeiten]Die wichtigste und umfangreichste Untergruppe der Säureamide sind die Carbonsäureamide die durch Umsetzung von Carbonsäuren oder Carbonsäurederivaten wie Carbonsäureestern und Carbonsäurechloriden mit Ammoniak oder Aminen hergestellt werden. Verbindungen mit mehreren Carbonsäureamidgruppen werden als Polyamide bezeichnet.[7] Natürlich vorkommende sind die Peptide und Proteine.
Cyclische Verbindungen mit einer Amidgruppe im Ring werden als Lactame bezeichnet.
Carbonsäureamide die eine zweite Acylgruppe am Stickstoffatom aufweisen gehören zur Stoffgruppe der Imide.
Sulfonsäureamide
[Bearbeiten | Quelltext bearbeiten]Sulfonsäureamide leiten sich von Sulfonsäuren ab, bei denen eine Hydroxygruppe durch eine Aminogruppe ersetzt ist. Die bedeutsamsten Sulfonsäureamide sind die Sulfonamide – Benzolsulfonsäureamide, die in ‘‘para‘‘-Stellung eine Aminogruppe enthalten. Diese Verbindungen besitzen eine bakteriostatische Wirkung. Durch Substitution eines der beiden Amid-Wasserstoffatome des einfachsten Vertreters Sulfanilamid durch einen organischen Rest, leiten sich alle pharmakologisch wirksamen Sulfonamide ab.[8]
Metallamide
[Bearbeiten | Quelltext bearbeiten]Anorganische Metallamide sind Derivate des Ammoniaks, bei denen ein Wasserstoffatom durch ein Metallatom ersetzt ist. Die wichtigsten Vertreter sind Natriumamid und Lithiumamid, die beide als starke Basen bei Eliminierung- und Kondensationsreaktionen eingesetzt werden.[2] Natriumamid erhält man durch Reaktion von Natrium mit flüssigem Ammoniak und ist beispielsweise großtechnisch bedeutsam bei der Synthese von Indigo.[9] Lithiumamid wird durch Erhitzen von Lithium im Ammoniak-Strom hergestellt.[10]
Organische Metallamide leiten sich von primären oder sekundären Aminen ab. So erhält man beispielsweise durch die Deprotonierung von wasserfreiem Diisopropylamin das Lithiumdiisopropylamid (LDA), welches in der organische Synthese häufig zur Erzeugung von Carbanionen eingesetzt wird.[11]
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu Amide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. Mai 2023.
- ↑ a b Eintrag zu Metallamide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. Mai 2023.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Phosphoramidsäure: CAS-Nr.: 2817-45-0, PubChem: 65107, ChemSpider: 58617, Wikidata: Q27098293.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Phosphordiamidsäure: CAS-Nr.: 10043-91-1, EG-Nr.: 233-145-5, ECHA-InfoCard: 100.030.119, PubChem: 165802, ChemSpider: 145304, Wikidata: Q27276706.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Phosphorsäuretriamid: CAS-Nr.: 13597-72-3, PubChem: 123317, ChemSpider: 109920, Wikidata: Q22693530.
- ↑ Eintrag zu Phosphoramide. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Juni 2023.
- ↑ M. D. Lechner, K. Gehrke, E. H. Nordmeier: Makromolekulare Chemie. Ein Lehrbuch für Chemiker, Physiker, Materialwissenschaftler und Verfahrenstechniker. 4. Auflage, Birkhäuser, Basel / Boston, Mass. / Berlin 2010, ISBN 978-3-7643-8890-4, S. 121–125.
- ↑ Bernd Schmidt, Jolanda Hermanns: Grundlagen der organischen Chemie. Begründet von Joachim Buddrus. 6. Auflage. De Gruyter, Berlin, Boston 2022, ISBN 978-3-11-070087-9, S. 538.
- ↑ Eintrag zu Natiumamid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Juni 2023.
- ↑ Eintrag zu Lithiumamid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Juni 2023.
- ↑ Eintrag zu Lithiumdiisopropylamid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 13. Juni 2023.


