Kupferselenit
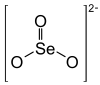
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
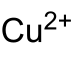 
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Kupferselenit | |||||||||||||||
| Andere Namen |
Kupfer(II)-selenit | |||||||||||||||
| Summenformel | CuSeO3 | |||||||||||||||
| Kurzbeschreibung |
blauer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 226,53 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||
| Dichte |
3,31 g·cm−3[2] | |||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Kupferselenit ist eine anorganische chemische Verbindung des Kupfers aus der Gruppe der Selenite.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Kupferselenit kommt natürlich in Form des Minerals Chalkomenit vor.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Kupferselenit kann durch Reaktion von Kupfernitrat mit Natriumselenitlösungen gewonnen werden.[4][5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Kupferselenit-Dihydrat[6] ist ein blauer Feststoff, der praktisch unlöslich in Wasser ist.[2] Die Verbindung gibt bei Temperaturen über 265 °C ihr Kristallwasser ab und zersetzt sich ab 460 °C.[1] Er besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/n (Raumgruppen-Nr. 14, Stellung 2) oder eine orthorhombische Kristallstruktur mit der Raumgruppe Pcab (Raumgruppen-Nr. 61, Stellung 2).[7][8] Das Anhydrat ist ferromagnetisch.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Dale L. Perry: Handbook of Inorganic Compounds. CRC Press, 2016, ISBN 978-1-4398-1462-8, S. 151 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d e f Datenblatt Copper(II) selenite dihydrate, bei Sigma-Aldrich, abgerufen am 25. April 2019 (PDF).
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag Selenverbindungen mit Ausnahme von Cadmiumsulfoselenid, soweit in diesem Anhang nicht gesondert aufgeführt im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 11. Januar 2023. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Marina V. Charykova, Maxim I. Lelet u. a.: A calorimetric and thermodynamic investigation of the synthetic analogue of chalcomenite, CuSeO3-2H2O. In: European Journal of Mineralogy. 29, 2017, S. 269, doi:10.1127/ejm/2017/0029-2595.
- ↑ Chemical Thermodynamics of Selenium. Elsevier, 2005, ISBN 978-0-08-045751-2, S. 294 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Kupferselenit-Dihydrat: CAS-Nr.: 15168-20-4, EG-Nr.: 683-639-3, ECHA-InfoCard: 100.209.144, PubChem: 160923, ChemSpider: 21241696, Wikidata: Q15627472.
- ↑ S. Lee, W.-J. Lee u. a.: Anomalous spin dynamics in the coupled spin tetramer system. In: Physical Review B. 95, 2017, doi:10.1103/PhysRevB.95.054405.
- ↑ F. C. Hawthorne, T. S. Ercit, L. A. Groat: Structures of zinc selenite and copper selenite. In: Acta Crystallographica Section C Crystal Structure Communications. 42, S. 1285, doi:10.1107/S0108270186092545.
- ↑ Kay Kohn, Katsuhiko Inoue u. a.: Crystal chemistry of MSeO3 and MTeO3 (M = Mg, Mn, Co, Ni, Cu, and Zn). In: Journal of Solid State Chemistry. 18, 1976, S. 27, doi:10.1016/0022-4596(76)90075-X.


