Natriumaurothiomalat
| Strukturformel | |||||||||
|---|---|---|---|---|---|---|---|---|---|
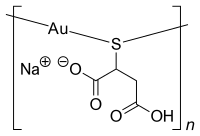
| |||||||||
| Allgemeines | |||||||||
| Name | Natriumaurothiomalat | ||||||||
| Andere Namen |
| ||||||||
| CAS-Nummer | 12244-57-4 | ||||||||
| Monomer | Gold(I)-thiomalat | ||||||||
| Summenformel der Wiederholeinheit | C4H4AuNaO4S | ||||||||
| Molare Masse der Wiederholeinheit | 344,10 g·mol−1 | ||||||||
| PubChem | 4479093 | ||||||||
| ATC-Code | |||||||||
| Arzneistoffangaben | |||||||||
| Wirkstoffklasse |
Goldpräparat | ||||||||
| Eigenschaften | |||||||||
| Aggregatzustand |
fest | ||||||||
| Löslichkeit |
sehr gut löslich in Wasser[1]
| ||||||||
| Sicherheitshinweise | |||||||||
| |||||||||
| Toxikologische Daten | |||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||
Natriumaurothiomalat (auch bekannt als Goldnatriumthiomalat) ist eine organometallische Verbindung, die zur Behandlung von chronischer Polyarthritis verwendet wird.
Aufgrund des hohen Preises und der zum Teil erheblichen Nebenwirkungen – etwa 50 % der (intramuskulär erfolgenden) Behandlungen werden aufgrund der Nebenwirkungen abgebrochen – wird es aber zunehmend von anderen Medikamenten verdrängt.
Mögliche Nebenwirkungen sind unter anderem Allergische Reaktionen, Übelkeit, Durchfall, Juckreiz und Ausschläge.[3]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Die Synthese der Verbindung erfolgt durch Umsetzung von Gold(I)-iodid mit Mercaptobernsteinsäure in Gegenwart von Natronlauge.[4][5]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Natriumaurothiomalat ist eine hellgelbe, kristalline Verbindung.[6] In fester Phase konnte resultierend aus Einkristalluntersuchungen eine polymere Struktur aus koordinierten Au-S-Einheiten nachgewiesen werden, die sich in einer komplexen Doppelhelixstruktur mit einer Ganghöhe aus vier Au-S-Einheiten anordnet.[7] Es wird ein tetragonales Kristallgitter gebildet. Die berechnete Dichte beträgt 3,402 g·cm−3.[7] In wässriger Lösung zerfällt die Struktur in oligomere Teilstrukturen mit 6 bis 14 Au-S-Einheiten.[8]
Handelsnamen[Bearbeiten | Quelltext bearbeiten]
Natriumaurothiomalat ist in Deutschland und der Schweiz unter dem Namen Tauredon im Handel erhältlich.
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b Datenblatt Sodium aurothiomalate(I), 99.9% (metals basis) bei Alfa Aesar, abgerufen am 8. Dezember 2019 (Seite nicht mehr abrufbar).
- ↑ a b c Datenblatt Sodium aurothiomalate hydrate bei Sigma-Aldrich, abgerufen am 12. April 2011 (PDF).
- ↑ gold sodium thiomalate. Drugs.com
- ↑ A. Kleemann, J. Engel, B. Kutscher, D. Reichert: Pharmaceutical Substances - Synthesis, Patents, Applications. 4. Auflage. Thieme 2001, ISBN 3-13-115134-X.
- ↑ Patent US 1 994 213 (Rhone-Poulenc 1935).
- ↑ W.F. Kean, C.J.L. Lock, D. Singal, Y.B. Kassam, H. Howard-Lock, J. Rischke: Biological action of colorless and yellow solutions of gold sodium thiomalate on thrombin activity and the mixed lymphocyte reaction. In: J Pharm Sci. 77 (1988), S. 1033–1036, doi:10.1002/jps.2600771209.
- ↑ a b R. Bau: Crystal Structure of the Antiarthritic Drug Gold Thiomalate (Myochrysine): A Double-Helical Geometry in the Solid State. In: J. Am. Chem. Soc. 120 (1998), S. 9380–9381, doi:10.1021/ja9819763.
- ↑ C. F. Shaw III, N.A. Schaeffer, R.C. Elder, M.K. Eidsness, J.M. Trooster, G.H. M. Calis: Bovine serum albumin-gold thiomalate complex: gold-197 Moessbauer, EXAFS and XANES, electrophoresis, sulfur-35 radiotracer, and fluorescent probe competition studies. In: J. Am. Chem. Soc. 106 (1984), S. 3511–3521, doi:10.1021/ja00324a019.