Vinylsulfonfarbstoffe

(R = Alkyl- oder Arylrest)
Vinylsulfonfarbstoffe sind Reaktivfarbstoffe, die als Reaktivgruppe (Reaktivanker[1]) eine Vinylsulfongruppe (VS-Gruppe) besitzen. Aufgrund der relativ hohen Reaktivität der Vinylsulfongruppe gegenüber Wasser (Restfeuchte, Luftfeuchtigkeit), liegt sie in vielen Handelsprodukten in geschützter Form vor. Dabei ist eine Ethylsulfonylgruppe mit einer Abgangsgruppe substituiert. Beim Färbeprozess unter alkalischen Bedingungen wird die VS-Gruppe durch eine Eliminierungsreaktion freigesetzt:
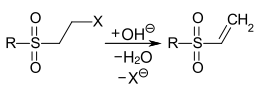
Erzeugung der Vinylsulfon-Gruppe durch alkalische Eliminierung.
R = Alkyl- oder Arylrest, X = –OSO3H, –Cl
Chemische Struktur[Bearbeiten | Quelltext bearbeiten]
Der Vinylsulfon-Reaktivanker wird in aller Regel über ein aromatisches oder aliphatisches Amin in den Reaktivfarbstoff eingeführt.

(4-[2-(Sulfooxy)ethylsulfonyl]anilin)
Das älteste und gängigste Zwischenprodukt ist der Parabaseester, ein mit einer [2-(Sulfooxy)ethyl]sulfonyl-Gruppe substituiertes Anilin. Parabaseester kann als Diazokomponente bei der Herstellung von Azofarbstoffen verwendet werden.[2] Eine weitere Reaktionsmöglichkeit ist die Kondensationsreaktion von Parabaseester mit einem Chlor- oder Fluortriazin-Rest, der wiederum über eine weitere Aminogruppe mit einem beliebigen Chromophor verbunden ist.
Variationsmöglichkeiten ergeben sich durch weitere Substituenten am aromatischen Ring – meist Hydroxy-, Methyl- oder Methoxygruppen, bzw. durch die Stellung der Amino- zur VS-Gruppe. Neben der para-substituierten Verbindung werden auch meta- und orthosubstituierten Vinylsulfonaniline verwendet.[3]

Wird die VS-Gruppe über ein primäres oder sekundäres aliphatisches Amin eingeführt, so erfolgt dies ebenfalls durch Kondensation mit einer Halogentriazin-Verbindung. Ein Beispiel ist das 2-[2-(2-Chlorethylsulfonyl)ethoxy]ethanamin, das bei bifunktionellen Reaktivfarbstoffen in Kombination mit einem Monofluor- oder Monochlortriazin-Anker Verwendung findet.[4]
Färbeprozess[Bearbeiten | Quelltext bearbeiten]
Die Vinylsulfongruppe reagiert mit den nukleophilen funktionellen Gruppen der Fasern im Sinne einer Michael-Addition unter Bildung einer kovalenten Etherbindung:
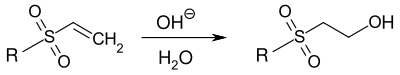
Eine unerwünschte Nebenreaktion beim Färbeprozess ist die Umsetzung der VS-Gruppe zur 2-(Hydroxy)ethylsulfonyl-Gruppe:[5]
Der unreaktive Farbstoff muss bei der Nachbehandlung der Färbung ausgewaschen werden.
Geschichte[Bearbeiten | Quelltext bearbeiten]
Die ersten Farbstoffe mit einer [2-(Sulfooxy)ethyl]sulfonyl-Gruppe wurden 1949 von den damaligen Farbwerken Hoechst patentiert[2] und in den Folgejahren als Wollfarbstoffe unter dem Markennamen Remalan, bzw. als Baumwollfarbstoffe unter der Markenbezeichnung Remazol vermarktet. Ab den frühen 1980er wurden Reaktivfarbstoffe, die neben der VS-Reaktivgruppe einen weiteren Monochlortriazinanker aufweisen durch die Farbstoffhersteller Sumitomo (Markenname Sumifix Supra) und Hoechst AG produziert. 1988 wurden von der Ciba-Geigy Doppelankerfarbstoffe mit der Kombination einer VS-Reaktivgruppe mit einer Monofluortriazin-Reaktivgruppe unter der Markenbezeichnung Cibacron in den Markt eingeführt.[6]
Beispiele[Bearbeiten | Quelltext bearbeiten]
Reaktivfarbstoffe mit einem Vinylsulfon-Reaktivanker
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu Reaktivanker. In: Römpp Online. Georg Thieme Verlag, abgerufen am 4. April 2019.
- ↑ a b Patent DE965902: Verfahren zum Fixieren wasserloeslicher organischer Verbindungen auf Unterlagen faseriger Struktur. Angemeldet am 19. Juli 1949, veröffentlicht am 19. September 1957, Anmelder: Hoechst AG, Erfinder: Johannes Heyna, Willy Schumacher.
- ↑ E. Siegel: Reactive Groups. In: K. Venkataraman (Hrsg.): The Chemistry of Synthetic Dyes. Band VI. Academic Press, New York, London 1972, S. 36 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Patent EP0775731: Reactive dyestuffs, process for their preparation and use thereof. Veröffentlicht am 28. Mai 1997, Anmelder: Ciba Geigy, Erfinder: Urs Lehmann, Marcel Frick.
- ↑ Die Reaktion der VS-Reaktivfarbstoffe mit Wasser wird in der Literatur auch als "Hydrolyse" bezeichnet, siehe:I. D. Rattee: Reactive Dyes – Physicochemical Aspects of Dye Fixation and Dye-Fibre Bond Hydrolysis. In: K. Venkataraman (Hrsg.): The Chemistry of Synthetic Dyes. Band VIII. Academic Press, New York, London 1978, ISBN 0-12-717008-1, S. 2 ff.
- ↑ Klaus Hunger (Hrsg.): Industrial Dyes: Chemistry, Properties, Applications. WILEY-VCH Verlag, Weinheim 2003, ISBN 978-3-662-01950-4, S. 113, 117–118 (eingeschränkte Vorschau in der Google-Buchsuche).