Yttriumoxid
Zur Navigation springen
Zur Suche springen
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
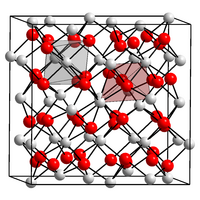
| ||||||||||||||||
| _ Y3+ _ O2− | ||||||||||||||||
| Kristallsystem |
kubisch | |||||||||||||||
| Raumgruppe |
Ia3 (Nr. 206) | |||||||||||||||
| Gitterparameter |
a = 926,84 pm | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Yttriumoxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Y2O3 | |||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 225,81 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
5,01 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
4300 °C[1] | |||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Brechungsindex |
1,930[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Yttriumoxid ist eine chemische Verbindung, genauer das Oxid von Yttrium. Es ist thermodynamisch sehr stabil und beständig gegenüber vielen reaktiven Metallschmelzen wie Titan oder Uran.
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Yttriumoxid kommt natürlich als Bestandteil in verschiedenen Yttriummineralen (Samarskit, Yttrobetafit) vor.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Yttriumoxid wird technisch durch Verglühen von z. B. Yttriumoxalat an der Luft gewonnen.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Yttriumoxid hat einen Brechungsindex von 1,930[3] und eine kubische Kristallstruktur im C-Oxid-Typ der Lanthanoide (Raumgruppe Ia3 (Raumgruppen-Nr. 206), Gitterparameter a = 10,12 Å).[4]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Yttriumoxid wird verwendet:
- als Verbindung für hochtemperaturfeste Anwendungen (z. B. als Beschichtungsmaterial für Graphit in der Kerntechnik[5])
- als Sinterhilfsmittel für keramische Materialien
- zur Stabilisierung von Zirconium(IV)-oxid eingesetzt (z. B. für Lambda-Sonden[6] oder in der Dentaltechnik[7])
- Verdünnungsmittel von Uranoxid für Brennstäbe (bildet mit Uranoxid eine feste Lösung)
- zur Gewinnung von Yttrium und anderen Yttriumverbindungen
- für optische Beschichtungen[8]
- als Ausgangsstoff für Hochtemperatursupraleiter (YBCO)
- als Ausgangsstoff für (rote) Luminophore für Röhrenbildschirme
- zusammen mit Thoriumdioxid zur Herstellung von IR- und UV-Licht durchlässigem Glas
- YInMn-Blau ist ein Mischoxid aus Yttrium-, Indium- und Manganoxiden, das ein sehr reines und brillantes Blau zeigt
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f Eintrag zu Yttrium(III)-oxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 19. Dezember 2019. (JavaScript erforderlich)
- ↑ Yttrium Oxide (AmericanElements)
- ↑ a b David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Index of Refraction of Inorganic Crystals, S. 10-248.
- ↑ M. Marezio: Refinement of the crystal structure of In2O3 at two wavelengths, in: Acta Cryst, 1966, 20, S. 723–728; doi:10.1107/S0365110X66001749.
- ↑ Ausfuhrliste 110. ÄVO ( vom 8. Dezember 2012 im Internet Archive) (PDF; 156 kB)
- ↑ vias.org: Lambda-Sonde
- ↑ AGC Galvanotechnik ( vom 8. Juni 2009 im Internet Archive)
- ↑ Beschichtungswerkstoffe für die optische Industrie. In: gfe.com. Gesellschaft für Elektrometallurgie, abgerufen am 3. Januar 2018.
