„Calciumphosphat“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
K Änderungen von 217.83.168.68 (Diskussion) rückgängig gemacht und letzte Version von Pittimann wiederhergestellt |
Rjh (Diskussion | Beiträge) Keine Bearbeitungszusammenfassung |
||
| Zeile 48: | Zeile 48: | ||
Calciumphosphat wird verwendet als [[Lebensmittelzusatzstoff]] (E 341c), z. B. für Fertigkuchenmischungen, bei denen es als [[Rieselhilfe|Trennmittel]] ein Klumpen verhindern und die Rieselfähigkeit erhalten soll. |
Calciumphosphat wird verwendet als [[Lebensmittelzusatzstoff]] (E 341c), z. B. für Fertigkuchenmischungen, bei denen es als [[Rieselhilfe|Trennmittel]] ein Klumpen verhindern und die Rieselfähigkeit erhalten soll. |
||
| ⚫ | |||
{{Quelle}} |
|||
Volume 341, Number 2, 77-86, [http://www.springerlink.com/content/m732q43u1396k681/ Experimenteller Knochenersatz durch resorbierbare Calciumphosphat-Keramik], {{DOI|10.1007/BF01262779}}</ref> |
|||
| ⚫ | |||
== Quellen == |
|||
== Einzelnachweise == |
|||
<references/> |
<references/> |
||
== Weblinks == |
== Weblinks == |
||
| ⚫ | |||
| ⚫ | |||
[[Kategorie:Calciumverbindung]] |
[[Kategorie:Calciumverbindung]] |
||
Version vom 7. Mai 2011, 15:31 Uhr
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
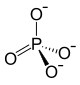
| ||||||||||
| Allgemeines | ||||||||||
| Name | Calciumphosphat | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | Ca3(PO4)2 | |||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Arzneistoffangaben | ||||||||||
| ATC-Code | ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 310,18 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte |
3,14 g·cm−3[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (0,02 g·l−1 bei 20 °C)[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Calciumphosphat, Tricalciumorthophosphat oder Tricalciumphosphat (Ca3(PO4)2) ist ein Calciumsalz der ortho-Phosphorsäure und gehört zu den Phosphaten. Der Begriff Tricalciumphosphat wird gelegentlich für die sehr ähnliche Verbindung Pentacalciumhydroxytriphosphat (Ca5(PO4)3·OH) verwendet.
Vorkommen
In der Natur kommt Calciumphosphat nicht in reiner Form vor. Mineralische Calciumphosphate wie zum Beispiel Apatit oder Phosphorit enthalten immer noch andere Anionen.[3] Von beiden gibt es große Lagerstätten, technische Bedeutung zur Produktion von Phosphor und Dünger (Superphosphat) besitzen aber lediglich die Apatite.[4]
Eigenschaften
Calciumphosphat ist ein farb- und geruchloser Feststoff, der bei 1670 °C schmilzt. Es ist praktisch unlöslich in Wasser.
Verwendung
Man verwendet das (wasserunlösliche) tertiäre Calciumphosphat zur Herstellung des (wasserlöslichen) primären Calciumphosphats Ca(H2PO4)2, besser bekannt als Superphosphat, einem weit verbreiteten Düngemittel.[5]
Calciumphosphat dient auch zur Herstellung von Phosphorsäure, indem es mit Schwefelsäure reagiert:[6]
Calciumphosphat wird verwendet als Lebensmittelzusatzstoff (E 341c), z. B. für Fertigkuchenmischungen, bei denen es als Trennmittel ein Klumpen verhindern und die Rieselfähigkeit erhalten soll.
In der Medizintechnik wird Tricalciumphosphat als synthetisches Knochenersatzmaterial eingesetzt; es wird langsam resorbiert und durch Eigenknochen ersetzt.[7]
Einzelnachweise
- ↑ a b c d e Eintrag zu Calciumphosphat in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich)
- ↑ Datenblatt Calciumphosphat bei Merck
- ↑ Holleman-Wiberg: Lehrbuch der Anorganischen Chemie. 91.-100. Auflage, Walter de Gruyter, 1985, S.655
- ↑ N. N. Greenwood, A. Earnshaw: Chemie der Elemente. VCH 1988, S. 611, 675.
- ↑ N. N. Greenwood, A. Earnshaw: Chemie der Elemente. VCH 1988, S. 675.
- ↑ Holleman-Wiberg: Lehrbuch der Anorganischen Chemie. 91.-100. Auflage, Walter de Gruyter, 1985, S.652
- ↑ Langenbeck's Archives of Surgery Volume 341, Number 2, 77-86, Experimenteller Knochenersatz durch resorbierbare Calciumphosphat-Keramik, doi:10.1007/BF01262779
