Calciumphosphat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
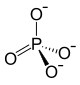
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Calciumphosphat | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | Ca3(PO4)2 | |||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 310,18 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
3,14 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (0,02 g·l−1 bei 20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Calciumphosphat, Tricalciumorthophosphat oder Tricalciumphosphat (Ca3(PO4)2) ist ein Calciumsalz der ortho-Phosphorsäure und gehört zu den Phosphaten. Der Begriff Tricalciumphosphat wird gelegentlich für die sehr ähnliche Verbindung Pentacalciumhydroxytriphosphat (Ca5(PO4)3·OH) (= Hydroxylapatit) verwendet.
Vorkommen[Bearbeiten | Quelltext bearbeiten]

In der Natur kommt Calciumphosphat nicht in reiner Form vor. Calciumphosphatminerale wie Apatit oder Whitlockit enthalten stets weitere Kationen (z. B. Natrium, Magnesium oder Eisen) und Anionen (Hydroxid, Carbonat, Fluorid oder Chlorid).[4] Das mit Abstand häufigste und wirtschaftlich bedeutendste Calciumphosphatmineral ist Apatit.[5] Abiogener Apatit ist akzessorischer Bestandteil zahlreicher magmatischer Gesteine und Hauptbestandteil des marin gebildeten Gesteins Phosphorit. Mehr als 80 % der weltweiten Förderung von Apatit entstammen Phosphoritlagerstätten.[6]
Apatit wird aber auch von bzw. in Lebewesen gebildet: Die mineralische Substanz der Knochen und Zähne der Wirbeltiere besteht daher überwiegend aus Hydroxylapatit. In Elfenbein liegt der Gesamtanteil bei 55 bis 61 %. Außerdem enthält Guano, ein biogenes „Sediment“ aus Tierexkrementen, geringe Mengen an Apatit. Biogenes Calciumphosphat ist eine wichtige Phosphatquelle für die sogenannte Phosphogenese, einen Teilschritt bei der Entstehung von Phosphoriten.[7]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Calciumphosphat ist ein weißer und geruchloser Feststoff, der bei 1670 °C schmilzt. Es ist praktisch unlöslich in Wasser.
Verwendung[Bearbeiten | Quelltext bearbeiten]
Das (wasserunlösliche) tertiäre Calciumphosphat wird zur Herstellung des (wasserlöslichen) primären Calciumphosphats Ca(H2PO4)2 verwendet, eines weit verbreiteten Düngemittels, besser bekannt als Superphosphat.[8]
Calciumphosphat dient auch zur Herstellung von Phosphorsäure, indem man es mit Schwefelsäure reagieren lässt:[9]
Hierbei anfallendes Calciumsulfat ist aufgrund seiner Verunreinigung mit diversen Begleitmineralien des ursprünglichen Phosphatgesteins üblicherweise nicht wirtschaftlich nutzbar und wird als Phosphorgips deponiert.
In der Lebensmitteltechnik wird Calciumphosphat als Säureregulator, Festigungsmittel oder Trennmittel eingesetzt; zum Beispiel für Fertigkuchenmischungen, bei denen es als Rieselhilfe die Bildung von Klumpen verhindern und die Rieselfähigkeit erhalten soll. Calciumphosphat ist zusammen mit Calciumdihydrogenphosphat und Calciumhydrogenphosphat in der EU als Lebensmittelzusatzstoff unter der gemeinsamen Nummer E 341 („Calciumphosphate“) für bestimmte Lebensmittel mit jeweils unterschiedlichen Höchstmengenbeschränkungen auch für Öko-Lebensmittel zugelassen. Nach der Zusatzstoff-Zulassungsverordnung sind dies – für die meisten zugelassenen Phosphate weitgehend einheitliche – einzelne Festlegungen für eine breite Palette mit zahlreichen unterschiedlichen Lebensmittelsorten. Die zugelassenen Höchstmengen variieren von 0,5 bis hin zu 50 Gramm pro Kilogramm (in Getränkeweißer für Automaten) oder auch dem Fehlen einer festen Beschränkung (quantum satis – nach Bedarf, bei Nahrungsergänzungsmitteln und teils bei Kaugummis). Es wurde eine erlaubte Tagesdosis von 70 Milligramm pro Kilogramm Körpergewicht für die Gesamtmenge aufgenommener Phosphorsäure und Phosphate festgelegt.
In der Knochenchirurgie und Implantologie wird Tricalciumphosphat als synthetisches Knochenersatzmaterial eingesetzt; es wird langsam resorbiert und durch Eigenknochen ersetzt.[10]
Adjuvanzien in Impfstoffen[Bearbeiten | Quelltext bearbeiten]
Bis in die 80er Jahre wurden in Frankreich Calciumphosphate als Adjuvanzien in Impfstoffen (DTP und Kinderlähmung) eingesetzt.[11] Jedoch lag nicht Calciumphosphat als Salz selbst vor, sondern nicht-stöchiometrische Hydroxylapatitformen wie Ca10(PO4)6(OH)2 oder Ca9(HPO4)(PO4)5(OH), die alle dasselbe Ca/P-Verhältnis aufweisen wie Calciumphosphat. Die OH-Gruppe ist für die Oberflächenladung und für die Absorption von Antigenen hilfreich.
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Weblinks[Bearbeiten | Quelltext bearbeiten]
- zusatzstoffe-online.de: E 341 - Calciumphosphat
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu TRICALCIUM PHOSPHATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 21. März 2020.
- ↑ a b c d e f Eintrag zu Calciumphosphat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Dezember 2012. (JavaScript erforderlich)
- ↑ Datenblatt Calciumphosphat bei Merck, abgerufen am 19. Januar 2011.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verbesserte und stark erweiterte Auflage. Walter de Gruyter, Berlin 1985, ISBN 3-11-007511-3, S. 655.
- ↑ N. N. Greenwood, A. Earnshaw: Chemie der Elemente. VCH 1988, S. 611, 675.
- ↑ Steven J. Van Kauwenbergh: World Phosphate Rock Reserves and Resources. International Fertilizer Development Center Technical Bulletin. Nr. 75, S. 2 f. (PDF 2,6 MB).
- ↑ Gabriel M. Filippelli: Phosphate rock formation and marine phosphorus geochemistry: The deep time perspective. Chemosphere. Bd. 84, Nr. 6 (Sonderausgabe The Phosphorous Cycle), 2011, S. 759–766, doi:10.1016/j.chemosphere.2011.02.019
- ↑ N. N. Greenwood, A. Earnshaw: Chemie der Elemente. VCH 1988, S. 675.
- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verbesserte und stark erweiterte Auflage. Walter de Gruyter, Berlin 1985, ISBN 3-11-007511-3, S. 652.
- ↑ Kari Köster, Eberhard Karbe, Horst Kramer, Helmut Heide, Rainer König: Experimenteller Knochenersatz durch resorbierbare Calciumphosphat-Keramik. In: Langenbecks Archiv für Chirurgie. 1976, Bd. 341, Nr. 2, S. 77–86, doi:10.1007/BF01262779
- ↑ Jean-Daniel Masson et al.: Calcium phosphate: a substitute for aluminum adjuvants? In: Expert Review of Vaccines. Band 16, Nr. 3, März 2017, S. 289–299, doi:10.1080/14760584.2017.1244484, PMID 27690701.
