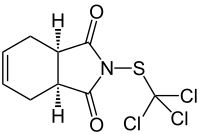
Captan
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Captan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C9H8Cl3NO2S | ||||||||||||||||||
| Kurzbeschreibung |
weißer bis gelber Feststoff mit schwach mercaptanartigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 300,59 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,74 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (< 0,5 mg·l−1 bei 25 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 5 mg·m−3 (gemessen als einatembarer Staub)[3] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Captan ist eine chemische Verbindung aus der Gruppe der Phthalimide.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Captan kann durch Reaktion von 1,2,3,6-Tetrahydrophthalimid mit Trichlormethansulfenylchlorid (Perchlormethylmercaptan) in Gegenwart von Natriumhydroxid gewonnen werden.[4]

Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Captan ist ein brennbarer weißer bis gelber (technisches Produkt) Feststoff mit schwach mercaptanartigem Geruch, der praktisch unlöslich in Wasser ist. Er zersetzt sich bei Erhitzung[1] und hydrolysiert langsam unter neutralen und rasch unter basischen Bedingungen.[5]
Verwendung[Bearbeiten | Quelltext bearbeiten]

Captan wird als Wirkstoff in Pflanzenschutzmitteln verwendet.[1] Es dient als Fungizid gegen eine Reihe von Krankheiten.[5] Captan wurde im März 1949 in den USA erstmals zugelassen.[6] Dort werden jährlich über 1400 t Captan – meist im Wein- und Obstbau – eingesetzt.
Im Obstbau wird Captan als Kontaktfungizid gegen pilzliche Lagerfäulen und Apfelschorf verwendet.
Zulassung[Bearbeiten | Quelltext bearbeiten]
Der Wirkstoff Captan wurde in der Europäischen Union mit Wirkung zum 1. Oktober 2007 für Anwendungen als Fungizid zugelassen.[7]
In vielen Staaten der EU, unter anderem in Deutschland und Österreich, sowie in der Schweiz sind Pflanzenschutzmittel (z. B. Malvin, Merpan) mit diesem Wirkstoff zugelassen.[8]
Geschichte[Bearbeiten | Quelltext bearbeiten]
Captan ist vermutlich karzinogen. Aus Gründen der Anwendersicherheit (Einatmen von Captanstaub beim Einfüllen) wurde 1986 die seit 1971 bestehende Zulassung nicht verlängert.[9] Erst 2001 wurde Captan in Deutschland als nichtstaubendes wasserdispergierbares Granulat (WG) wieder zugelassen.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Poisons Information Monograph (PIM) für Captan
- EFSA: Peer review of the pesticide risk assessment of the active substance captan, 4. Juni 2009, doi:10.2903/j.efsa.2009.296r
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g h i j k l Eintrag zu Captan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ Eintrag zu Captan im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 133-06-2 bzw. Captan), abgerufen am 2. November 2015.
- ↑ Thomas A. Unger: Pesticide synthesis handbook. 1996, ISBN 0-8155-1401-8, S. 454 (englisch, eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Terence Robert Roberts, D. H. Hutson: Metabolic pathways of agrochemicals. Royal Soc of Chemistry, 1999, ISBN 0-85404-499-X (englisch, eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Robert Irving Krieger: Handbook of Pesticide Toxicology: Principles. 2001, ISBN 0-12-426261-9, S. 1712 (englisch, eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Richtlinie 2007/5/EG der Kommission vom 7. Februar 2007 zur Änderung der Richtlinie 91/414/EWG des Rates zwecks Aufnahme der Wirkstoffe Captan, Folpet, Formetanat und Methiocarb
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Captan in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs (Eingabe von „Captan“ im Feld „Wirkstoff“) und Deutschlands, abgerufen am 23. Februar 2016.
- ↑ Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Frau Hönes, Werner (Dierstorf) und der Fraktion DIE GRÜNEN – Drucksache 10/5953 – Nichtverlängerung der Zulassung von 36 Pflanzenschutzmitteln mit den Wirkstoffen Captan, Captafol und Folpet (22. September 1986)



