Natriumhydrid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
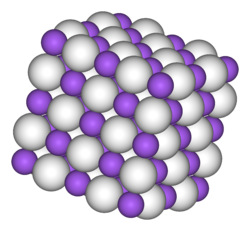
| ||||||||||||||||
| _ Na+ _ H− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Natriumhydrid | |||||||||||||||
| Verhältnisformel | NaH | |||||||||||||||
| Kurzbeschreibung |
grauweiße Kristalle[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 23,99 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,396 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
reagiert heftig mit Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Natriumhydrid (NaH) ist das Hydrid des Natriums, also eine Ionenverbindung, in der Wasserstoff negativ geladen ist und Natrium positiv.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Es wird technisch bei 250–300 °C durch Überleiten von reinem Wasserstoffgas über geschmolzenes Natrium hergestellt. Dabei dürfen weder Wasser noch Sauerstoff zugegen sein.[3]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]

Natriumhydrid ist eine ionische, salzartige Verbindung: Es hat die Struktur eines Ionengitters, das der Natriumchlorid-Struktur ähnelt. Bei Kontakt mit Wasser reagiert es heftig zu Natronlauge und molekularem Wasserstoff, der leicht entzündlich ist. Als Schutz gegen Luftfeuchtigkeit wird Natriumhydrid meist als Mischung von 60 % NaH in Paraffinöl oder Petrolether verkauft.
Es zeigt alle typischen Eigenschaften eines salzartigen Hydrids. So erfolgt mit allen Säuren sofortige, oftmals explosionsartige Bildung von elementarem Wasserstoff. Dies gilt z. B. für die Reaktion mit Wasser, Alkoholen, Ammoniak und Halogenwasserstoffen:
- Reaktion mit Wasser zu Natriumhydroxid und Wasserstoff
- Reaktion mit Ethanol zu Natriumethanolat und Wasserstoff
- Reaktion mit Ammoniak zu Natriumamid und Wasserstoff
- Reaktion mit Chlorwasserstoff zu Natriumchlorid und Wasserstoff
Diese Reaktionen sind gleichzeitig Redoxreaktionen; es handelt sich um Komproportionierung.
Die basische Wirkung des Hydrid-Ions nutzt man auch bei der Claisen-Kondensation. Darüber hinaus ist Natriumhydrid ein starkes Reduktionsmittel und wird zur Reduktion organischer Verbindungen eingesetzt.[4]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Natriumhydrid ist eine starke Base (nach Brønsted ist das Hydrid-Ion die Base), die vor allem in der organischen Synthese Verwendung findet, da sie in der Lage ist, auch schwache Säuren wie z. B. Alkohole zu deprotonieren. Des Weiteren kann Natriumhydrid als Reduktionsmittel verwendet werden, z. B. um aus Disulfiden Thiole zu gewinnen.
Literatur[Bearbeiten | Quelltext bearbeiten]
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Eintrag zu Natriumhydrid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Eintrag zu Sodium hydride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 949.
- ↑ Spektrum der Wissenschaft Verlagsgesellschaft mbH: Natriumhydrid.






