Natriumpersulfat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
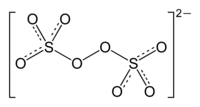
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Natriumpersulfat | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | Na2S2O8 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Kristalle[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 238,11 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,20 g·cm−3 (20 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
gut in Wasser (545 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Natriumpersulfat (chemische Formel Na2S2O8) ist das Natriumsalz der Peroxodischwefelsäure. Da es – besonders in unreinem oder feuchtem Zustand – zum Zerfallen unter Sauerstoffentstehung neigt, dürfen das Salz und seine Lösungen wegen Berstgefahr niemals in dicht verschlossenen Behältern aufbewahrt werden.
Das Persulfat-Ion enthält Sauerstoff in der instabilen Oxidationsstufe −1, daher wirkt Natriumpersulfat als sehr starkes Oxidationsmittel. Zur Unterscheidung von Kaliumperoxomonosulfat wird aus Iodidlösungen langsam Iod abgeschieden, Mangan(II)-Lösungen werden zu Braunstein oxidiert, in Gegenwart katalytisch wirkender Silberionen sogar bis zum Permanganat.
Verwendung[Bearbeiten | Quelltext bearbeiten]
In Wasser gelöst wird Natriumpersulfat in der Leiterplattentechnik zum Ätzen der Kupferschichten von Platinen verwendet:
Statt Natriumpersulfat kann auch das entsprechende Ammoniumsalz verwendet werden.
Gegenüber dem üblichen Ätzen mit Eisen(III)-chlorid-Lösung hat Natriumpersulfat den Vorteil einer geringeren Unterätzung auch bei höheren Temperaturen (nicht über 50 °C, erhöhter Zerfall), und damit einer genaueren Konturenschärfe (daher der Handelsname Feinätzkristall).
Die Lösung muss nach der Verwendung aufgrund des Kupfergehaltes als Sondermüll entsorgt oder das Kupfer durch Reduktion an Stahlwolle aus der Lösung entfernt[3] werden.
Natriumpersulfat wird auch als wasserlöslicher Initiator für die radikalische Polymerisation (z. B. Emulsionspolymerisation) eingesetzt.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu SODIUM PERSULFATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 17. April 2020.
- ↑ a b c d e f Eintrag zu Natriumperoxodisulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Entsorgung von Ätzflüssigkeiten ( vom 7. September 2009 im Internet Archive)



