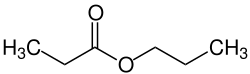
Propionsäurepropylester
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Propionsäurepropylester | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C6H12O2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit birnenartigem Geruch[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 116,16 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[2] | ||||||||||||||||||
| Dichte |
0,88 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
122 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,3930 (20 °C)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Propionsäurepropylester ist ein in der Natur vorkommender Fruchtester und eine chemische Verbindung aus der Gruppe der Carbonsäureester.
Vorkommen[Bearbeiten | Quelltext bearbeiten]

Propionsäurepropylester wurde unter den flüchtigen Bestandteilen von Weintrauben, in frischem Äpfeln, Apfelsaft, Aprikosen, Melonen, Papaya, Birnen, bestimmten Käsesorten, Rum, Apfelwein, Popcorn, Oliven, Malzwhiskey und Kaffee nachgewiesen.[3]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Propionsäurepropylester kann durch Veresterung von Propylalkohol mit Propionsäure in Gegenwart von konzentrierter Schwefelsäure oder Bortrifluorid gewonnen werden.[3]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Propionsäurepropylester ist eine farblose Flüssigkeit mit birnenartigem Geruch, die schwer löslich in Wasser ist.[2]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Propionsäurepropylester wird in der Autoreparaturlackierung, OEM-Lacken, Gerätebeschichtungen, Druckfarben und als Polymerisationslösungsmittel eingesetzt. Seine gute Aktivität ermöglicht eine effiziente Viskositätssenkung des Harzes, die die Entwicklung von VOC-ärmeren Beschichtungen ermöglicht. Sein hoher elektrischer Widerstand ist von Vorteil bei der Optimierung der Übertragungseffizienz von Beschichtungen, die über elektrostatische Sprühgeräte aufgebracht werden.[4] Die Verbindung wird in der Aromen- und Riechstoffindustrie sowie als Lösemittel verwendet.[6]
Sicherheitshinweise[Bearbeiten | Quelltext bearbeiten]
Die Dämpfe von Propionsäurepropylester können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 24 °C, Zündtemperatur 445 °C) bilden.[2]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu PROPYL PROPIONATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 19. September 2021.
- ↑ a b c d e f g h i j k l m Eintrag zu Propionsäurepropylester in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28. November 2018. (JavaScript erforderlich)
- ↑ a b c George A. Burdock: Fenaroli's Handbook of Flavor Ingredients. CRC Press, 2004, ISBN 978-1-4200-3787-6, S. 1648 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Datenblatt n-Propyl propionate, 99% bei Alfa Aesar, abgerufen am 28. November 2018 (Seite nicht mehr abrufbar).
- ↑ Eintrag zu Propylpropionat im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 30. November 2018. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Martin Cruz-Díaz, Carstens Buchaly, Peter Kreis, Eduardo S. Pérez-Cisneros, Ricardo Lobo-Oehmichen, Andrzej Górak: Synthesis of n-propyl propionate in a pilot-plant reactive distillation column: Experimental study and simulation. In: Computers & Chemical Engineering. Band 39, 2012, S. 118–128, doi:10.1016/j.compchemeng.2012.01.004.

