Carbonsäureester
| Carbonsäureester |
|---|

|
| R1 und R2 sind Organylgruppen. R1 kann aber auch ein Wasserstoffatom sein. Die funktionelle Gruppe ist blau markiert. |
Carbonsäureester (R1–COO–R2) sind Ester, die formal aus einer Carbonsäure (R1–COOH) und einem Alkohol bzw. einem Phenol (R2-OH) zusammengesetzt sind bzw. gebildet werden. Ester von kurzkettigen Monocarbonsäuren mit kurzkettigen Alkoholen kommen als wohlriechende Verbindungen in ätherischen Ölen (sogn. Fruchtester) vor oder sie dienen wie der Essigsäureethylester als ein häufig benutztes Lösungsmittel. Ester von längerkettigen Monocarbonsäuren (Fettsäuren mit längerkettigen Alkoholen) kommen in natürlichen Wachsen vor.
Pflanzliche und tierische Fette und Öle sind dreifache Ester. Sie werden als Triglyceride bezeichnet, weil sie aus dem Triol Glycerin und drei gleichen oder unterschiedlichen Fettsäuren gebildet werden.
Eine spezielle Gruppe von Estern sind die Lactone. Es handelt sich dabei um cyclische Ester, die sich intramolekular bilden können, wenn die Carboxygruppe einer Carbonsäure und die Hydroxygruppe eines Alkohols im gleichen Molekül und im passenden Abstand vorhanden sind und miteinander zur Reaktion gebracht werden können. Das ist z. B. der Fall bei der Bildung von γ-Butyrolacton aus der γ-Hydroxybuttersäure
Die als Polyester bezeichneten wichtigen Kunststoffe sind polymere Carbonsäureester und können aus Dicarbonsäuren und Diolen oder aus geeigneten Lactonen gebildet werden.
Nomenklatur und Strukturerklärung[Bearbeiten | Quelltext bearbeiten]
Carbonsäureester setzen sich aus einem Carbonsäureteil und einem Alkoholteil zusammen. Es gibt zwei mögliche Typen von Trivialnamen für Carbonsäureester. Beim ersten Typ wird der Name des Esters aus dem Namen der Carbonsäure, der Bezeichnung für den organischen Rest des Alkohols, und aus dem Wort Ester als Bezeichnung für die funktionelle Gruppe zusammengesetzt. Ein Beispiel ist der Name Essigsäureethylester, der aus dem Namen der Säure Essigsäure, der Bezeichnung für den Alkylrest des Alkohols Ethanol (ethyl-) und dem Wort Ester gebildet wird. Dieser Trivialname beschreibt den strukturellen Aufbau des Esters gut. Beim zweiten Typ von Trivialnamen wird der Carbonsäureester als ein Salz der Carbonsäure aufgefasst und auch namentlich nicht mehr als Ester bezeichnet, sondern als Salz der jeweiligen Säure, im Falle der Essigsäure also als Acetat. Der Ethanolester der Essigsäure wird dann als Ethylacetat bezeichnet. Dieser Trivialname beschreibt den strukturellen Aufbau des Esters nicht, ist aber kurz und eindringlich.
Der systematische Name dieses Esters ist jedoch Ethylethanoat und wird nach dem Prinzip „Rest des Alkohols (= Ethyl) + Grundkörper der Säure (= Ethan) + oat“ gebildet. Das Suffix „R-oat“ ist jedoch nicht bei allen Verbindungen zulässig. Befindet sich in einer Verbindung eine weitere funktionelle Gruppe mit höherer Priorität, wie zum Beispiel eine Säure oder ein Kation, dann muss der Ester als Präfix genannt werden. Die zu verwendende Bezeichnung lautet R-oxycarbonyl-.
Beispiele[Bearbeiten | Quelltext bearbeiten]
| Säure | Alkohol | Ester |
|---|---|---|
| Einfache Carbonsäureester am Beispiel der Essigsäure | ||
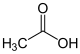 Essigsäure |
Methanol |
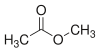 Essigsäuremethylester Essigsäuremethylester
|
Ethanol |
||
1-Butanol |
||
| Lactone: innere Carbonsäureester | ||
4-Hydroxybutansäure |
||
| Fette und fette Öle | ||
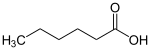 als Beispiel: Hexansäure (allg.: → Fettsäuren) |
Glycerin |
 Triglyceride |
| Polyester: z. B. PET | ||
 Terephthalsäure |
Ethylenglycol |
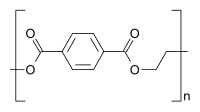 Polyethylenterephthalat |
Physikalische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Aufgrund der Elektronegativitätsdifferenz zwischen Kohlenstoff und Sauerstoff ist die Carbonsäureester-Gruppe polar und ermöglicht im Prinzip eine Löslichkeit in Wasser durch Bildung von Wasserstoffbrückenbindungen. Vom kurzkettigen Carbonsäureester Essigsäuremethylester lösen sich etwa 250 g/l in Wasser. Von dem etwas langkettigeren Essigsäurebutylester gehen nur noch ca. 10 g/l in Lösung. Die Gesamtlöslichkeit wird durch die organischen Reste bestimmt, sodass bei hinreichend unpolaren Resten die Wasserlöslichkeit sehr gering wird. Die meisten Ester sind hydrophob und sind Öle oder Wachse.
Die Siedepunkte von kurzkettigen Carbonsäureestern liegen im Vergleich zu Alkoholen oder Carbonsäuren von vergleichbarer molarer Masse wesentlich niedriger, da sie anders als Carbonsäuren oder Alkohole keine starken Wasserstoffbrückenbindungen ausbilden können.
Reaktionen[Bearbeiten | Quelltext bearbeiten]
Synthese[Bearbeiten | Quelltext bearbeiten]
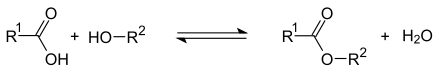
Alkohole und Carbonsäuren lassen sich durch Veresterung zu Carbonsäureestern umsetzen. Die Veresterung erfolgt durch eine Säure als Katalysator und ist eine Gleichgewichtsreaktion. Durch Entfernung des entstehenden Wassers aus dem Reaktionsgemisch z. B. durch eine azeotrope Destillation oder durch Einsatz eines Molekularsiebs wird das Gleichgewicht Richtung Ester verschoben.
Neben der Umsetzung von Carbonsäuren führen auch Reaktionen der entsprechenden Carbonsäureanhydride und Carbonsäurechloride zu Estern. Eine weitere, technisch bedeutende Reaktion ist die Umesterung, der Austausch eines Alkohols im Ester gegen einen anderen. Dies wird beispielsweise eingesetzt, um aus Rapsöl die Methylester der Fettsäuren herzustellen, die als Biodiesel verwendet werden.

Eine bekannte Reaktion zur Estersynthese der organischen Chemie ist die Baeyer-Villiger-Oxidation. Dabei werden Percarbonsäuren mit Ketonen zu Carbonsäureestern umgesetzt.[1]
Esterspaltung[Bearbeiten | Quelltext bearbeiten]
Ester können hydrolytisch und pyrolytisch gespalten werden. Für die Hydrolyse werden meist Basen, aber auch Säuren eingesetzt. Bei der Spaltung mit Säuren entstehen entsprechend dem eingesetzten Edukt der Alkohol und die Carbonsäure. Wird der Ester mit Basen gespalten, entstehen der jeweilige Alkohol und das Carboxylat-Anion. Die basische Esterspaltung wird auch Verseifung genannt. Diese Bezeichnung rührt daher, dass aus Fetten und fetten Ölen (die Ester von Fettsäuren mit Glycerin sind) die Alkalisalze der Fettsäuren, also Seifen, gewonnen werden. Die Esterspaltung kann auch mit Lipasen, einer Enzymgruppe, erfolgen,[2] die bei der Verdauung von Fetten eine wichtige Rolle spielen. Praktische Bedeutung hat die Esterspaltung bei Waschmitteln, die Lipasen enthalten, um die wasserunlöslichen Fettreste auf Textilien unter Bildung leidlich wasserlöslicher Fettsäuren und gut wasserlöslichen Glycerins zu spalten. Zur Gewinnung enantiomerenreiner Carbonsäuren oder Alkohole wird in der Chemie stereoselektiv ein Enantiomer racemischer Carbonsäureester gespalten. Dabei bleibt das zweite Enantiomer des Carbonsäureesters unverändert und erlaubt eine Racemat-Trennung.
C,H-Acidität[Bearbeiten | Quelltext bearbeiten]
Ester sind keine Säuren, jedoch C,H-acide Verbindungen, da das Proton in α-Position durch sehr starke Basen abgespalten (abstrahiert) werden kann. Hierdurch entsteht ein mesomeriestabilisiertes Enolat:

(R1= H, Organylrest, wie z. B. ein Alkyl- oder Arylrest; R2= Organylrest, wie z. B. ein Alkyl- oder Arylrest).
Säureteil gegen Alkoholteil[Bearbeiten | Quelltext bearbeiten]

Wie abgebildet, stammt bei der (oft üblichen) Bildung des Esters aus Carbonsäure und Alkohol der blau dargestellte Teil des Esters aus dem Alkohol (hier: Ethanol) und der rot dargestellte Teil aus der Carbonsäure (hier: Essigsäure). Eine Ausnahme ist die Bildung der Ester aus Salzen der Carbonsäure (Carboxylaten) und Alkylierungsmitteln; hierbei stammt der im Bild blau dargestellte Sauerstoff aus der Carbonsäure.
Bei der Spaltung von Estern (sowohl sauer als auch basisch katalysierbar) enthält der dabei gebildete Alkohol den im Bild blau dargestellten Sauerstoff. Auch hier gibt es eine Ausnahme, nämlich die sauer katalysierte Spaltung von Estern tertiärer Alkohole, bei denen aus dem Alkohol-Teil ein Alken gebildet wird (E1-Reaktion).
Dass das bei der Esterbildung verbleibende Sauerstoffatom aus dem Alkohol stammt, ist durch Isotopenmarkierung unter Verwendung des Sauerstoffisotops 18O belegbar.[3]
Weitere Reaktionen[Bearbeiten | Quelltext bearbeiten]
- Arylester können mittels Fries-Umlagerung zu Arylketonen reagieren.
- Spezielle Ester könne eine Chan-Umlagerung eingehen.
- Umwandlung in Isocyanate mittels Lossen-Abbau.
Carbonsäureester-Vorkommen in Früchten (Auswahl)[Bearbeiten | Quelltext bearbeiten]
-
Äpfel enthalten 2-Methylbuttersäureethylester, Buttersäureethylester, Essigsäure-2-methylbutylester, Essigsäure-n-butylester und Essigsäurehexylester.
-
Bananen enthalten Essigsäureamylester, Buttersäure-3-methylbutylester, 3-Methylbuttersäure-3-methylbutylester[5]
-
Birnen enthalten Essigsäureamylester, (2E,4Z)-Deca-2,4-diensäureethylester[5]
-
Kiwi enthält 3-Hydroxybuttersäureethylester[6]
-
Mandarinen enthalten N-Methylanthranilsäuremethylester[7]
-
Passionsfrucht enthält Buttersäureethylester, Hexansäureethylester, Buttersäurehexylester, Hexansäurehexylester[4]
-
Pfirsiche enthalten Ester der Essigsäure[8]
-
Pflaumen enthalten Zimtsäuremethylester[4]
-
Quitten enthalten 2-Methylbuttersäureethylester[9]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Ethylacetat wird als Extraktionsmittel zur Entkoffeinierung von Kaffeebohnen benutzt.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Baeyer-Villiger-Oxidation. Abgerufen am 15. März 2019.
- ↑ Maryadele J. O’Neil (Hrsg.): The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, Merck, Whitehouse Station 2006, ISBN 978-0-911910-00-1, S. 955.
- ↑ Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie. Springer, Wien/New York 1972, ISBN 3-211-81060-9, S. 73–74.
- ↑ a b c H.-D. Belitz u. a.: Lehrbuch der Lebensmittelchemie. 5. Auflage. Springer, Berlin u. a. 2001, S. 821–825 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d Eintrag zu Fruchtester. In: Römpp Online. Georg Thieme Verlag, abgerufen am 9. Dezember 2014.
- ↑ M. J. Jordán u. a.: Aroma active components in aqueous kiwi fruit essence and kiwi fruit puree by GC-MS and multidimensional GC/GC-O. In: J. Agric. Food Chem. 2002, 50, 5386-5390. PMID 12207479.
- ↑ W. Legrum: Riechstoffe, zwischen Gestank und Duft. Vieweg + Teubner, Wiesbaden 2011, S. 88 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ R. Ebermann, I. Elmadfa: Lehrbuch Lebensmittelchemie und Ernährung. 2. Auflage. Springer, Wien und New York 2011, S. 420–425 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ W. Ternes: Naturwissenschaftliche Grundlagen der Lebensmittelzubereitung. 3. Auflage. Behr’s Verlag, Hamburg 2008, S. 824 (eingeschränkte Vorschau in der Google-Buchsuche).

![Ananas enthält (S)-2-Methylbuttersäure-ethylester[4][5]](http://upload.wikimedia.org/wikipedia/commons/thumb/c/cb/Pineapple_and_cross_section.jpg/120px-Pineapple_and_cross_section.jpg)

![Bananen enthalten Essigsäureamylester, Buttersäure-3-methylbutylester, 3-Methylbuttersäure-3-methylbutylester[5]](http://upload.wikimedia.org/wikipedia/commons/thumb/4/4c/Bananas.jpg/120px-Bananas.jpg)
![Birnen enthalten Essigsäureamylester, (2E,4Z)-Deca-2,4-diensäureethylester[5]](http://upload.wikimedia.org/wikipedia/commons/thumb/c/cf/Pears.jpg/79px-Pears.jpg)
![Erdbeeren enthalten Anthranilsäuremethylester, Buttersäureethylester, Hexansäureethylester[5]](http://upload.wikimedia.org/wikipedia/commons/thumb/1/1b/Erdbeeren_2.jpg/94px-Erdbeeren_2.jpg)
![Kiwi enthält 3-Hydroxybuttersäureethylester[6]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d3/Kiwi_aka.jpg/120px-Kiwi_aka.jpg)
![Mandarinen enthalten N-Methylanthranilsäuremethylester[7]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/77/Mandarinenb%C3%A4umchen.JPG/90px-Mandarinenb%C3%A4umchen.JPG)
![Passionsfrucht enthält Buttersäureethylester, Hexansäureethylester, Buttersäurehexylester, Hexansäurehexylester[4]](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f9/Maracuy%C3%A1.jpg/120px-Maracuy%C3%A1.jpg)
![Pfirsiche enthalten Ester der Essigsäure[8]](http://upload.wikimedia.org/wikipedia/commons/thumb/9/9e/Autumn_Red_peaches.jpg/120px-Autumn_Red_peaches.jpg)
![Pflaumen enthalten Zimtsäuremethylester[4]](http://upload.wikimedia.org/wikipedia/commons/thumb/6/67/Fruits_Prunus_domestica.jpg/120px-Fruits_Prunus_domestica.jpg)
![Quitten enthalten 2-Methylbuttersäureethylester[9]](http://upload.wikimedia.org/wikipedia/commons/thumb/0/04/Quitte_am_Baum.jpg/120px-Quitte_am_Baum.jpg)