Salvinorine

Die Salvinorine sind eine Gruppe strukturell eng verwandter diterpenoider Sekundärmetabolite des Aztekensalbeis (Salvia divinorum). In deutlich geringerer Konzentration lassen sich einige Salvinorine auch in anderen Salbeiarten finden, darunter auch im klebrigen Salbei oder in Salvia recognita.[1]
Übersicht
[Bearbeiten | Quelltext bearbeiten]Als erste Substanz von inzwischen neun Einzelvertretern der Salvinorine (A–H, J) wurde 1982 Salvinorin A isoliert.[2] Salvinorin A ist ein Halluzinogen mit dissoziativen Effekten.[3] Die Salvinorine B–E gelten als psychotropisch inaktiv, von Salvinorin F ist keine psychotrope Wirkung bekannt. Salvinorin A wurde identifiziert als selektiver Agonist des κ-Opioid-Rezeptors.[4] Auch für Salvinorin G wurde in niedrigen Konzentrationen eine Bindung an diesen Rezeptor nachgewiesen.[5]
Salvinorin A ist die potenteste bekannte natürlich vorkommende psychoaktive Substanz, mit einer Wirkdosis ab 200 µg.[6][7] Auffällig ist, dass die Substanz im Gegensatz zu anderen natürlichen Halluzinogenen wie DMT, Psilocybin oder Mescalin, oder vergleichbaren synthetischen Drogen wie LSD oder 2C-B, über kein basisches Stickstoffatom verfügt.
| Name | Struktur | R1 | R2 | Summenformel | Molmasse | CAS-Nummer | PubChem |
|---|---|---|---|---|---|---|---|
| Salvinorin A | 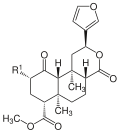 |
–OCOCH3 | − | C23H28O8 | 432,46 g·mol−1 | 83729-01-5 | 128563 |
| Salvinorin B | –OH | − | C21H26O7 | 390,43 g·mol−1 | 92545-30-7 | 11440685 | |
| Salvinorin C | 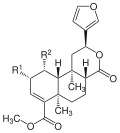 |
–OCOCH3 | –OCOCH3 | C25H30O9 | 475,29 g·mol−1 | 385785-99-9 | – |
| Salvinorin D | –OCOCH3 | –OH | C23H28O8 | 432,47 g·mol−1 | 540770-13-6 | – | |
| Salvinorin E | –OH | –OCOCH3 | C23H28O8 | 432,47 g·mol−1 | 540770-14-7 | – | |
| Salvinorin F | –OH | –H | C21H26O6 | 374,43 g·mol−1 | 540770-15-8 | – | |
| Salvinorin G | =O | –OCOCH3 | C23H26O8 | 430,45 g·mol−1 | 866622-54-0 | – | |
| Salvinorin H | –OH | –OH | C21H26O7 | 390,43 g·mol−1 | 872004-62-1 | – | |
| Salvinorin I |  |
– | – | C21H28O7 | 392,45 g·mol−1 | 917951-71-4 | – |
| 17α-Salvinorin J | 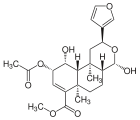 |
– | – | C23H30O8 | 434,49 g·mol−1 | 1157894-83-1 | – |
| 17β-Salvinorin J | 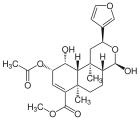 |
– | – | C23H30O8 | 434,49 g·mol−1 | 1157894-85-3 | – |
Kürzlich wurde die Isolierung einer weiteren Verbindung publiziert, die den Salvinorinen zuzurechnen ist. Die Struktur von Salvinorin J ist der von Salvinorin E ähnlich, allerdings ist C-17 dort nicht als Lacton ausgebildet, sondern als Halbacetal.[8]
Synthetisch hergestellte Salvinorin-Analoga
[Bearbeiten | Quelltext bearbeiten]Aufgrund der hohen pharmakologischen Wirksamkeit sind inzwischen weitere Derivate synthetisch hergestellt worden, die teilweise noch höhere Wirksamkeiten als Salvinorin A am κ-Opioid-Rezeptor aufweisen.[9] Strukturell verwandte Substanzen sind auch Herkinorin, Divinatorin und Salvinicin.
Rechtlicher Status
[Bearbeiten | Quelltext bearbeiten]In Deutschland wurde mit der 21. BtMÄndV Salvia divinorum (Pflanzen und Pflanzenteile) in Anlage I des BtMG aufgenommen und zählt damit zu den „nicht verkehrsfähigen Betäubungsmitteln“.
Literatur
[Bearbeiten | Quelltext bearbeiten]- D. M. Turner: Salvinorin: The Psychedelic Essence of Salvia Divinorum. Panther Press, 1996, ISBN 0-9642636-2-9 (englisch).
- Jochen Gartz: Salvia divinorum – Die Wahrsagesalbei. Nachtschatten Verlag, 2001, ISBN 3-907080-28-9, 80 Seiten.
- Bastian Borschke: Salvia Divinorum und andere psychoaktive Salbeiarten. Grüne Kraft, 2002, ISBN 3-930442-55-8, 32 Seiten.
- Salvia divinorum. In: Entheogene Blätter, Ausgabe #16, 09/2003, ISSN 1610-0107.
- Thomas E. Prisinzano, Richard B. Rothman: Salvinorin A Analogs as Probes in Opioid Pharmacology. In: Chemical Reviews, 2008, 108, S. 1732–1743. doi:10.1021/cr0782269
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Daniel Siebert: Salvinorin (englisch)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Muslum Akgoz, Seda Damla Hatipoglu, Gulacti Topcu, Ahmet Ceyhan Goren, Turan Oztur, Burhanettin Yalcinkaya: Screening of Hallucinogenic Compounds and Genomic Characterisation of 40 Anatolian Salvia Species. In: Phytochemical Analysis. 2017, S. 541–549, doi:10.1002/pca.2703.
- ↑ A Ortega, JF Blount, PS Manchand: Salvinorin, a new trans-neoclerodane diterpene from Salvia divinorum(Labiatae). In: J. Chem. Soc., Perkin Trans. 1. 1982, S. 2505–2508, doi:10.1039/P19820002505.
- ↑ K. A. MacLean, M. W. Johnson, C. J. Reissig, T. E. Prisinzano, R. R. Griffiths: Dose-related effects of salvinorin A in humans: dissociative, hallucinogenic, and memory effects. In: Psychopharmacology. Band 226, Nummer 2, März 2013, S. 381–392, doi:10.1007/s00213-012-2912-9, PMID 23135605, PMC 3581702 (freier Volltext).
- ↑ B.L. Roth et al.: Salvinorin A: A potent naturally occurring nonnitrogenous opioid selective agonist. In: PNAS. Band 99, 2002, S. 11934–11939. PMID 12192085 doi:10.1073/pnas.182234399.
- ↑ Timothy A. Vortherms, Bryan L. Roth: Salvinorin A – From Natural Product to Human Therapeutics. In: Molecular Interventions, 2006, Vol. 6, No. 5, S. 257–265. doi:10.1124/mi.6.5.7.
- ↑ D.J. Siebert: Salvia divinorum and salvinorin A: new pharmacologic findings. (PDF; 284 kB) In: J. Ethnopharmacol, Band 43, 1994, S. 53–56. PMID 16426651.
- ↑ Robin Marushia: Salvia divinorum: The Botany, Ethnobotany, Biochemistry and Future of a Mexican Mint. (PDF; 54 kB) In: Ethnobotany. 7. Oktober 2007, abgerufen am 11. August 2024.
- ↑ Lukasz Kutrzeba, Ferreira, Zjawiony: Salvinorins J from Salvia divinorum: Mutarotation in the Neoclerodane System. In: J. Nat. Prod. 72. Jahrgang, Nr. 7, 2009, S. 1361–1363, doi:10.1021/np900181q.
- ↑ TA Munro, KK Duncan, W Xu, Y Wang, LY Liu-Chen, WA Carlezon, BM Cohen, C Béguin: Standard protecting groups create potent and selective kappa opioids: salvinorin B alkoxymethyl ethers. In: Bioorganic & Medicinal Chemistry. 16. Jahrgang, Nr. 3, Februar 2008, S. 1279–86, doi:10.1016/j.bmc.2007.10.067, PMID 17981041, PMC 2568987 (freier Volltext).
