Tifluadom
{{Infobox Chemikalie
| Strukturformel = 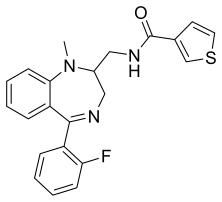 | Freiname = Tifluadom
| Suchfunktion = C22H20FN3OS
| Andere Namen = * IUPAC: N-{[5-(2-Fluorphenyl)-1-methyl-2,3-dihydro-1,4-benzodiazepin-2-yl]methyl}thiophen-3-carboxamid
| Freiname = Tifluadom
| Suchfunktion = C22H20FN3OS
| Andere Namen = * IUPAC: N-{[5-(2-Fluorphenyl)-1-methyl-2,3-dihydro-1,4-benzodiazepin-2-yl]methyl}thiophen-3-carboxamid
- MeSH: 1-Methyl-2-(3-thienylcarbonyl)aminomethyl-5-(2-fluorphenyl)-H-2,3-dihydro-1,4-benzodiazepin
| Summenformel = C22H20FN3OS | CAS = 83386-35-0 | PubChem = 115208 | ATC-Code = | DrugBank = | Wirkstoffgruppe = Benzodiazepin | Wirkmechanismus = Bindung an den κ-Opioidrezeptor | Molare Masse = 393,48 g·mol−1 | Dichte = | Schmelzpunkt = | Siedepunkt = | Dampfdruck = | pKs = | Löslichkeit = | Quelle GHS-Kz = NV | GHS-Piktogramme =
| keine Einstufung verfügbar |
| GHS-Signalwort = | H = siehe oben | EUH = siehe oben | P = siehe oben | Quelle P = | Quelle GefStKz = NV | Gefahrensymbole =
keine Einstufung verfügbar
|
| R = siehe oben | S = siehe oben }}
Tifluadom ist ein nicht therapeutisch genutztes Benzodiazepin-Derivat mit einem für diese Substanzklasse abnormen Wirkmechanismus.
Wirkmechanismus
Tifluadom zeigt im Gegensatz zu anderen Benzodiazepinen keine Wirkung am GABAA-Rezeptor und entfaltet daher auch nicht die für diese Stoffgruppe typischen anxiolytischen, sedierenden, hypnotischen und zentral muskelrelaxierenden Wirkungen. Durch entsprechende Substitutionen wurde das Benzodiazepin-Grundgerüst so verändert, dass die Substanz eine hohe Affinität zum κ-Rezeptor aufweist,[1] woraus sich eine opioidähnliche Wirkung ergibt: Trifluadom zeigt im Tierversuch ein hohes analgetisches Potenzial,[2] verursacht eine verstärkte Diurese[3] sowie eine Anregung des Appetits[4][5][6] und besitzt sedierende Effekte. Weiterhin wirkt es als peripherer Cholecystokininrezeptor-Antagonist.[7]
Verwendung
Aufgrund der unerwünschten Wirkungen (siehe unten) wird Tifluadom zurzeit nicht als Arzneimittel eingesetzt, findet aber in der Forschung Anwendung.
Nebenwirkungen
Tifluadom zeigt bedingt durch den κ-Agonismus unangenehme Nebenwirkungen wie Dysphorie und Halluzinationen, vergleichbar dem 2006 aus dem Handel genommenen Arzneistoff Pentazocin (Fortral®) und dem ebenfalls als Betäubungsmittel eingestuften Salvinorin A, das im Aztekensalbei vorkommt und psychoaktive Wirkungen hat. Das Abhängigkeitspotenzial von Tifluadom soll hingegen nur gering ausgeprägt sein.[8]
Einzelnachweise
- ↑ D. Romer, H. H. Buscher, R. C. Hill, R. Maurer, T. J. Petcher, H. Zeugner, W. Benson, E. Finner, W. Milkowski, P. W. Thies: Unexpected opioid activity in a known class of drug. In: Life Sciences. 20–27;31(12–13) 1982, S. 1217–1220.
- ↑ R. F. Genovese, L. A. Dykstra: Tifluadom's effects under electric shock titration and tail-immersion procedures in squirrel monkeys. In: Life Sciences. 10;39(19), 1986, S. 1713–1719.
- ↑ J. D. Leander: Kappa opioid agonists and antagonists: effects on drinking and urinary output. In: Appetite. 5(1), 1984, S. 7–14.
- ↑ H. C. Jackson, R. D. Sewell: The role of opioid receptor sub-types in tifluadom-induced feeding. In: Journal of Pharmacy and Pharmacology. 36(10), 1984, S. 683–686.
- ↑ L. A. Dykstra, D. E. Gmerek, G. Winger, J. H. Woods: Kappa opioids in rhesus monkeys. I. Diuresis, sedation, analgesia and discriminative stimulus effects. In: Journal of Pharmacology and Experimental Therapeutics. 242(2), 1987, S. 413–420.
- ↑ S. J. Cooper, W. R. Moores, A. Jackson, D. J. Barber: Effects of tifluadom on food consumption compared with chlordiazepoxide and kappa agonists in the rat. In: Neuropharmacology. Sep. 1985, PMID 2997653.
- ↑ R. S. Chang, V. J. Lotti, T. B. Chen, M. E. Keegan: Tifluadom, a kappa-opiate agonist, acts as a peripheral cholecystokinin receptor antagonist. In: Neuropharmacology. Sep. 1985, PMID 3027627.
- ↑ Th. Geschwinde: Rauschdrogen. Marktformen und Wirkungsweisen. Springer, Heidelberg/ Dordrecht/ London/ New York 2013, ISBN 978-3-642-30162-9, S. 716 RN 3449.