(−)-α-Bisabolol
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
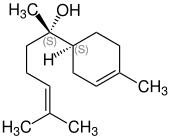
| |||||||||||||||||||
| (−)-α-Bisabolol | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | (−)-α-Bisabolol | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C15H26O | ||||||||||||||||||
| Kurzbeschreibung |
hellgelbe Flüssigkeit[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 222,37 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
0,929 g·cm−3[2] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
(−)-α-Bisabolol (synonym: Levomenol) bezeichnet eine chemische Verbindung aus der Reihe der isomeren Bisabolole. Es handelt sich um einen monocyclischen Sesquiterpen-Alkohol.
Natürliches Vorkommen[Bearbeiten | Quelltext bearbeiten]

(−)-α-Bisabolol ist Hauptbestandteil des Kamillenöls, das aus der traditionell als Heilpflanze verwendeten Echten Kamille (Matricaria chamomilla) gewonnen wird.[3] Die ursprünglich aus Spanien stammende Manzana-Kamille, eine Zuchtform, enthält besonders große Mengen an Bisabolol (bis zu 45 % des ätherischen Öls) und wird deshalb mittlerweile auch in Ländern wie Frankreich, Deutschland und den USA angebaut.[4] Daneben kann α-Bisabolol unter anderem in Gemeiner Schafgarbe (Achillea millefolium),[5] Sideritis mugronensis,[5] Helmkräutern (Scutellaria parvula),[5] Basilikum (Ocimum basilicum),[5] Breitblättrigem Lavendel (Lavandula latifolia)[5] und Alpen-Steinquendel (Acinos alpinus),[5] gefunden werden.
Auch das von Bienen hergestellte Propolis kann beträchtliche Mengen Bisabolol – bis zu ca. 20 % in chinesischem/mongolischem Propolis – enthalten.[6]
Synthese[Bearbeiten | Quelltext bearbeiten]
Enantiomerenreines (−)-α-Bisabolol wird üblicherweise aus natürlichen Quellen gewonnen, gleichwohl sind Syntheserouten zu (−)-α-Bisabolol bekannt; diese gehen häufig von Nerolidol aus.[7]
Racemisches α-Bisabolol, das ebenfalls Verwendung findet, ist meist synthetischen Ursprungs.[3]
Analytik[Bearbeiten | Quelltext bearbeiten]
Zur zuverlässigen qualitativen und quantitativen Bestimmung von (−)-α-Bisabolol kann die Kopplung der Gaschromatographie mit der Massenspektrometrie nach adäquater Probenvorbereitung eingesetzt werden.[8][9] Auch die Anwendung der HPLC kann zur sicheren Identifizierung der Inhaltsstoffe in Pflanzenmaterial dienen.[10]
Unter Einsatz der Dampfraumanalyse eignen sich diese Verfahren auch zum Nachweis in verschiedenen Körperflüssigkeiten wie z. B. Blut, Urin oder auch Gewebeproben und Faeces.[11]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
(−)-α-Bisabolol ist eine farblose bis schwach gelbliche, viskose Flüssigkeit, die unlöslich in Wasser, aber leicht löslich in Alkoholen und Ölen ist. Ihr Geruch wird als schwach blumig-süßlich beschrieben.[3]
Wirkung und Verwendung[Bearbeiten | Quelltext bearbeiten]
Bisabolol wirkt entzündungshemmend auf Haut und Schleimhäute, es wird zur Hautregeneration und Wundheilung beispielsweise nach Verbrennungen oder Sonnenbrand verwendet.[12]
Diese Wirkungen wurden sowohl für den enantiomerenreinen Naturstoff wie auch für das synthetisch zugängliche Racemat beschrieben.[3]
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Eintrag zu Bisabolole in der Consumer Product Information Database
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu BISABOLOL in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2019.
- ↑ a b c d Datenblatt (−)-α-Bisabolol bei Sigma-Aldrich, abgerufen am 17. Juli 2016 (PDF).
- ↑ a b c d e Eintrag zu (−)-α-Bisabolol. In: Römpp Online. Georg Thieme Verlag, abgerufen am 17. Juli 2016.
- ↑ Rolf Franke, Heinz Schilcher (Hrsg.): Chamomile. Industrial Profiles (= Medicinal and aromatic Plants – Industrial Profiles. Band 42). CRC Press, New York NY u. a. 2005, ISBN 0-415-33463-2.
- ↑ a b c d e f ALPHA-BISABOLOL (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 11. September 2021.
- ↑ Yu-Xin Fu, Yuan-Jun Xu, Bin Chen, Yan Li, Li-Ping Luo: Analysis of Volatile Components from Inner Mongolia Propolis by Gas Chromatography-Mass Spectrometry. In: Chinese Journal of Analytical Chemistry. Band 37, Nr. 5, 2009, S. 745–748.
- ↑ Patent DE10246038: Verfahren zur Herstellung von alpha-Bisabolol aus Nerolidol. Veröffentlicht am 15. April 2004, Erfinder: Wilhelm Dr. Pickenhagen, Dietmar Schatkowski.
- ↑ M. Ghasemi, N. Babaeian Jelodar, M. Modarresi, N. Bagheri, A. Jamali: Increase of Chamazulene and α-Bisabolol Contents of the Essential Oil of German Chamomile (Matricaria chamomilla L.) Using Salicylic Acid Treatments under Normal and Heat Stress Conditions. In: Foods. Band 5, Nr. 3, 27. Aug 2016. PMID 28231151
- ↑ E. S. Chernetsova, A. N. Shikov, E. A. Crawford, S. Grashorn, I. Laakso, O. N. Pozharitskaya, V. G. Makarov, R. Hiltunen, B. Galambosi, G. E. Morlock: Characterization of volatile and semi-volatile compounds in green and fermented leaves of Bergenia crassifolia L. by gas chromatography-mass spectrometry and ID-CUBE direct analysis in real time-high resolution mass spectrometry. In: Eur J Mass Spectrom (Chichester). Band 20, Nr. 2, 2014, S. 199–205. PMID 24895781
- ↑ X. Duan, J. Li, J. Cui, H. Li, B. Hasan, X. Xin: Chemical component and in vitro protective effects of Matricaria chamomilla (L.) against lipopolysaccharide insult. In: J Ethnopharmacol. Band 296, 5. Okt 2022, S. 115471. PMID 35716917.
- ↑ L. Perbellini, R. Gottardo, A. Caprini, F. Bortolotti, S. Mariotto, F. Tagliaro: Determination of alpha-bisabolol in human blood by micro-HPLC-ion trap MS and head space-GC-MS methods. In: J Chromatogr B Analyt Technol Biomed Life Sci. Band 812, Nr. 1-2, 5. Dez 2004, S. 373–377. PMID 15556509
- ↑ Ernst Luppold: Matricaria chamomilla – eine alte und neue Arzneipflanze. In: Pharmazie in unserer Zeit. Band 13, Nr. 3, 1984, S. 65, doi:10.1002/pauz.19840130301.