Phthalazin
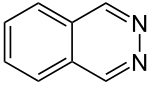
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Phthalazin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H6N2 | ||||||||||||||||||
| Kurzbeschreibung |
blassgelber Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 130,15 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
317 °C[1] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Phthalazin ist eine organische Verbindung, die zu den Heterocyclen (genauer: Heteroaromaten und Diazanaphthalinen) zählt. Die Verbindung besteht aus einem Benzolring, an dem ein Pyridazinring anelliert ist. Phthalazin ist isomer zu Chinazolin, Chinoxalin und Cinnolin.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Phthalazin kann durch Kondensation von ω-Tetrabromorthoxylol mit Hydrazin oder durch Reduktion von Chlorphthalazin mit Phosphor und Iodwasserstoff gewonnen werden.[4] Ebenfalls möglich ist die Darstellung durch Oxidation von 1-Hydrazinophthalazin.[2]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Phthalazin ist ein blassgelber Feststoff, der löslich in Wasser ist.[1] Es besitzt basische Eigenschaften und bildet Additionsprodukte mit Alkyliodiden.[4] Phthalazin und seine Derivate kommen nicht in der Natur vor.[2]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Phthalazin wird als Ausgangsprodukt für verschiedene organischen Synthesen verwendet.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Datenblatt Phthalazine, 98% bei Alfa Aesar, abgerufen am 12. Juni 2013 (Seite nicht mehr abrufbar).
- ↑ a b c Raymond N. Castle: The Chemistry of Heterocyclic Compounds, Condensed Pyridazines Including … John Wiley & Sons, 2009, ISBN 0-470-18848-0, S. 324 ff. (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Datenblatt Phthalazine, 98% bei Sigma-Aldrich, abgerufen am 10. November 2021 (PDF).
- ↑ a b Phthalazines. In: Encyclopædia Britannica. 11. Auflage. Band 21: Payn – Polka. London 1911, S. 545 (englisch, Volltext [Wikisource]).
- ↑ Desmond J. Brown, Jonathan A. Ellman, Edward C. Taylor: Cinnolines and Phthalazines: Chemistry of Heterocyclic Compounds, Supplement II. John Wiley & Sons, 2005, ISBN 0-471-74411-5, S. 175 (eingeschränkte Vorschau in der Google-Buchsuche).
